8. H
2与ICl的反应分两步完成,其能量曲线如图所示。
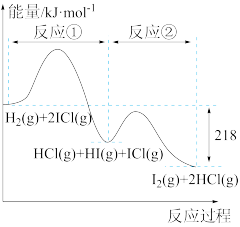
反应①:H
2(g)+2ICl(g)=HCl(g)+HI(g)+ICl(g)
反应②:HCl(g)+HI(g)+ICl(g)=I
2(g)+2HCl(g)
下列有关说法不正确的是
| A.反应①的能垒比反应②的大,所以总反应的反应速率取决于第②步反应 |
| B.反应①、②均是反应物总能量高于生成物总能量 |
| C.H2(g)+2ICl(g)=I2(g)+2HCl(g) △H=-218kJ•mol-1 |
| D.温度升高,活化分子百分数增大,反应碰撞概率增大,反应速率加快 |