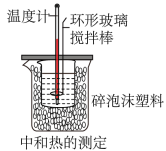
15. 50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)理论上稀强酸、稀强碱反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式:
___________。
(2)倒入NaOH溶液的正确操作是
___________ (从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入
C.一次迅速倒入
(3)实验需要多次测量盐酸和NaOH溶液及反应后溶液的温度,以求出反应前后的平均温度差,每次测量温度后都必须采取的操作是
___________。
(4)大烧杯如不盖硬纸板,求得的中和热数值
___________(填“偏大”“偏小”“无影响”)。
(5)实验中改用60 mL 0.50 mol·L
-1盐酸进行反应,与上述实验相比,所放出的热量
___________(填“相等”、“不相等”),所求中和热
___________(填“相等”、“不相等”),简述理由
___________。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
___________(填“偏大”、“偏小”“无影响”)。