第30届(2016年11月26日)中国化学奥林匹克(决赛)理论试题(试题解析)
全国
高三
竞赛
2021-07-03
243次
整体难度:
困难
考查范围:
物质结构与性质、化学反应原理、化学实验基础、有机化学基础、竞赛
第30届(2016年11月26日)中国化学奥林匹克(决赛)理论试题(试题解析)
全国
高三
竞赛
2021-07-03
243次
整体难度:
困难
考查范围:
物质结构与性质、化学反应原理、化学实验基础、有机化学基础、竞赛
一、解答题 添加题型下试题
解答题-结构与性质
|
较难(0.4)
解题方法
1. (1)简要解释为什么水溶液中HCN是弱酸,而液态HCN的酸性相比其水溶液显著增强________ 。
(2) Hg2+离子具有亲硫性,可与二硫代氨基甲酸盐形成[Hg(S2CNEt2)2]的二聚体,请画出该二聚体的立体结构________ ,并指出中心原子的杂化方式________ 。
异烟酰腙的结构如下:
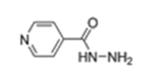
它与2-乙酰基吡啶反应生成一种配体L。 将一定量的四水醋酸镍、配体L以及4,4'-联吡啶溶解在1:1的乙醇-水的混合溶剂中回流2小时,冷却至室温,析出物质经洗涤干燥后得到褐色片状晶体M。分析结果表明,M中N元素含量为21.0%。
(3)画出配体L的结构,请在图中用*号标出配位原子________ 。
(4)通过计算,写出配合物M符合IUPAC规则的分子式,画出M的所有几何异构体的结构,在每个几何异构体下面标注I、II、 III┄┄等,指出哪些几何异构体存在旋光异构现象________ ?哪个几何异构体稳定性最高________ ?请说明理由________ 。
(5)说明4,4′-联吡啶的作用________ 。
(2) Hg2+离子具有亲硫性,可与二硫代氨基甲酸盐形成[Hg(S2CNEt2)2]的二聚体,请画出该二聚体的立体结构
异烟酰腙的结构如下:

它与2-乙酰基吡啶反应生成一种配体L。 将一定量的四水醋酸镍、配体L以及4,4'-联吡啶溶解在1:1的乙醇-水的混合溶剂中回流2小时,冷却至室温,析出物质经洗涤干燥后得到褐色片状晶体M。分析结果表明,M中N元素含量为21.0%。
(3)画出配体L的结构,请在图中用*号标出配位原子
(4)通过计算,写出配合物M符合IUPAC规则的分子式,画出M的所有几何异构体的结构,在每个几何异构体下面标注I、II、 III┄┄等,指出哪些几何异构体存在旋光异构现象
(5)说明4,4′-联吡啶的作用
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
较难(0.4)
2. 某白色固体A室温时不稳定,而在水中稳定。A具有弱碱性和较显著的还原性,分子只有1个镜面,有顺式和反式异构体。在酸性条件下A分解为三种产物B、C和D,其中B为二元化合物,与CO2是等电子体。在中性溶液中,A与亚硝酸作用可生成化合物E和C.纯净的E是一种无色晶体,为二元酸(pKa1=6.9,pKa2= 11.6)。E的阴离子有C2轴和与此轴垂直的镜面,其钠盐F可通过金属钠与硝酸铵1:1反应而成,也可在乙醇介质中由A与RONO和乙醇钠反应而成。
(1)写出以上两种方法合成F的反应方程式________ 。
(2)画出A的顺式和反式异构体的立体结构________ 。
(3)干燥的E晶体极易爆炸,水溶液中较稳定,但仍会逐渐分解,写出其分解反应方程式________ 。
(4)E的异构体G是弱酸,pKa=6.6,画出G的路易斯结构________ 。
(5)用液态N2O4与F反应生成H,此法得到的H为β构型,其中Na的百分含量为37.69%。存在一个O- O键。推断H的化学式并画出其阴离子的结构(孤对电子不需标出)________ 、________ 。
(6)H的α构型同分异构体(没有O-O键)可由A与BuONO2和甲醇钠在甲醇介质中反应而成,写出α-H的制备反应方程式________ 。
(1)写出以上两种方法合成F的反应方程式
(2)画出A的顺式和反式异构体的立体结构
(3)干燥的E晶体极易爆炸,水溶液中较稳定,但仍会逐渐分解,写出其分解反应方程式
(4)E的异构体G是弱酸,pKa=6.6,画出G的路易斯结构
(5)用液态N2O4与F反应生成H,此法得到的H为β构型,其中Na的百分含量为37.69%。存在一个O- O键。推断H的化学式并画出其阴离子的结构(孤对电子不需标出)
(6)H的α构型同分异构体(没有O-O键)可由A与BuONO2和甲醇钠在甲醇介质中反应而成,写出α-H的制备反应方程式
【知识点】 电离平衡常数及影响因素解读
您最近一年使用:0次
填空题
|
较难(0.4)
3. 某金属M的氧化物A是易挥发的液体,有毒,微溶于水。在氯化氢气氛中蒸发A的盐酸溶液(含1.000 g的A)得到1.584 g晶体MCl3·3H2O。
(1)假定转化反应按化学计量比进行,通过计算确定A的化学式________ ,并写出金属M的价电子构型________ 。从精炼镍的阳极泥提取M的步骤为:
①用王水处理溶解Pt、Pd和Au;
②固体不溶物与碳酸铅共热,然后用稀硝酸处理除去可溶物B;
③剩余固体不溶物与硫酸氢钠共熔,用水浸取除去可溶物C;
④留下的固体不溶物与过氧化钠共熔,用水浸取,过滤。滤液中含有M的盐D,D为Na2SO4型电解质,无水D中氧含量为30.32%;
⑤往D溶液中通入Cl2,加热,收集40- 50 °C的馏分,得到A.A收集在盐酸中,加热得到E的溶液,E中Cl含量为67.14%;
⑥溶液E中加入适量NH4Cl溶液得到沉淀F,F中Cl含量为57.81%。F在氢气中燃烧即得到金属M。
已知φ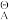 (NO
(NO /NO)= 0.957V,φ
/NO)= 0.957V,φ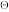 ([PtCl4]2-/Pt)= 0.755V,φ
([PtCl4]2-/Pt)= 0.755V,φ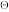 (PtCl6]2-/[PtCl4]2-= 0.680V,所有离子活度系数为1.00。
(PtCl6]2-/[PtCl4]2-= 0.680V,所有离子活度系数为1.00。
(2)写出步骤(1)中除去Pt的化学反应方程式________ ,计算该反应在298 K下的K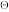
________ 。
(3)写出步骤(2)中除去银的化学反应方程式________ 。
(4)D、E、F中均只有1个金属原子,试通过计算确定D、E、F的化学式________ 、________ 、________ 。
(1)假定转化反应按化学计量比进行,通过计算确定A的化学式
①用王水处理溶解Pt、Pd和Au;
②固体不溶物与碳酸铅共热,然后用稀硝酸处理除去可溶物B;
③剩余固体不溶物与硫酸氢钠共熔,用水浸取除去可溶物C;
④留下的固体不溶物与过氧化钠共熔,用水浸取,过滤。滤液中含有M的盐D,D为Na2SO4型电解质,无水D中氧含量为30.32%;
⑤往D溶液中通入Cl2,加热,收集40- 50 °C的馏分,得到A.A收集在盐酸中,加热得到E的溶液,E中Cl含量为67.14%;
⑥溶液E中加入适量NH4Cl溶液得到沉淀F,F中Cl含量为57.81%。F在氢气中燃烧即得到金属M。
已知φ
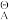 (NO
(NO /NO)= 0.957V,φ
/NO)= 0.957V,φ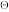 ([PtCl4]2-/Pt)= 0.755V,φ
([PtCl4]2-/Pt)= 0.755V,φ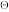 (PtCl6]2-/[PtCl4]2-= 0.680V,所有离子活度系数为1.00。
(PtCl6]2-/[PtCl4]2-= 0.680V,所有离子活度系数为1.00。(2)写出步骤(1)中除去Pt的化学反应方程式
(3)写出步骤(2)中除去银的化学反应方程式
(4)D、E、F中均只有1个金属原子,试通过计算确定D、E、F的化学式
【知识点】 核外电子排布的表示形式
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-实验探究题
|
困难(0.15)
4. 镍是钢中的重要元素之一,镍的加入可以增加钢的硬度、弹性、延展性和抗腐蚀性。某实验室有两份含Ni钢样,1号钢样中Ni的质量分数为0.362%,2号钢样Ni含量未知。实验人员用过二硫酸铵-丁二酮肟吸光光度法对钢样中Ni含量进行测定:取一定质量的钢样在通风柜中加入适量硝酸,加热溶解,转移至100 mL容量瓶,定容摇匀。移取10.00 mL试样溶液于50 mL容量瓶中,依次加入酒石酸钠、NaOH、丁二酮肟和过二硫酸铵。丁酮肟加入后有浑浊现象,加入过二硫酸铵后溶解成酒红色溶液,再加水定容。
(1)请写出镍溶解及氧化过程中的离子方程式_________ ,并说明酒石酸钠和NaOH的作用_________ 。
(2) 1号钢样经上述分解步骤和显色反应后制备的溶液,利用普通吸光光度法进行检测。使用2 cm吸收池于530 nm处(ε = 6.60 × 103 L·mol-1·cm-1 )测量,欲使测量的相对误差最小,称取1号钢样的质量应为多少_________ ?
(3)请指出(2)中普通吸光光度法使用的参比溶液的组成_________ ,为何使用该溶液作为参比溶液_________ ?
(4)以示差吸光光度法测定2号钢样中Ni含量,称取0.382 g2号钢样,经与测定1号钢样同样步骤配制的溶液,使用2 cm吸收池,波长选择530 nm,以4-2中配制的1号钢样显色反应后的溶液作参比液,并以此调节透射比为100%,此时测得2号钢样显色后溶液的透射比为T= 31.4%,计算2号钢样中Ni的质量分数_________ 。
(1)请写出镍溶解及氧化过程中的离子方程式
(2) 1号钢样经上述分解步骤和显色反应后制备的溶液,利用普通吸光光度法进行检测。使用2 cm吸收池于530 nm处(ε = 6.60 × 103 L·mol-1·cm-1 )测量,欲使测量的相对误差最小,称取1号钢样的质量应为多少
(3)请指出(2)中普通吸光光度法使用的参比溶液的组成
(4)以示差吸光光度法测定2号钢样中Ni含量,称取0.382 g2号钢样,经与测定1号钢样同样步骤配制的溶液,使用2 cm吸收池,波长选择530 nm,以4-2中配制的1号钢样显色反应后的溶液作参比液,并以此调节透射比为100%,此时测得2号钢样显色后溶液的透射比为T= 31.4%,计算2号钢样中Ni的质量分数
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
解题方法
5. 近年来,光电材料领域有一类有机无机杂化材料获得突破,某该类材料由三种离子组成,其晶体的晶胞有4条沿体对角线的C3轴,A为显正价的阳离子或基团, 其分数坐标为: (0,0, 0); B为金属Pb2+,Sn2+等阳离子,其分数坐标为: (1/2, 1/2, 1/2); X为Cl-、Br-、I-等卤素离子,分数坐标为:(0, 1/2, 1/2); (1/2,0, 1/2); (1/2, 1/2, 0)。
(1)分别以 、●和○代表A、B和X离子,画出该晶体的正当晶胞
、●和○代表A、B和X离子,画出该晶体的正当晶胞________ 。
(2)写出A为CH3NH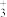 、B为Pb2+、X为I-形成晶体的化学式
、B为Pb2+、X为I-形成晶体的化学式________ 。
(3)指出A、B、X的配位数________ ,并推断该晶体是否存在分离的配位离子________ 。
(4)某该类晶体材料的带隙Eg为1.55eV,计算其吸收光的波长________ 。
(5)通过改变晶体中的阳离子和/或阴离子,可能对其光电性能进行调节,但是为了使该晶体结构保持稳定,离子尺寸受到限制,即要求填隙离子半径与空隙半径比b在一定范围。现有一同类晶体,B位Pb2+半径为133 pm, X位I-半径为203 pm,如b为0.9- 1.05,试估算A位阳离子的半径范围________ 。
(6)此类有机/无机杂化薄膜太阳能电池材料的优异特性源于其无机组分和有机组分特性的优异组合,请分别指出各自特性所起的作用________ 。
(1)分别以
 、●和○代表A、B和X离子,画出该晶体的正当晶胞
、●和○代表A、B和X离子,画出该晶体的正当晶胞(2)写出A为CH3NH
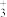 、B为Pb2+、X为I-形成晶体的化学式
、B为Pb2+、X为I-形成晶体的化学式(3)指出A、B、X的配位数
(4)某该类晶体材料的带隙Eg为1.55eV,计算其吸收光的波长
(5)通过改变晶体中的阳离子和/或阴离子,可能对其光电性能进行调节,但是为了使该晶体结构保持稳定,离子尺寸受到限制,即要求填隙离子半径与空隙半径比b在一定范围。现有一同类晶体,B位Pb2+半径为133 pm, X位I-半径为203 pm,如b为0.9- 1.05,试估算A位阳离子的半径范围
(6)此类有机/无机杂化薄膜太阳能电池材料的优异特性源于其无机组分和有机组分特性的优异组合,请分别指出各自特性所起的作用
【知识点】 物质结构与性质综合考查解读 晶胞的有关计算解读
您最近一年使用:0次
6. 甲醇既是重要的化工原料,又是一种很有发展前途的代用燃料,甲醇分解制氢已经成为制取氢气的重要途径,它具有投资省、流程短、操作简便、氢气成本相对较低等特点。我们可以根据298 K时的热力学数据(如下表)对于涉及甲醇的各种应用进行估算、分析和预判。
(1)估算400.0K,总压为100.0 kPa时甲醇裂解制氢反应的平衡常数_________ (设反应的ΔrH 和ΔrS
和ΔrS 不随温度变化,下同)。
不随温度变化,下同)。
(2)将0.426 g甲醇置于体积为1.00 L的抽真空刚性容器中,维持温度为298 K时,甲醇在气相与液相的质量比为多少_________ ?已知甲醇在大气中的沸点为337.7 K。
(3)由甲醇制氢的实际生产工艺通常是在催化剂的作用下利用水煤气转化反应与裂解反应耦合,以提高甲醇的平衡转化率。请写出耦合后的总反应方程式_________ ,并求总压为100.0kPa,甲醇与水蒸气体积进料比为1 : 1时,使甲醇平衡转化率达到99.0%所需的温度_________ 。
(4)设想利用太阳能推动反应进行,可将甲醇裂解反应设计为光电化学电池,请写出电极反应_________ ,并指出需要解决的两个最关键的问题_________ 。
(5)有研究者对甲醇在纳米Pd催化剂上的分解反应提出如下反应机理:
CH3OH(g)+ S CH3OH(ad)
CH3OH(ad)
CH3OH(ad) CH3O(ad) + H(ad)
CH3O(ad) + H(ad)
CH3O(ad) CH2O(ad) + H(ad)
CH2O(ad) + H(ad)
CH2O(ad) CHO(ad) + H(ad)
CHO(ad) + H(ad)
CHO(ad)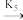 CO(ad) + H(ad)
CO(ad) + H(ad)
CO(ad) CO(g)+ S
CO(g)+ S
2H(ad)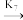 H2(g)
H2(g)
以上各式中“S”表示表面活性中心,“g”表示气态,“ad” 表示吸附态。设S的浓度仅随甲醇吸附而变化,请根据以上机理用稳态近似推导反应速率方程_________ ,并对结果进行讨论_________ 。
(6)金属催化剂的表面活性与表面原子的能量有关,假设表面为完整的二维结构,表面能量由原子的断键引起。请估算Pd金属(110)面(即与二重轴垂直的面)的单位表面能量_________ 。已知Pd为立方最密堆积,Pd原子半径为179 pm,原子化热为351.6 kJ·mol-1。
| 物质 | H2(g) | O2(g) | CO(g) | CO2(g) | H2O(g) | H2O(l) | CH3OH(l) | CH3OH(g) |
-ΔfH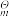 /kJ·mol-1 /kJ·mol-1S 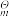 /J·mol-1·K-1 /J·mol-1·K-1 | 0 130.68 | 0 205.14 | 110.52 197.67 | 393.51 213.74 | 285.83 69.91 | 241.82 18883 | 238.66 126.80 | 200.66 239.81 |
(1)估算400.0K,总压为100.0 kPa时甲醇裂解制氢反应的平衡常数
 和ΔrS
和ΔrS 不随温度变化,下同)。
不随温度变化,下同)。(2)将0.426 g甲醇置于体积为1.00 L的抽真空刚性容器中,维持温度为298 K时,甲醇在气相与液相的质量比为多少
(3)由甲醇制氢的实际生产工艺通常是在催化剂的作用下利用水煤气转化反应与裂解反应耦合,以提高甲醇的平衡转化率。请写出耦合后的总反应方程式
(4)设想利用太阳能推动反应进行,可将甲醇裂解反应设计为光电化学电池,请写出电极反应
(5)有研究者对甲醇在纳米Pd催化剂上的分解反应提出如下反应机理:
CH3OH(g)+ S
 CH3OH(ad)
CH3OH(ad)CH3OH(ad)
 CH3O(ad) + H(ad)
CH3O(ad) + H(ad)CH3O(ad)
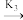 CH2O(ad) + H(ad)
CH2O(ad) + H(ad)CH2O(ad)
 CHO(ad) + H(ad)
CHO(ad) + H(ad)CHO(ad)
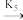 CO(ad) + H(ad)
CO(ad) + H(ad)CO(ad)
 CO(g)+ S
CO(g)+ S2H(ad)
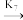 H2(g)
H2(g)以上各式中“S”表示表面活性中心,“g”表示气态,“ad” 表示吸附态。设S的浓度仅随甲醇吸附而变化,请根据以上机理用稳态近似推导反应速率方程
(6)金属催化剂的表面活性与表面原子的能量有关,假设表面为完整的二维结构,表面能量由原子的断键引起。请估算Pd金属(110)面(即与二重轴垂直的面)的单位表面能量
您最近一年使用:0次
四、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
7. 醇转化为相应的卤代烃,一类重要的反应。下列由醇制备相应氯代烃的方法具有高的立体选择性。其反应机理可以用下图表示。
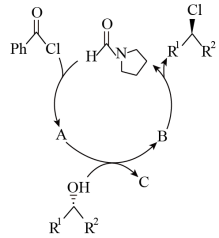
(1)请给出活性中间体A、B及另一产物C的结构简式___________ 。标出电子的流向,并表明其立体化学___________ 。
(2)该反应的活性大小主要取决于___________ 。如果用p-O2NC6H4COCl代替PhCOCl,该反应的速率将___________ (增大/减小/不变)。

(1)请给出活性中间体A、B及另一产物C的结构简式
(2)该反应的活性大小主要取决于
您最近一年使用:0次
五、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
解题方法
8. 串联反应,也称多米诺(domino)反应,即多步合成反应结合在一种合成操作中完成,无需额外的试剂或反应条件变化;中间体无需分离,随后转化为能量较低的物种。化合物I是许多药物中具有生物活性的天然产物,具有降糖、抗癌、抗病毒、抗肿瘤、抗疟药、抑制HIV-1活性等功效,其制备方法如下:

原料D形成活性中间体F; F与E通过下列串联反应,形成化合物I:
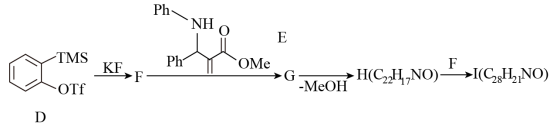
如果用异腈J代替E,则得到产物K:

(1)请写出F、G、H、I及K的结构简式______ 、______ 、______ 、______ 、______ 。
(2)给出D→F,F→G,G→H及H→I的具体反应类型______ 、______ 、______ 、______ 。

原料D形成活性中间体F; F与E通过下列串联反应,形成化合物I:

如果用异腈J代替E,则得到产物K:

(1)请写出F、G、H、I及K的结构简式
(2)给出D→F,F→G,G→H及H→I的具体反应类型
您最近一年使用:0次
六、填空题 添加题型下试题
填空题
|
困难(0.15)
解题方法
9. 2-吡喃酮(N)的衍生物广泛存在于自然界,有强心、抑菌等作用。化合物L真空热裂解,经中间体M转化为N。M是具有一定稳定性和强反应活性的非环状分子。
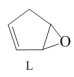
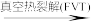 M(C5H4O2)→
M(C5H4O2)→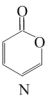
利用该反应原理,起始原料O通过系列反应,成功合成2-吡喃酮衍生物T。Q→R的反应具有很好的立体选择性。
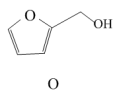

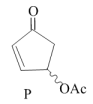
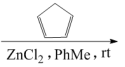 Q
Q R(C17H16O2)
R(C17H16O2) S
S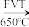 T(C12H10O3) 备注:DCM=CH2Cl2
T(C12H10O3) 备注:DCM=CH2Cl2
(1)请写出M及Q、R、S、T的结构简式(如为立体选择性反应产物,须表明立体化学结构)_____ 、_____ 、_____ 、_____ 、_____ 。
(2)判断化合物N有无芳香性_____ ,并简述理由_____ 。
(3)请比较化合物N及1,3-环己二烯作为双烯体发生Diels-Alder反应的相对活性大小_____ ,并简述理由_____ 。
(4)请指出在Q → R反应中,PhOH的作用_____ 。

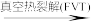 M(C5H4O2)→
M(C5H4O2)→
利用该反应原理,起始原料O通过系列反应,成功合成2-吡喃酮衍生物T。Q→R的反应具有很好的立体选择性。



 Q
Q R(C17H16O2)
R(C17H16O2) S
S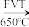 T(C12H10O3) 备注:DCM=CH2Cl2
T(C12H10O3) 备注:DCM=CH2Cl2(1)请写出M及Q、R、S、T的结构简式(如为立体选择性反应产物,须表明立体化学结构)
(2)判断化合物N有无芳香性
(3)请比较化合物N及1,3-环己二烯作为双烯体发生Diels-Alder反应的相对活性大小
(4)请指出在Q → R反应中,PhOH的作用
您最近一年使用:0次
试卷分析
整体难度:较难
考查范围:物质结构与性质、化学反应原理、化学实验基础、有机化学基础、竞赛
试卷题型(共 9题)
题型
数量
解答题
5
填空题
4
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、解答题 | |||
| 1 | 0.4 | 物质结构与性质综合考查 利用杂化轨道理论判断化学键杂化类型 配合物的应用 | 结构与性质 |
| 4 | 0.15 | 酸碱中和滴定原理的应用 探究物质组成或测量物质的含量 | 实验探究题 |
| 5 | 0.4 | 物质结构与性质综合考查 晶胞的有关计算 | 结构与性质 |
| 6 | 0.15 | 化学平衡的移动及其影响因素 化学平衡常数的有关计算 原电池电极反应式书写 晶胞的有关计算 | 原理综合题 |
| 8 | 0.65 | 有机推断综合考查 | 有机推断题 |
| 二、填空题 | |||
| 2 | 0.4 | 电离平衡常数及影响因素 | |
| 3 | 0.4 | 核外电子排布的表示形式 | |
| 7 | 0.65 | 醇类的化学性质 有机化学 | |
| 9 | 0.15 | 有机物的推断 有机合成综合考查 | |



