8. 氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用。
(1)NaH是一种生氢剂,NaH与H
2O反应放出H
2.NaH含有的化学键为
________(填“离子键”或“共价键”),NaH与H
2O反应的化学方程式为
________________.
(2)写出实验室用锌与稀硫酸反应制取H
2的离子方程式:
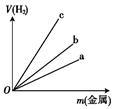
_________.图中三根曲线表示锌、铝、铁分别与稀硫酸反应时金属质量与H
2体积的关系,其中能表示铝的是
________(填“a”“b”或“c”).
(3)金属-有机框架物(MOFs)储氢材料是由金属氧化物团簇通过有机高分子链组装形成的晶态材料.MOFs储氢材料比表面积大,空隙率高,储氢容量大,其储氢和放氢的原理可表示为MOFs(s)+nH
2(g)

(H
2)
nMOFs(s),ΔH<0,则储氢时的适宜条件为
________(填字母).
(4)某硝酸厂处理尾气中的NO的方法是用H
2将NO还原为N
2.

已知:H
2还原NO生成氮气和水蒸气的热化学方程式是
_________________________.
(5)一定条件下,用H
2将二氧化碳转化为甲烷的反应如下:
CO
2(g) + 4H
2(g)

CH
4(g) + 2H
2O(g)
向一容积为2 L的恒容密闭容器中充入一定量的CO
2和H
2,在300℃时发生上述反应,10 min后达到平衡时各物质的浓度分别为: CO
2为0.2 mol·L
-1, H
2为0.8 mol·L
-1, CH
4为0.8 mol·L
-1, H
2O为1.6 mol·L
-1.
①0~10 min内v(H
2)=
_______________.
②300℃时上述反应的平衡常数K=
___________,若200℃时该反应的平衡常数K=64.8,则该反应的ΔH
__________(填“>”或“<”)0.