2015届四川省广安市高三二诊理综化学试卷
四川
高三
阶段练习
2017-07-26
565次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质、有机化学基础
2015届四川省广安市高三二诊理综化学试卷
四川
高三
阶段练习
2017-07-26
565次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质、有机化学基础
一、单选题 添加题型下试题
单选题
|
容易(0.94)
1. 化学与科技、社会、生产、生活密切相关。下列有关说法正确的是
| A.氟利昂和NOX都能破坏臭氧层,从而导致“温室效应” |
| B.针对H 7 N 9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、活性银离子、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学核心 |
| C.光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 |
| D.肌红蛋白、蚕丝、过氧化氢酶、鱼油充分水解后不能全部都得到氨基酸 |
【知识点】 化学与STSE
您最近一年使用:0次
单选题
|
适中(0.64)
2. 下列说法正确的是
| A.分馏、蒸馏、煤的液化都是物理变化,干馏、裂化、裂解都是化学变化 |
| B.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 |
| C.需要加热的反应不一定是吸热反应 |
| D.根据是否具有丁达尔效应, 将分散系分为溶液、浊液和胶体 |
【知识点】 物质的分类
您最近一年使用:0次
单选题
|
较难(0.4)
3. 能正确表示下列反应离子方程式的是( )
| A.向NaAlO2溶液中通入过量CO2制Al(OH)3:2AlO2—+CO2+3H2O===2Al(OH)3↓+CO32— |
| B.双氧水中加入稀硫酸和KI溶液:2I-+H2O2+2H+===I2+O2↑+2H2O |
| C.Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO42—+Ba2++3OH-===Fe(OH)3↓+BaSO4↓ |
| D.草酸使酸性KMnO4溶液褪色:5H2C2O4+2MnO4—+6H+===2Mn2++10CO2↑+8H2O |
【知识点】 离子反应的发生及书写
您最近一年使用:0次
2016-12-09更新
|
325次组卷
|
4卷引用:2015届四川省广安市高三二诊理综化学试卷
2015届四川省广安市高三二诊理综化学试卷2017届辽宁省沈阳东北育才学校高三上模拟二化学试卷(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化 第2讲 离子反应和离子方程式【押题专练】(已下线)2019届高考热点题型和提分秘籍 第二章 化学物质及其变化 第2讲 离子反应 (题型专练)
单选题
|
适中(0.64)
4. 下列有关实验操作及现象与相应结论都正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 将Cl2通入品红溶液中,品红溶液褪色 | 证明Cl2有还原性 |
| B | 蔗糖溶液在硫酸存在下水浴加热一段时间后,再与银氨溶液混合水浴加热,无银镜出现 | 蔗糖没有水解 |
| C | 向鸡蛋清溶液中加入饱和硫酸铵溶液,有白色沉淀生成 | 蛋白质变性 |
| D | 铝箔在酒精灯火焰上,加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| A.A | B.B | C.C | D.D |
【知识点】 化学实验基础
您最近一年使用:0次
单选题
|
适中(0.64)
5. 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 mol[Zn(NH3)4]Cl2中含有σ键的数目为16 NA |
| B.电解精炼粗铜时,每转移NA电子,阳极上溶解的铜原子数必为0.5 NA |
| C.3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA |
| D.60 g石英晶体中含有的Si—O键数目为2NA |
【知识点】 化学计量
您最近一年使用:0次
单选题
|
适中(0.64)
6. 向甲、乙、丙三个密闭容器中充入一定量的X和Y,发生反应:x(g)+aY(g) 2Z(g)。各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以下图和下表表示。下列说法不正确的是
2Z(g)。各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以下图和下表表示。下列说法不正确的是
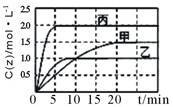
 2Z(g)。各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以下图和下表表示。下列说法不正确的是
2Z(g)。各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以下图和下表表示。下列说法不正确的是
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.0molX 0.5molY | 1.0molX 0.5molY | 4.0molX 2.0molY |
| A.该反应温度升高,平衡常数减小 |
| B.20min内甲容器中反应的平均速率: v(X) = 0.075mol·(L·min)-1 |
| C.其他条件不变,若缩小乙的体积,Y的转化率不变 |
| D.10min时,其他条件不变,向乙容器中再加入2 molZ,平衡向逆反应方向移动 |
【知识点】 化学平衡
您最近一年使用:0次
单选题
|
较难(0.4)
7. 下列物质的量浓度关系不正确的是
| A.常温下0.1 mol/L的下列溶液①NH4Al(SO4)2 ②NH3·H2O③NH4Cl ④CH3COONH4中,c(NH4+)由大到小的顺序是:①>③>④>② |
| B.将0.1 mol·L-1的NaHS和0.1 mol·L-1Na2S溶液等体积混合:c(S2-)+2c(OH-)=2c(H+)+ c(HS-)+3c(H2S) |
| C.将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶解于同一烧杯的水中,制得1 L溶液:c(CH3COO-)+c(OH-)=0.10 mol·L-1 |
| D.已知HClO+Na2CO3=NaClO+NaHCO3,在等物质的量浓度等体积次氯酸溶液与碳酸钠溶液混合溶液中:c(HClO) + c(H+)+ c(H2CO3)="=" c(OH-) + c(CO32-) |
【知识点】 盐类的水解
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
较难(0.4)
8. 有A、B、C、D、E、F、G、H八种原子序数依次增大的元素(原子序数均小于30)。A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,A、E同主族,F的基态原子s能级的电子总数与p能级的电子数相等,B、G同族,H的基态原子的3d轨道电子数是4s电子数的4倍。请回答下列问题:
(1)H元素在周期表中属于____ 区。G的基态原子电子排布式为____ CD2中C的杂化类型是___________
(2)下列说法不正确的是____ 。
a.B2A2分子中含有σ键和π键
b.B2A2分子的沸点明显低于A2D2分子
c.A2D2分子的空间构型为直线形
d.B、C、D的电负性由大到小的顺序为D>C>B
e.B、C、D的第一电离能由大到小的顺序为D>C>B
f.H2+能与BD分子形成[H(BD)4]2+,其原因是BD分子中含有空轨道
g.B和G的单质能形成相同类型的晶体,其熔点B > G
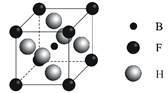
(3)由B、F、H三种元素形成的一种具有超导性的晶体,B位于F和H原子紧密堆积所形成的空隙当中。晶胞如图所示,该晶体的化学式为___________
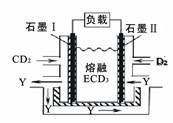
(4)CD2、D2和熔融ECD3可制作燃料电池,其原理如下图所示。该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,石墨Ⅰ电极反应式为___________
(1)H元素在周期表中属于
(2)下列说法不正确的是
a.B2A2分子中含有σ键和π键
b.B2A2分子的沸点明显低于A2D2分子
c.A2D2分子的空间构型为直线形
d.B、C、D的电负性由大到小的顺序为D>C>B
e.B、C、D的第一电离能由大到小的顺序为D>C>B
f.H2+能与BD分子形成[H(BD)4]2+,其原因是BD分子中含有空轨道
g.B和G的单质能形成相同类型的晶体,其熔点B > G
(3)由B、F、H三种元素形成的一种具有超导性的晶体,B位于F和H原子紧密堆积所形成的空隙当中。晶胞如图所示,该晶体的化学式为

(4)CD2、D2和熔融ECD3可制作燃料电池,其原理如下图所示。该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,石墨Ⅰ电极反应式为

您最近一年使用:0次
三、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
9. 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,其熔点为-59 ℃,沸点为11.0 ℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60 ℃时反应制得。某学生拟用下图所示装置模拟工业制取并收集ClO2。
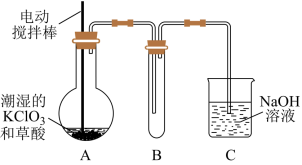
(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、__________ 。
(2)B装置必须放在冰水浴中,其原因是______________________________ 。
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图
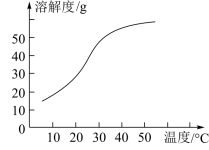
获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③______________________________________ ;
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:_______ 。
②若步骤2所得溶液放置时间太长,则测定结果____________ (填“偏高”、“偏低”或“不变”)
③ClO2溶液的浓度为________ g·L-1(用含字母的代数式表示)。

(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、
(2)B装置必须放在冰水浴中,其原因是
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图

获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:
②若步骤2所得溶液放置时间太长,则测定结果
③ClO2溶液的浓度为
您最近一年使用:0次
解答题-有机推断题
|
困难(0.15)
解题方法
10. 有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
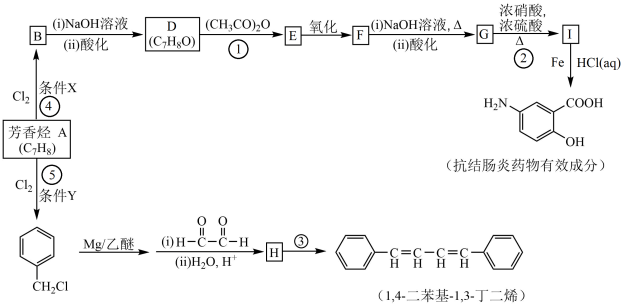
已知:
Ⅰ.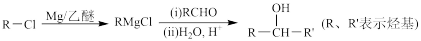
Ⅱ.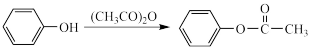
Ⅲ.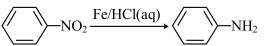
Ⅳ.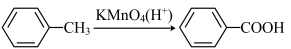
(1)抗结肠炎药物有效成分分子中的含氧官能团名称是______ 。
(2)D的结构简式是_______________
(3)写出F与NaOH反应的化学方程式______ 。
(4)下列说法正确的是________ (填选项字母)。
(5)检验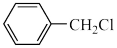 有氯原子的方法是
有氯原子的方法是______ 。
(6)③的化学方程式是______ 。
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的同分异构体的结构简式:______ 。
a.结构中有两个苯环,无其它环状结构
b.苯环上的一硝基取代产物有两种
c.其核磁共振氢谱有3种峰,峰面积之比为3∶2∶2

已知:
Ⅰ.
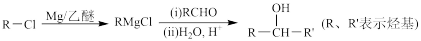
Ⅱ.
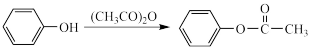
Ⅲ.
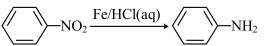
Ⅳ.
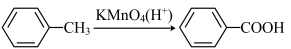
(1)抗结肠炎药物有效成分分子中的含氧官能团名称是
(2)D的结构简式是
(3)写出F与NaOH反应的化学方程式
(4)下列说法正确的是
| A.④的反应条件X和⑤的反应条件Y完全相同 |
| B.①②④⑤反应类型相同 |
| C.G不可以发生缩聚反应 |
| D.设计D→E和F→G两步反应的目的是防止酚羟基被氧化 |
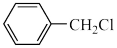 有氯原子的方法是
有氯原子的方法是(6)③的化学方程式是
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的同分异构体的结构简式:
a.结构中有两个苯环,无其它环状结构
b.苯环上的一硝基取代产物有两种
c.其核磁共振氢谱有3种峰,峰面积之比为3∶2∶2
您最近一年使用:0次
解答题-工业流程题
|
困难(0.15)
解题方法
11. 研究发现铜具有独特的杀菌功能, 能较好地抑制病菌的生长。现有工业上由辉铜矿石(主要成分Cu2S)的冶炼铜两种方案:
Ⅰ 火法炼铜在1200℃发生的主要反应为:
①2Cu2S+3O2=2Cu2O+2SO2 ②2Cu2O+Cu2S= 6Cu+SO2↑
此方案的尾气可以用表中方法处理
Ⅱ“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强;利用Fe2(SO4)3作氧化剂溶解辉铜矿石,溶液酸性又进一步增强,过滤未溶解完的辉铜矿石,在滤液中加入足量的铁屑,待反应完全后过滤出铜和剩余的铁屑,得溶液Xml(设整个过程中其它杂质不参与反应,不考虑溶液离子水解)。其流程如图:

(1)Ⅱ相对于Ⅰ的优点是______________________________ 。(说一点即可)
(2)Ⅰ中反应2Cu2O+Cu2S= 6Cu+SO2↑氧化剂是________
(3)已知CO的燃烧热283. 0 kJ·mol-1,写出S(g)与O2(g)反应生成SO2(g)的热化学方程式___________ 。
(4)若用Ⅰ中方法2吸收尾气,则开始时阳极的电极反应式为________________ 。
(5)写出Ⅱ中黄铁矿氧化过程的化学反应方程式______________________________
(6)假设Ⅱ中每一步都完全反应,消耗掉标况下空气5×22.4VL(氧气体积分数为20%),则所得c(Fe2+)=________________ (可以写表达式)。
Ⅰ 火法炼铜在1200℃发生的主要反应为:
①2Cu2S+3O2=2Cu2O+2SO2 ②2Cu2O+Cu2S= 6Cu+SO2↑
此方案的尾气可以用表中方法处理
| 方法1 | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫,其部分热化学方程式为: 2CO(g)+SO2(g)= S(g)+2CO2(g) ΔH="+8." 0 kJ·mol-1 2H2(g)+SO2(g)= S(g)+2H2O(g) ΔH="+90." 4 kJ·mol-1 |
| 方法2 | 用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸 |

(1)Ⅱ相对于Ⅰ的优点是
(2)Ⅰ中反应2Cu2O+Cu2S= 6Cu+SO2↑氧化剂是
(3)已知CO的燃烧热283. 0 kJ·mol-1,写出S(g)与O2(g)反应生成SO2(g)的热化学方程式
(4)若用Ⅰ中方法2吸收尾气,则开始时阳极的电极反应式为
(5)写出Ⅱ中黄铁矿氧化过程的化学反应方程式
(6)假设Ⅱ中每一步都完全反应,消耗掉标况下空气5×22.4VL(氧气体积分数为20%),则所得c(Fe2+)=
您最近一年使用:0次
试卷分析
整体难度:较难
考查范围:化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质、有机化学基础
试卷题型(共 11题)
题型
数量
单选题
7
填空题
1
解答题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 化学与STSE | |
| 2 | 0.64 | 物质的分类 | |
| 3 | 0.4 | 离子反应的发生及书写 | |
| 4 | 0.64 | 化学实验基础 | |
| 5 | 0.64 | 化学计量 | |
| 6 | 0.64 | 化学平衡 | |
| 7 | 0.4 | 盐类的水解 | |
| 二、填空题 | |||
| 8 | 0.4 | 物质结构与性质 化学电源 | |
| 三、解答题 | |||
| 9 | 0.4 | 物质的量浓度计算-溶液配制有关计算 物质分离、提纯综合应用 物质制备的探究 氧化还原原理滴定 | 实验探究题 |
| 10 | 0.15 | 有机物的推断 有机合成综合考查 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |
| 11 | 0.15 | 盖斯定律与热化学方程式 电解池电极反应式及化学方程式的书写与判断 | 工业流程题 |



