山西省怀仁市第一中学2021-2022学年高三上学期期中理科综合化学试题
山西
高三
期中
2022-08-20
174次
整体难度:
容易
考查范围:
化学反应原理、有机化学基础、化学实验基础、化学与STSE、认识化学科学、常见无机物及其应用、物质结构与性质
山西省怀仁市第一中学2021-2022学年高三上学期期中理科综合化学试题
山西
高三
期中
2022-08-20
174次
整体难度:
容易
考查范围:
化学反应原理、有机化学基础、化学实验基础、化学与STSE、认识化学科学、常见无机物及其应用、物质结构与性质
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
解题方法
1. 古诗词是我国传统文化的瑰宝。下列诗词解读不正确的是
| A.宋·陈鼓年《广韵》中有“酢浆也,醋也”,食醋的主要成分醋酸为弱电解质 |
| B.“此即地霜也。所在山泽,冬月地上有霜,扫取以水淋汁,后乃煎炼而成。”对硝酸钾的提取涉及溶解、蒸发、结晶操作 |
| C.“章山之铜,所谓丹阳铜也。今世有白铜,盖点化为之,非其本质。”纯铜比白铜硬度大、熔点低 |
| D.《诗经》有“周原膴膴(wu),堇荼如饴(麦芽糖)”,麦芽糖属于二糖 |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
解题方法
2. 化学知识与科技、生产、生活有密切关系。下列叙述中正确的是
| A.检验从月球上带回来的月岩中是否含有Fe2O3的操作步骤是:样品→粉碎→加水→过滤→向滤液中滴加KSCN溶液 |
| B.500米口径球面射电望远镜被誉为“中国天眼”,其“眼眶”是钢铁结成的圈梁,属于新型纯金属材料 |
| C.三星堆二号祭祀坑出土的商代铜人铜像填补了我国考古学、青铜文化史上的诸多空白。青铜器的出土表明我国商代已经掌握冶炼铜的技术 |
| D.新冠疫情期间,常用“84”消毒液消毒,其有效成分次氯酸钙有强氧化性,可使细菌蛋白质变性 |
【知识点】 化学科学对人类文明发展的意义解读 常见金属的冶炼解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 捕获二氧化碳生成甲酸的过程如图所示,N(C2H5)3的化学性质与NH3类似。NA为阿伏加德罗常数的值,下列说法正确的是
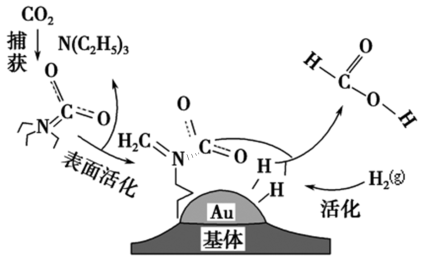

| A.100g 46%的甲酸水溶液中所含的氧原子数目为2NA |
| B.0.1mol N(C2H5)3与盐酸恰好完全反应所得盐溶液中[N(C2H5)3H]+的数目小于0.1NA |
| C.若有11.2L CO2参与反应,则拆开CO2分子中共用电子对的数目为2NA |
| D.每生成0.5mol甲酸,该捕获过程中转移的电子数为2NA |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
4. 乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:
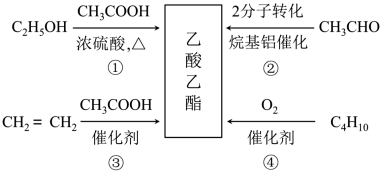
下列说法正确的是

下列说法正确的是
| A.反应①③为取代反应,反应④为氧化反应 |
| B.反应②③④的原子利用率均为100% |
| C.与乙酸乙酯互为同分异构体的酯类化合物有2种 |
| D.乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
5. 短周期主族元素X、Y、Z、W的原子序数依次增大,X和Z位于同一主族,Y的原子半径是短周期元素中最大的,由X、Y、Z三种元素形成的化合物M结构如图所示。下列叙述错误的是
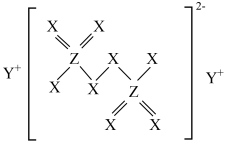

| A.原子半径:Y>Z>W |
| B.在化合物M中,存在极性共价键、非极性共价键和离子键 |
| C.化合物M、WX2、ZX2均为漂白剂,三者漂白原理相同 |
| D.由X、Y、Z形成的化合物的水溶液可能呈碱性 |
您最近一年使用:0次
6. 中国科学院兰州化物所和中国科学技术大学在锂硫电池的研究上获得重大进展。一种锂硫电池的总反应为16Li+S8 8Li2S,该电池的装置如图甲所示,充、放电过程中物质的转化关系如图乙所示。该装置工作时,下列叙述不正确的是
8Li2S,该电池的装置如图甲所示,充、放电过程中物质的转化关系如图乙所示。该装置工作时,下列叙述不正确的是
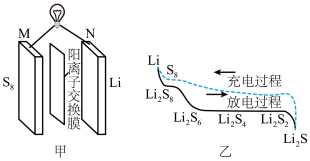
 8Li2S,该电池的装置如图甲所示,充、放电过程中物质的转化关系如图乙所示。该装置工作时,下列叙述不正确的是
8Li2S,该电池的装置如图甲所示,充、放电过程中物质的转化关系如图乙所示。该装置工作时,下列叙述不正确的是
| A.放电时,电池的负极反应式为Li-e-=Li+ |
| B.放电时,1mol Li2S6转化为Li2S4得到1mol电子 |
| C.充电时,M电极的电势比N电极的高 |
| D.充电时,Li+通过阳离子交换膜,到达M电极附近 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
7. 从光盘金属层中提取Ag(其他金属忽略不计)的一种工艺流程如图,下列说法正确的是
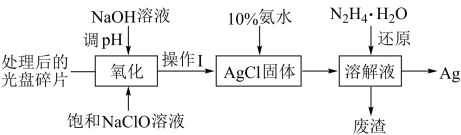
已知:NaClO溶液在受热或酸性条件下易分解

已知:NaClO溶液在受热或酸性条件下易分解
| A.“氧化”过程若在加强热和强酸性条件下进行,可提高氧化速率 |
| B.“氧化”过程还生成O2,则可能发生反应的化学方程式为4Ag+4NaClO+2H2O=4AgCl+4NaOH+O2↑ |
C.AgCl固体溶于10%氨水的离子方程式为:AgCl+2NH3·H2O [Ag(NH3)2]++Cl-+H2O [Ag(NH3)2]++Cl-+H2O |
| D.“还原”过程中N2H4·H2O转化为无害气体N2,则理论上消耗0.5molN2H4·H2O可提取Ag108g |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
8. 氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为2Ga+2NH3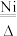 2GaN+3H2。
2GaN+3H2。
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示。
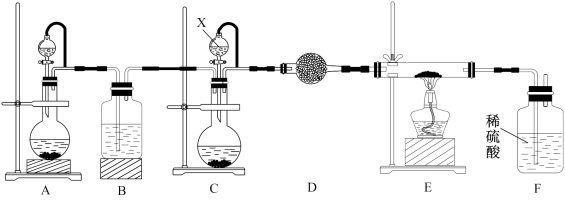
设计实验步骤如下:
①滴加几滴NiCl2溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应后过滤、洗涤、干燥。
(1)仪器X中的试剂是_______ ,A和C装置中都有一个连接分液漏斗的导管,其作用为_______ 。
(2)该套装置中存在一处明显的错误是_______ 。
(3)步骤①中选择NiCl2溶液,不选择氧化镍的原因是_______ (填字母序号)。
a.增大接触面积,加快化学反应速率
b.使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,判断该反应接近完成时,观察到的现象是_______ 。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤于净的操作:_______ 。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热的NaOH浓溶液的离子方程式:_______ 。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为2Ga+2NH3
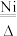 2GaN+3H2。
2GaN+3H2。某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示。

设计实验步骤如下:
①滴加几滴NiCl2溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应后过滤、洗涤、干燥。
(1)仪器X中的试剂是
(2)该套装置中存在一处明显的错误是
(3)步骤①中选择NiCl2溶液,不选择氧化镍的原因是
a.增大接触面积,加快化学反应速率
b.使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,判断该反应接近完成时,观察到的现象是
(5)请写出步骤⑤中检验产品氮化镓固体洗涤于净的操作:
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热的NaOH浓溶液的离子方程式:
您最近一年使用:0次
9. 造成大气污染的NOx、SO2主要来自于汽车尾气及工厂废气的排放,对其进行处理是我们研究的重要课题。
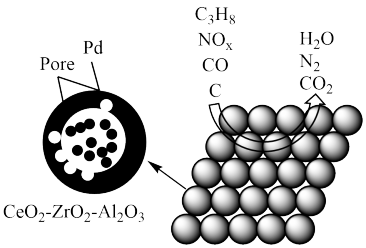
(1)某汽车安装的尾气净化装置工作原理如图所示。下列叙述错误的是_______(填字母)。
(2)已知:2C(s)+O2(g) 2CO(g) ΔH1=-221.0kJ·mol-1
2CO(g) ΔH1=-221.0kJ·mol-1
N2(g)+O2(g) 2NO(g) ΔH2=+180.5kJ·mol-1
2NO(g) ΔH2=+180.5kJ·mol-1
2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1
2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1
则用焦炭还原NO生成无污染气体的热化学方程式为_______ 。
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓。
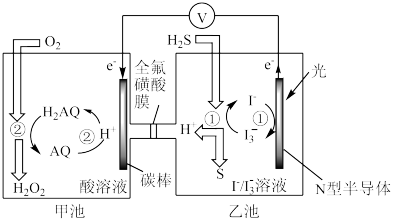
①装置中H+向_______ 池迁移。
②写出乙池溶液中发生反应的离子方程式_______ 。
(4)铈元素(Ce)常见有+3、+4两种价态。NO可以被含Ce4+的溶液吸收,生成含有Ce3+和 的吸收液,反应的离子方程式为
的吸收液,反应的离子方程式为_______ ;现采用电解法将上述吸收液中的 转化为无毒物质,同时再生Ce4+,其原理如图所示。
转化为无毒物质,同时再生Ce4+,其原理如图所示。

①Ce4+从电解槽的_______ (填字母代号)口流出。
②写出阴极的电极反应式:_______ 。
(1)某汽车安装的尾气净化装置工作原理如图所示。下列叙述错误的是_______(填字母)。

| A.Pd-Pore催化剂可提高尾气净化反应的平衡转化率 |
| B.NOx的生成主要是与汽油燃烧不充分有关 |
| C.在此变化过程中,NOx被还原 |
| D.在催化剂的作用下,CO、NOx、C3H8都转化为无毒的物质 |
 2CO(g) ΔH1=-221.0kJ·mol-1
2CO(g) ΔH1=-221.0kJ·mol-1N2(g)+O2(g)
 2NO(g) ΔH2=+180.5kJ·mol-1
2NO(g) ΔH2=+180.5kJ·mol-12NO(g)+2CO(g)
 2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1
2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1则用焦炭还原NO生成无污染气体的热化学方程式为
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓。

①装置中H+向
②写出乙池溶液中发生反应的离子方程式
(4)铈元素(Ce)常见有+3、+4两种价态。NO可以被含Ce4+的溶液吸收,生成含有Ce3+和
 的吸收液,反应的离子方程式为
的吸收液,反应的离子方程式为 转化为无毒物质,同时再生Ce4+,其原理如图所示。
转化为无毒物质,同时再生Ce4+,其原理如图所示。
①Ce4+从电解槽的
②写出阴极的电极反应式:
您最近一年使用:0次
2022-08-20更新
|
148次组卷
|
2卷引用:山西省怀仁市第一中学2021-2022学年高三上学期期中理科综合化学试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
10. 钌(Ru)粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以钌废料制备高纯钌粉的流程如下:
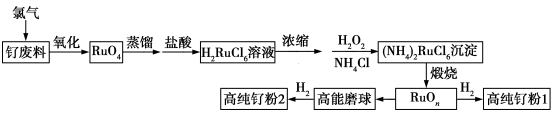
已知:含钌废料中钌主要以单质的形式存在,钌在碱性条件下被氯气“氧化”为RuO4,RuO4是有毒的挥发性物质,蒸馏、用盐酸吸收得到红色H2RuCl6溶液,其中还含有少量 。回答下列问题:
。回答下列问题:
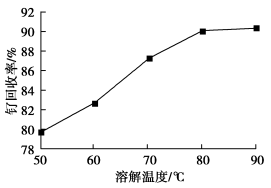
(1)钌废料在碱性条件下被氯气“氧化”的离子方程式为_______ ;钌废料氧化时,随着温度的升高,钉的回收率变化如图所示。综合考虑,确定氧化时的温度以_______ °C为宜。
(2)用盐酸吸收蒸馏产物时发生氧化还原反应,生成一种可循环到“氧化”环节的气体,若标准状况下产生0.448L该气体,则消耗盐酸中HCl的物质的量为_______ (不考虑生成 )。
)。
(3)“浓缩”步骤时用到的仪器有酒精灯、烧杯,还有_______ 。
(4)加入H2O2的主要作用是使溶液中少量 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(5)煅烧的过程可以分为两步,第1步是氯钌酸铵分解生成钌单质和一种无毒的气体单质,同时有两种化合物生成;第2步是钌单质与氧气反应生成钌的氧化物RuOn(n=1~3)。第1步反应的化学方程式为_______ 。

已知:含钌废料中钌主要以单质的形式存在,钌在碱性条件下被氯气“氧化”为RuO4,RuO4是有毒的挥发性物质,蒸馏、用盐酸吸收得到红色H2RuCl6溶液,其中还含有少量
 。回答下列问题:
。回答下列问题:(1)钌废料在碱性条件下被氯气“氧化”的离子方程式为

(2)用盐酸吸收蒸馏产物时发生氧化还原反应,生成一种可循环到“氧化”环节的气体,若标准状况下产生0.448L该气体,则消耗盐酸中HCl的物质的量为
 )。
)。(3)“浓缩”步骤时用到的仪器有酒精灯、烧杯,还有
(4)加入H2O2的主要作用是使溶液中少量
 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为(5)煅烧的过程可以分为两步,第1步是氯钌酸铵分解生成钌单质和一种无毒的气体单质,同时有两种化合物生成;第2步是钌单质与氧气反应生成钌的氧化物RuOn(n=1~3)。第1步反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
名校
解题方法
11. ClCH2COOH(乙氯酸,熔点为50°C)是一种化工原料,实验室制备氨乙酸的装置如图:
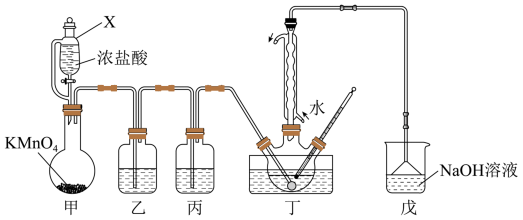
按下列实验步骤回答问题:
(1)①在500 mL三颈烧瓶中放置300 g冰醋酸和15 g催化剂乙酸酐。加热至105°C时,开始徐徐通入干燥纯净的氯气。加热的方法是_______ ,仪器X的名称是_______ ,甲中反应的离子方程式为_______ 。
(2)②氯气通入冰醋酸中呈黄色,随即黄色褪去,氯气通入速率以三颈烧瓶中无黄绿色气体逸出为度,控制氯气通入速率的方法是_______ ,用化学方程式表示黄色褪去的原因:_______ ,反应类型为_______ 。氯乙酸可以和乙醇在浓硫酸加热条件下生成一种酯,该酯的结构简式为_______ 。
(3)③反应约需10小时,每隔2小时向三颈烧瓶中加入5 g乙酸酐,当取出样品测得其熔点为50°C时,停止通入氯气。
④蒸馏:收集186~188°C馏分,冷凝后生成无色氯乙酸晶体378 g,产率为_______ 。选择装置a蒸馏,直形冷凝管易炸裂,原因是_______ 。
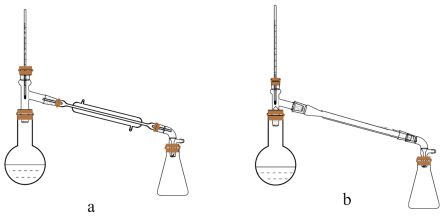

按下列实验步骤回答问题:
(1)①在500 mL三颈烧瓶中放置300 g冰醋酸和15 g催化剂乙酸酐。加热至105°C时,开始徐徐通入干燥纯净的氯气。加热的方法是
(2)②氯气通入冰醋酸中呈黄色,随即黄色褪去,氯气通入速率以三颈烧瓶中无黄绿色气体逸出为度,控制氯气通入速率的方法是
(3)③反应约需10小时,每隔2小时向三颈烧瓶中加入5 g乙酸酐,当取出样品测得其熔点为50°C时,停止通入氯气。
④蒸馏:收集186~188°C馏分,冷凝后生成无色氯乙酸晶体378 g,产率为

您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、有机化学基础、化学实验基础、化学与STSE、认识化学科学、常见无机物及其应用、物质结构与性质
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 强电解质和弱电解质的判断 糖类定义及分类 物质分离、提纯的常见物理方法 金属与合金性能比较 | |
| 2 | 0.94 | 化学科学对人类文明发展的意义 常见金属的冶炼 | |
| 3 | 0.65 | 阿伏加德罗常数的求算 22.4L/mol适用条件 结合氧化还原反应知识与NA相关推算 | |
| 4 | 0.85 | 有机合成综合考查 | |
| 5 | 0.65 | 二氧化硫的漂白性 根据原子结构进行元素种类推断 “位构性”关系理解及应用 共价键的形成及主要类型 | |
| 6 | 0.65 | 原电池正负极判断 原电池电极反应式书写 原电池原理的综合应用 原电池、电解池综合考查 | |
| 7 | 0.85 | 离子方程式的书写 常见无机物的制备 | |
| 二、解答题 | |||
| 8 | 0.65 | 氨气的实验室制法 原电池原理对化学反应速率的影响 常见无机物的制备 物质制备的探究 | 实验探究题 |
| 9 | 0.65 | 盖斯定律与热化学方程式 化学平衡的移动 原电池电子流向判断及应用 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 10 | 0.65 | 化学方程式计算中物质的量的运用 离子方程式的书写 氧化还原反应的应用 物质制备的探究 | 工业流程题 |
| 11 | 0.65 | 取代反应 乙酸的酯化反应 化学实验基础操作 物质含量的测定 | 实验探究题 |



