9. 工业合成氨是人工固氮研究的重要领域,回答下列问题:
(1)诺贝尔化学奖获得者格哈德·埃特尔确认了合成氨反应机理。673K时,各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。
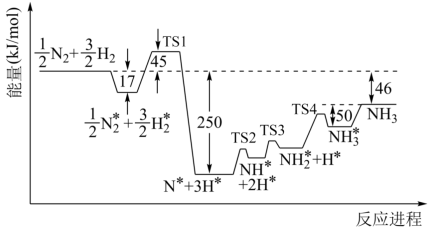
图中决速步骤的反应方程式为
___________________,该步反应的活化能E
a=
______ kJ·mol
-1。
(2)相同质量的同种催化剂,在载体上的分散度越高,催化作用越强,原因是
_________________ 。
NH
3在少量某催化剂下分解的实验数据如下表:
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
c( NH3)/mol·L-1 | c0 | 0.9 c0 | 0.8 c0 | 0.7 c0 | 0.6 c0 | 0. 5 c0 |
分析表中数据可知,随着反应进行,c( NH
3 )减小,平均反应速率
____________(填“增大”、“减小”或“不变”),对该分析结果的合理解释是
____________________。
(3)在一定条件下,向某反应容器中投入4 mol N
2和10 mol H
2在不同温度下反应,平衡体系中氨的物质的量分数随压强变化曲线如图所示:
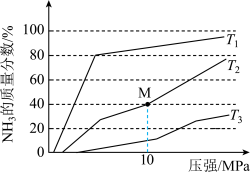
①T
1、T
2、T
3中温度最高的是
______,M点N
2的转化率为
_________________。
②1939年捷姆金和佩热夫推出合成氨反应在接近平衡时净速率方程式为:v(NH
3) =k
1p(N
2)
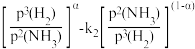
,k
1、k
2的分别为正反应和逆反应的速率常数;p(N
2)、p(H
2)、p(NH
3)代表各组分的分压;α为常数。工业上以铁为催化剂,α=0.5,由M点数据计算
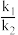
=
___________(MPa)
-2。