2017四川省自贡市高三第一次诊断考试化学试卷
四川
高三
阶段练习
2017-07-27
366次
整体难度:
较难
考查范围:
化学与STSE、认识化学科学、物质结构与性质、化学实验基础、化学反应原理、有机化学基础、常见无机物及其应用
2017四川省自贡市高三第一次诊断考试化学试卷
四川
高三
阶段练习
2017-07-27
366次
整体难度:
较难
考查范围:
化学与STSE、认识化学科学、物质结构与性质、化学实验基础、化学反应原理、有机化学基础、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 化学物质丰富多彩,其与生产、生活密切相关。下列物质的用途不正确的是( )
| A.食醋可用于除去暖水瓶中的水垢 |
| B.纯碱可除去灶具上的油污 |
| C.酒精可用于杀菌消毒 |
| D.单质硅可用作光导纤维 |
【知识点】 化学科学对人类文明发展的意义解读
您最近一年使用:0次
2020-01-17更新
|
24次组卷
|
2卷引用:2017四川省自贡市高三第一次诊断考试化学试卷
单选题
|
适中(0.65)
2. 用 表示阿伏伽德罗常数的值.下列叙述正确的是
表示阿伏伽德罗常数的值.下列叙述正确的是
 表示阿伏伽德罗常数的值.下列叙述正确的是
表示阿伏伽德罗常数的值.下列叙述正确的是A.1mol碳正离子( )所含质子总数为8 )所含质子总数为8 |
B.常温常压下,46g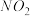 和 和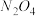 混和气体中含原子总数为3 混和气体中含原子总数为3 |
C.标准状况下,11.2L氟化氢中含有氟原子的数目为0.5 |
D.14g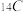 原子形成的石墨中,所含C—C键的个数为 原子形成的石墨中,所含C—C键的个数为 |
您最近一年使用:0次
2016-12-27更新
|
259次组卷
|
2卷引用:2017四川省自贡市高三第一次诊断考试化学试卷
单选题
|
适中(0.64)
3. X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体, X、Y、W在周期表中的相对位里关系如图.下列说法正确的是


| A.五种元素中,原子半径最大的是W |
| B.Y的氢化物的沸点比W的氢化物的沸点低 |
| C.Y与Z 形成的化合物都可以和盐酸反应 |
| D.Z与Q形成的化合物的水解液一定显酸性 |
【知识点】 元素周期表 元素周期律
您最近一年使用:0次
单选题
|
适中(0.64)
4. 用下图装置制取、提纯并收集下表中的四种气体(a、b、c、d表示相应仪器中加入的试剂,收集装置略去)。其中可行的是


| 气体 | a | b | c | d | |
| A |  | 稀硫酸 | 石灰石 | 饱和 溶液 溶液 | 浓 |
| B |  | 浓盐酸 |  固体 固体 | 饱和 溶液 溶液 | 浓 |
| C |  | 饱和 溶液 溶液 | 消石灰 |  | 碱石灰 |
| D |  | 硝酸 | 锌粒 |  |  |
| A.A | B.B | C.C | D.D |
【知识点】 化学实验基础
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
5. 氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是: 据此反应式判断,下列叙述中不正确的是
据此反应式判断,下列叙述中不正确的是
 据此反应式判断,下列叙述中不正确的是
据此反应式判断,下列叙述中不正确的是| A.电池放电时,电池负极周围溶液的pH不断增大 |
B.电池放电时,正极的电极反应为: |
| C.电池充电时,阳极周围溶液的的pH不断减小 |
D.电池充电时,阴极的电极反应为: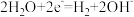 |
您最近一年使用:0次
单选题
|
较难(0.4)
名校
6. 下列各项判断,结论正确的是
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:乙烷、氯乙烯、苯 | 分子内所有原子均在同一平面上 |
| B | C4H8Cl2的同分异构体数目(不考虑立体异构) | 共有10种 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | 由乙酸和乙醇制乙酸乙酯,油脂水解 | 均属于取代反应 |
| A.A | B.B | C.C | D.D |
【知识点】 有机反应类型 同分异构体的数目的确定解读
您最近一年使用:0次
2017-07-07更新
|
241次组卷
|
6卷引用:2017四川省自贡市高三第一次诊断考试化学试卷
单选题
|
较难(0.4)
7. 有机化合物A的分子式是C13H20O8(相对分子质量为304),1molA在酸性条件下与4mol 反应得到4molCH2COOH和1molB.下列说法错误的是
反应得到4molCH2COOH和1molB.下列说法错误的是
 反应得到4molCH2COOH和1molB.下列说法错误的是
反应得到4molCH2COOH和1molB.下列说法错误的是| A.A和B的相对分子质量之差为168 |
| B.B一定不能发生加成反应 |
| C.有机物B与CH3CH2OH互为同系物 |
| D.分子式为C5H1002且与CH2COOH属于同类物质的有机物只有4种 |
您最近一年使用:0次
2017-02-17更新
|
358次组卷
|
2卷引用:2017四川省自贡市高三第一次诊断考试化学试卷
二、解答题 添加题型下试题
解答题-实验探究题
|
困难(0.15)
8. 氰化钠(NaCN)是一种重要的化工原料、有剧毒,一旦泄漏可以通过喷洒双氧水或硫代硫酸钠溶液来处理。
已知:氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3==NaSCN+Na2SO3回答下列问题:
(1)氰化物中碳的化合价为___________ ;用硫代硫酸钠处理1mol NaCN时,反应中转移电子的物质的量为___________ 。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是_____________ 。
(3)某化学兴趣小组在实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】制备Na2S2O3,其实验室装置如下:
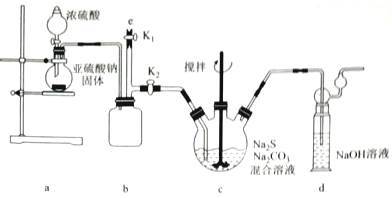
b装置的作用是___________ ;c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有_____________ 。
实验结束后,在e处最好连接盛____________ (填化学式)的注射器,再关闭K2打开K1,以防拆除装置过程中的有害气体污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定时1.000×10-4mol/L的标准AgNO3溶液应用_________ (填仪器名称)盛装;滴定终点时的现象是___________ 。
处理后的废水是否达到排放标准:__________ (填“是”或“否”),其依据是__________ (用实验数据说明)。
已知:氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3==NaSCN+Na2SO3回答下列问题:
(1)氰化物中碳的化合价为
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是
(3)某化学兴趣小组在实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】制备Na2S2O3,其实验室装置如下:

b装置的作用是
实验结束后,在e处最好连接盛
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定时1.000×10-4mol/L的标准AgNO3溶液应用
处理后的废水是否达到排放标准:
【知识点】 化学实验基础
您最近一年使用:0次
三、填空题 添加题型下试题
填空题
|
困难(0.15)
9. 甲醇是重要的绿色能源之一,目前科学家用水煤气(CO+H2)合成甲醇,其反应为:
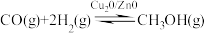 △H=-128.1kJ·mol-1,回答下列问题:
△H=-128.1kJ·mol-1,回答下列问题:
(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有_____________ (写两条)。
(2)恒温恒容条件能说明该可逆反应达平衡的是______________ ;
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中冲入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。
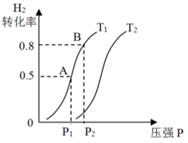
该反应的△S____________ 0,图中的T1___________ T2(填“<”“>”或“=”)
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为_____________ ,若达到平衡状态B时,则容器的体积V(B)=________ L。
(4)已知:H2(g)燃烧热△H=-285.8kJ·mol-1、和CO(g)燃烧热△H=-283.0kJ·mol-1,则CH3OH(g)燃烧热的热化学方程式是为____________ 。
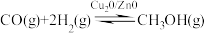 △H=-128.1kJ·mol-1,回答下列问题:
△H=-128.1kJ·mol-1,回答下列问题:(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有
(2)恒温恒容条件能说明该可逆反应达平衡的是
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中冲入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。

该反应的△S
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为
(4)已知:H2(g)燃烧热△H=-285.8kJ·mol-1、和CO(g)燃烧热△H=-283.0kJ·mol-1,则CH3OH(g)燃烧热的热化学方程式是为
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
解题方法
10. 从某废液(含有Fe2+、Cu2+、Cl-)中回收铜并制得纯净的FeCl3溶液。现以制得纯净的FeCl3溶液为原料制取优良的水处理剂高铁酸钾(K2FeO4),其流程如下:

已知:高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。高锰酸钾具有强氧化性。高铁酸钾(K2FeO4)与水作用产生Fe(OH)3。
(1)检验废液中含有Fe2+选用的试剂是________ (填化学式);从废液中制得纯净的FeCl3溶液加入的试剂除铁粉外,还需要一种试剂是_________ (填化学式),加入时发生反应的离子方程式为__________ 。
(2)高铁酸钾(K2FeO4)在处理水过程中的作用是_________ 和__________ 。
(3)“氧化”过程反应的离子方程式为__________ 。
(4)过滤时需用的玻璃仪器有玻璃棒、烧杯和________ ,上述工艺得到的高铁酸钾常含有杂志,可用重结晶法提纯,操作是:将粗产品用_________ 溶解,然后________ 。
(5)用回收的铜为原料可制得粗制CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂志的方法是:向溶液中加入H2O2,再调解溶液PH,过滤即可制得纯净的CuSO4溶液,进而制得纯净CuSO4·5H2O的晶体。
已知:室温时一些物质的Kaq如下表:
已知溶液中的离子浓度小于1×10-6mol·L-1时就认定沉淀完全。
加双氧水的目的是__________ ;若溶液中CuSO4的浓度为3.0mol·L-1,通过计算说明此方法可除去粗制CuSO4·5H2O晶体中FeSO4·7H2O的理由________ 。

已知:高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。高锰酸钾具有强氧化性。高铁酸钾(K2FeO4)与水作用产生Fe(OH)3。
(1)检验废液中含有Fe2+选用的试剂是
(2)高铁酸钾(K2FeO4)在处理水过程中的作用是
(3)“氧化”过程反应的离子方程式为
(4)过滤时需用的玻璃仪器有玻璃棒、烧杯和
(5)用回收的铜为原料可制得粗制CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂志的方法是:向溶液中加入H2O2,再调解溶液PH,过滤即可制得纯净的CuSO4溶液,进而制得纯净CuSO4·5H2O的晶体。
已知:室温时一些物质的Kaq如下表:
| 化学式 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| Kaq | 8.0×10-16 | 8.0×10-18 | 8.0×10-20 |
已知溶液中的离子浓度小于1×10-6mol·L-1时就认定沉淀完全。
加双氧水的目的是
您最近一年使用:0次
2017-02-17更新
|
352次组卷
|
2卷引用:2017四川省自贡市高三第一次诊断考试化学试卷
解答题-无机推断题
|
适中(0.65)
解题方法
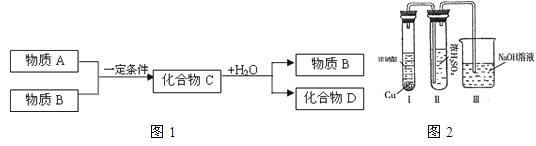
11. 已知由短周期常见元素形成的纯净物A、B、C、D转化关系如图1琐事,物质A与物质B之间的反应不再溶液中进行。
(1) 若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是__________ (填化学式)。
②化合物C的电子式为_________ ;化合物D中所含化学键的类型是_________ 。
③在常温下,向PH=a的醋酸溶液中加入等体积pH=b的D溶液,且a+b=14,则充分反应后,所得溶液中各种离子的浓度由大到小的顺序是:__________ .
(2)若A为非金属单质,C是有色气体,D是一元强酸.
①B为__________ (填化学式)。
②化合物C与H2O反应化学方程式___________ ,氧化剂与还原剂的量比为_________ 。
(3)某同学用图2装置完成有关探究实验。
Ⅰ试管中发生反应的离子方程式为__________ 。
Ⅱ试管中观察到__________ 的实验现象时,说明NO2能溶于浓硫酸中,浓硫酸不能干燥NO2。

(1) 若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是
②化合物C的电子式为
③在常温下,向PH=a的醋酸溶液中加入等体积pH=b的D溶液,且a+b=14,则充分反应后,所得溶液中各种离子的浓度由大到小的顺序是:
(2)若A为非金属单质,C是有色气体,D是一元强酸.
①B为
②化合物C与H2O反应化学方程式
(3)某同学用图2装置完成有关探究实验。
Ⅰ试管中发生反应的离子方程式为
Ⅱ试管中观察到
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
较难(0.4)
12. 已知二元酸H2A在水中存在以下电离:H2A==H++HA-,HA- H++A2-,回答下列问题:
H++A2-,回答下列问题:
(1)Na2A溶液呈________ 性,理由是___________ (用离子方程式表示)。
(2)NaHA溶液呈________ 性,理由是___________ 。
(3)0.1mol/L的NaHA溶液的pH=3,则Ka(HA-)=_____________ 。
(4)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至溶液中水的离子积常数Ka=c2(OH-),此时溶液呈___________ 性,V____________ 10 (填“<”“>”或“=”)c(K+)/c(Na+) ____________ 1(填“<”“>”或“=”),溶液中电荷守恒等式为____________ 。
 H++A2-,回答下列问题:
H++A2-,回答下列问题:(1)Na2A溶液呈
(2)NaHA溶液呈
(3)0.1mol/L的NaHA溶液的pH=3,则Ka(HA-)=
(4)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至溶液中水的离子积常数Ka=c2(OH-),此时溶液呈
【知识点】 弱电解质的电离平衡 电离平衡常数及影响因素解读
您最近一年使用:0次
试卷分析
整体难度:较难
考查范围:化学与STSE、认识化学科学、物质结构与性质、化学实验基础、化学反应原理、有机化学基础、常见无机物及其应用
试卷题型(共 12题)
题型
数量
单选题
7
解答题
3
填空题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 3 | 0.64 | 元素周期表 元素周期律 | |
| 4 | 0.64 | 化学实验基础 | |
| 5 | 0.4 | 新型电池 原电池、电解池综合考查 电解池电极反应式及化学方程式的书写与判断 | |
| 6 | 0.4 | 有机反应类型 同分异构体的数目的确定 | |
| 7 | 0.4 | 同系物的判断 同分异构体的数目的确定 加成反应 酯的水解反应机理 | |
| 二、解答题 | |||
| 8 | 0.15 | 化学实验基础 | 实验探究题 |
| 10 | 0.65 | 高铁酸钠 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 11 | 0.65 | 无机综合推断 浓硫酸的强氧化性 过氧化钠与水的反应 盐溶液中离子浓度大小的比较 | 无机推断题 |
| 三、填空题 | |||
| 9 | 0.15 | 化学反应热的计算 化学平衡 | |
| 12 | 0.4 | 弱电解质的电离平衡 电离平衡常数及影响因素 | |



