广州市广州市东圃中学2019-2020学年高三上学期期中考试理科综合化学试题
广东
高三
期中
2019-12-04
316次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、有机化学基础
广州市广州市东圃中学2019-2020学年高三上学期期中考试理科综合化学试题
广东
高三
期中
2019-12-04
316次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、有机化学基础
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
1. 化学与生活息息相关, 下列说法不正确的是
| A.硅胶多孔, 常用作食品干燥剂和催化剂的载体 |
| B.水玻璃可用作黏合剂和防火剂 |
| C.明矾是一种水处理剂,可用于水的杀菌、消毒 |
| D.“静电除尘”,“燃煤固硫”“汽车尾气催化净化"都能提高空气质量 |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 设NA为阿伏加 德罗常数的值,下列说法正确的是
| A.25C时,1L pH=1的硫酸溶液中,含有H+的数目为0.2NA |
| B.标况下,22.4L Cl2与足量Fe和Cu混合物点燃,反应后,转移的电子数为2 NA个 |
| C.50mL 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
| D.标准状况下,11.2L SO3含有分子数为0.5NA |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
3. 下列有关描述不正确的是
| A.新制饱和氯水和浓硝酸光照下均会有气体产生,其成分中都有氧气 |
| B.灼烧NaOH固体时不能使用瓷坩埚,因为瓷坩埚中的SiO2能与NaOH反应 |
| C.钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同 |
| D.浓硫酸具有较强酸性,能与Cu反应生成H2 |
您最近一年使用:0次
2019-12-02更新
|
137次组卷
|
2卷引用:广州市广州市东圃中学2019-2020学年高三上学期期中考试理科综合化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 下列反应的方程式正确的是
A.蔗糖与浓硫酸混合产生刺激性气味的气体:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O CO2↑+2SO2↑+2H2O |
| B.Cu溶于稀硝酸HNO3:Cu+2H++NO3—=Cu2++NO2↑+H2O |
| C.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42—=BaSO4↓ |
| D.Ca(HCO3)2溶液与足量NaOH溶液反应:HCO3—+Ca2++OH—=CaCO3↓+H2O |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
5. 一种可充电锂-空气电池如图所示,当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是


| A.充电时,电解质溶液中Li+向多孔碳材料区迁移 |
B.充电时,电池总反应为Li2O2-x==2Li+(1-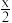 )O2 )O2 |
| C.放电时,多孔碳材料电极为负极 |
| D.放电时,外电路电子由多孔碳材料电极流向锂电极 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
6. W、X、Y、Z为四种短周期主族元素,在光照条件下W的简单氢化物与氯气反应生成油状液体,X的气态氢化物的水溶液呈碱性,Y原子半径是短周期主族元素原子中最大的,Z2—的电子层结构与氩相同。下列说法正确的是
| A.工业上常用电解熔融Y的氧化物制取Y的单质 |
| B.Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红 |
| C.简单氢化物沸点:W>X |
| D.简单离子半径:Z>X>Y |
【知识点】 元素周期律、元素周期表的推断
您最近一年使用:0次
2019-12-11更新
|
67次组卷
|
4卷引用:广东省广州市2018届高三上学期第一次调研考试理综化学试题
单选题
|
容易(0.94)
名校
7. 下列根据实验操作、现象和所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| B | 向Fe(NO3)2溶液中滴入H2SO4酸化的H2O2溶液 | 溶液变为黄色 | 氧化性:Fe3+﹥H2O2 |
| C | 向0.1mol·L-1 AgNO3溶液中滴入稀盐酸至不再有沉淀产生,再滴加0.1mol·L-1 NaI溶液 | 先有白色沉淀后变为黄色沉淀 | Ksp:AgCl<AgI |
| D | 将新制氯水和NaBr溶液在试管中混合后,加入CCl4,振荡静置 | 下层呈红棕色 | 氧化性:Cl2﹥Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-02更新
|
368次组卷
|
2卷引用:广州市广州市东圃中学2019-2020学年高三上学期期中考试理科综合化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
8. 二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(1)ClO2的制备:
已知:SO2+NaClO3+H2SO4=2ClO2↑+2NaHSO4
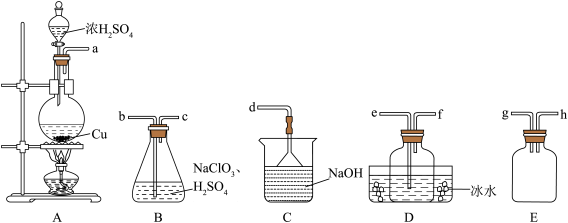
①装置A中反应的化学方程式为________________ 。
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为A→_______ 、_______ 、_______ →C(按气流方向)。
③装置D的作用是_______________ 。
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物。

④ClO2与Na2S反应的离子方程式为___________ 。用于处理含硫废水时,ClO2相对于Cl2的优点是______________ (任写一条)。
(1)ClO2的制备:
已知:SO2+NaClO3+H2SO4=2ClO2↑+2NaHSO4

①装置A中反应的化学方程式为
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为A→
③装置D的作用是
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物。

| 操作步骤 | 实验现象 | 结论 |
| 取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无 |
| 另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ② | 有SO42−生成 |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙内 | 有白色沉淀生成 | 有Cl−生成 |
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
名校
解题方法
9. 甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I:CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
反应II:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
①上述反应符合“原子经济"原则的是__________ (填“I”或“II”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
由表中数据判断反应I为__________ 热反应(填“吸"或“放”)。
③某温度下,将1mol CO和3mol H2充入1L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为________ ,此时的温度为___________ (从表中选择)。
(2)现以甲醇燃料电池。采用电解法来处理酸性含铬废水(主要含有Cr2O72—)时,实验室利用下图装置模拟该法:
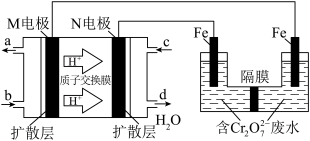
①N电极的电极反应式为_____________________ 。
②请完成电解池中Cr2O72—转化为Cr3+的离子反应方程式:( ) Cr2O72-+( ) Fe2++( ) ═( ) Cr3+ +( ) Fe3++( ) H2O
(3)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10—5mol-L-1时,Cr3+沉淀完全,此时溶液的pH=_____________ (已知,Ksp[Cr(OH)3]=1.0×10-32)
(1)以下是工业上合成甲醇的两个反应:
反应I:CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1反应II:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2①上述反应符合“原子经济"原则的是
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为
③某温度下,将1mol CO和3mol H2充入1L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为
(2)现以甲醇燃料电池。采用电解法来处理酸性含铬废水(主要含有Cr2O72—)时,实验室利用下图装置模拟该法:

①N电极的电极反应式为
②请完成电解池中Cr2O72—转化为Cr3+的离子反应方程式:
(3)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10—5mol-L-1时,Cr3+沉淀完全,此时溶液的pH=
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
名校
解题方法
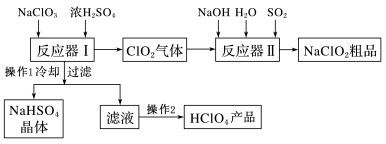
10. 工业上生产高氯酸时,还同时生产了一种常见的重要合氯消毒剂和漂白剂亚氯酸钠(NaClO2),工艺流程如下:
已知:a. NaHSO4的溶解度随着温度的升高而增大,适当条件下可结晶析出;
b.高氯酸是至今为止人们已知酸中的最强酸,沸点:90℃。
(1)操作①冷却过滤的目的是__________________
(2)反应器I中发生化学反应的方程式是_________________ ,反应器I中的温度最佳为__________ (填序号);操作②的名称为______________ 。
A.0℃ B. 20℃ C. 80℃ D. 120℃
(3)反应器II中发生反应的离子方程式为_________ ;SO2的作用为_______________ (氧化剂、还原剂)。
(4)加快反应器II中反应速率的措施有___________ (写出2种措施即可)等。从反应器II中获得NaClO2粗品的实验操作依次是______________ (选序号,下同),进一步提纯的操作名称为______________
A.过滤 B.重结晶 C.蒸馏 D.蒸发浓缩 E.蒸干灼烧 F.冷却结晶

已知:a. NaHSO4的溶解度随着温度的升高而增大,适当条件下可结晶析出;
b.高氯酸是至今为止人们已知酸中的最强酸,沸点:90℃。
(1)操作①冷却过滤的目的是
(2)反应器I中发生化学反应的方程式是
A.0℃ B. 20℃ C. 80℃ D. 120℃
(3)反应器II中发生反应的离子方程式为
(4)加快反应器II中反应速率的措施有
A.过滤 B.重结晶 C.蒸馏 D.蒸发浓缩 E.蒸干灼烧 F.冷却结晶
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
名校
解题方法
11. 有机物F(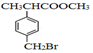 )是合成某种药物的中间体,它的一种合成路线如下:
)是合成某种药物的中间体,它的一种合成路线如下:
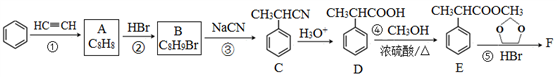
回答下列问题:
(1)A的结构简式为______ ,分子中处于同一平面的原子最多有____ 个。
(2)E中官能团名称是_____ ,①~④中属于加成反应的是_______ (填序号)。
(3)反应③的化学方程式为______________ 。
(4)反应⑤的生成物有两种,除了F以外,另一种生成物的名称是______ 。
(5)满足下列条件的D的同分异构体有______ 种。
①能与FeCl3溶液发生显色反应; ②能发生银镜反应; ③分子中有1个甲基
(6)仿照E的合成路线,设计一种由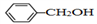 合成
合成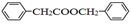 的合成路线
的合成路线_________________ 。
 )是合成某种药物的中间体,它的一种合成路线如下:
)是合成某种药物的中间体,它的一种合成路线如下:
回答下列问题:
(1)A的结构简式为
(2)E中官能团名称是
(3)反应③的化学方程式为
(4)反应⑤的生成物有两种,除了F以外,另一种生成物的名称是
(5)满足下列条件的D的同分异构体有
①能与FeCl3溶液发生显色反应; ②能发生银镜反应; ③分子中有1个甲基
(6)仿照E的合成路线,设计一种由
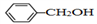 合成
合成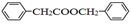 的合成路线
的合成路线
您最近一年使用:0次
2017-05-29更新
|
502次组卷
|
6卷引用:湖北省襄阳市第五中学2017届高三下学期第三次适应性考试化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、有机化学基础
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 硅酸的物理性质 明矾的净水作用及原理 大气污染的治理原理及方法 | |
| 2 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 3 | 0.85 | 氯水的性质 硝酸的不稳定性 浓硫酸的强氧化性 二氧化硅的化学性质 | |
| 4 | 0.65 | 离子方程式的正误判断 | |
| 5 | 0.65 | 新型电池 | |
| 6 | 0.65 | 元素周期律、元素周期表的推断 | |
| 7 | 0.94 | 硫酸根离子的检验 Fe2+的还原性 沉淀转化 同主族元素性质递变规律探究实验 | |
| 二、解答题 | |||
| 8 | 0.65 | 浓硫酸的强氧化性 物质性质的探究 物质性质实验方案的设计 综合实验设计与评价 | 实验探究题 |
| 9 | 0.65 | 化学反应原理综合考查 化学平衡常数的影响因素及应用 溶度积常数相关计算 电解原理的应用实验 | 原理综合题 |
| 10 | 0.65 | 氧化还原反应方程式的配平 物质分离、提纯的常见物理方法 常见无机物的制备 | 工业流程题 |
| 11 | 0.65 | 同分异构体的数目的确定 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |



