三轮冲刺2020届高三化学考题必刷——“拓展综合型”实验探究题
全国
高三
专题练习
2020-02-12
44次
整体难度:
适中
考查范围:
常见无机物及其应用、化学反应原理、化学实验基础、认识化学科学、有机化学基础、化学与STSE
三轮冲刺2020届高三化学考题必刷——“拓展综合型”实验探究题
全国
高三
专题练习
2020-02-12
44次
整体难度:
适中
考查范围:
常见无机物及其应用、化学反应原理、化学实验基础、认识化学科学、有机化学基础、化学与STSE
一、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
1. 铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。已知氯化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成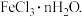
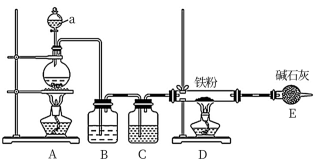
(1)某学习小组用如图装置在实验室制备无水氯化铁,请你一起参与该小组的活动。
①装置A 中仪器 a的名称是______ 。
②装置B的作用是______ ,C 中的试剂 ______ 。
③实验开始时先点燃______ 处酒精灯;装置 E的作用为 ______ 。
(2)工业上制备无水氯化铁的一种工艺流程如下:

①吸收塔中发生反应的离子方程式为______
②简述由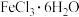 晶体得到无水氯化铁的操作:
晶体得到无水氯化铁的操作: ______
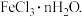

(1)某学习小组用如图装置在实验室制备无水氯化铁,请你一起参与该小组的活动。
①装置A 中仪器 a的名称是
②装置B的作用是
③实验开始时先点燃
(2)工业上制备无水氯化铁的一种工艺流程如下:

①吸收塔中发生反应的离子方程式为
②简述由
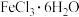 晶体得到无水氯化铁的操作:
晶体得到无水氯化铁的操作:
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
2. 利用如图所示的装置,可以验证 和 HCl的有关性质。实验前a、b、c活塞均关闭。
和 HCl的有关性质。实验前a、b、c活塞均关闭。
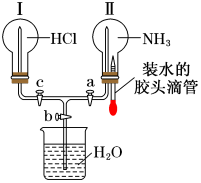
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是______
(2)若先打开a、c 活塞,再挤压胶头滴管 假设
假设 不被完全吸收
不被完全吸收 ,在烧瓶Ⅱ中可观察到的现象
,在烧瓶Ⅱ中可观察到的现象 ______ 
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是______ 。
 和 HCl的有关性质。实验前a、b、c活塞均关闭。
和 HCl的有关性质。实验前a、b、c活塞均关闭。 
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是
(2)若先打开a、c 活塞,再挤压胶头滴管
 假设
假设 不被完全吸收
不被完全吸收 ,在烧瓶Ⅱ中可观察到的现象
,在烧瓶Ⅱ中可观察到的现象 
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是
【知识点】 实验方案设计的基本要求解读 物质性质实验方案的设计解读
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
3. 最近几年我国已加大对氮氧化物排放的控制力度。消除氮氧化物污染有多种方法。
(l)用CH4还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l) △H=-44.0kJ·mol-1
CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式为_________________ 。
(2)用活性炭还原法也可处理氮氧化物。有关反应为:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始时向密闭容器中充入一定量的C(s)和NO2(g),在不同条件下,测得各物质的浓度变化状况如下图所示。

①0〜10min内,以CO2表示的平均反应速率v(CO2)=_______________ 。
②0~10min,10〜20 min,30〜40 min三个阶段NO2的转化率分别为α1、α2、α3,其中最小的为_________ ,其值是___________________ 。
③计算反应达到第一次平衡时的平衡常数K=____________ 。
④第10min时,若只改变了影响反应的一个条件,则改变的条件为______ (填选项字母)。
A.增加C(s)的量 B.减小容器体积 C.加入催化剂
⑤20~30min、40〜50 min时体系的温度分别为T1和T2,则T1_____ T2(填“> “<”或“=”), 判断的理由是_________________________ 。
(l)用CH4还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l) △H=-44.0kJ·mol-1
CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式为
(2)用活性炭还原法也可处理氮氧化物。有关反应为:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始时向密闭容器中充入一定量的C(s)和NO2(g),在不同条件下,测得各物质的浓度变化状况如下图所示。

①0〜10min内,以CO2表示的平均反应速率v(CO2)=
②0~10min,10〜20 min,30〜40 min三个阶段NO2的转化率分别为α1、α2、α3,其中最小的为
③计算反应达到第一次平衡时的平衡常数K=
④第10min时,若只改变了影响反应的一个条件,则改变的条件为
A.增加C(s)的量 B.减小容器体积 C.加入催化剂
⑤20~30min、40〜50 min时体系的温度分别为T1和T2,则T1
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
4. 某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______ (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________ 。
(3)判断滴定到达终点的现象是_________________________ 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________ 。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________ (填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为
(3)判断滴定到达终点的现象是
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | ||
| 验证不稳定性 |
【知识点】 氧化还原反应的应用 酸碱中和滴定的综合考查解读
您最近一年使用:0次
2016-12-09更新
|
575次组卷
|
4卷引用:2015届江苏省扬州中学高三质量检测化学试卷
2015届江苏省扬州中学高三质量检测化学试卷福建省2020届高三化学总复习专题训练——过氧化氢氧化性、还原性的探究三轮冲刺2020届高三化学考题必刷——“拓展综合型”实验探究题(已下线)微专题24 H2O2性质“四重性”探究及应用-备战2022年高考化学考点微专题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
5. Ⅰ.醋酸(已知:25℃,Ka(CH3COOH)=1.69×10-5)是日常生活中最常见的调味剂和重要的化工原料。下列实验方案能说明醋酸是弱酸的是________________________
a配制0.10mol / L的醋酸溶液,向其中滴入几滴甲基橙试液,然后再加入少量醋酸钠晶体,振荡。
b配制0.10mol / L的醋酸钠溶液,加入几滴酚酞试液。
c 取一定量的无水醋酸配制0.1mol/L的醋酸溶液,测溶液的pH值。
Ⅱ.某实验小组拟用酸碱中和滴定法测定食醋的总酸量(g/100mL), 实验步骤:
⑴取10.00mL市售白醋样品,稀释配成100mL的食醋溶液。
⑵用酸式滴定管取稀释后食醋溶液20.00mL于锥形瓶中。
⑶用某仪器 盛装0.1000mol/L NaOH标准溶液,静置后,读取数据,记录为NaOH标准溶液体积的初读数。
⑷滴定,并记录NaOH的终读数。重复滴定2-3次。
实验记录及数据处理
回答如下的问题:
①步骤⑶中使用到的某仪器名称是______________
②常温下,醋酸和氢氧化钠溶液恰好反应时,溶液pH________ 7(填“>”、“=”或“<”)。
③下列指示剂中,最适合于本实验的是________
A. 0.1%甲基橙溶液 B. 0.1%酚酞溶液 C. 0.1%石蕊溶液
滴定终点的判断依据是____________________________________________
④根据实验数据,样品总酸量=_______ g / 100mL。(醋酸的相对分子质量为60)
⑤若滴定时,读取NaOH溶液的初读数时仰视读数,滴定结束时俯视读数,则求得的醋酸溶液的物质的量浓度( )
A.偏低 B.偏高 C.偏低或偏高或不能确定 D.不受影响
a配制0.10mol / L的醋酸溶液,向其中滴入几滴甲基橙试液,然后再加入少量醋酸钠晶体,振荡。
b配制0.10mol / L的醋酸钠溶液,加入几滴酚酞试液。
c 取一定量的无水醋酸配制0.1mol/L的醋酸溶液,测溶液的pH值。
Ⅱ.某实验小组拟用酸碱中和滴定法测定食醋的总酸量(g/100mL), 实验步骤:
⑴取10.00mL市售白醋样品,稀释配成100mL的食醋溶液。
⑵用酸式滴定管取稀释后食醋溶液20.00mL于锥形瓶中。
⑶用
⑷滴定,并记录NaOH的终读数。重复滴定2-3次。
实验记录及数据处理
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.00 | 0.200 | 0.10 | 0.00 |
| V(NaOH)/mL(终读数) | 14.98 | 15.20 | 15.12 | 15.95 |
| V(NaOH)/mL(消耗) | 14.98 | 15.00 | 15.02 | 15.95 |
①步骤⑶中使用到的某仪器名称是
②常温下,醋酸和氢氧化钠溶液恰好反应时,溶液pH
③下列指示剂中,最适合于本实验的是
A. 0.1%甲基橙溶液 B. 0.1%酚酞溶液 C. 0.1%石蕊溶液
滴定终点的判断依据是
④根据实验数据,样品总酸量=
⑤若滴定时,读取NaOH溶液的初读数时仰视读数,滴定结束时俯视读数,则求得的醋酸溶液的物质的量浓度
A.偏低 B.偏高 C.偏低或偏高或不能确定 D.不受影响
您最近一年使用:0次
2018-06-22更新
|
203次组卷
|
2卷引用:【全国百强校】广东仲元中学2017-2018学年高二下学期期中考试(理)化学试题
6. 氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素 的碱性溶液制氢气的装置示意图
的碱性溶液制氢气的装置示意图 电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极
电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极 。
。
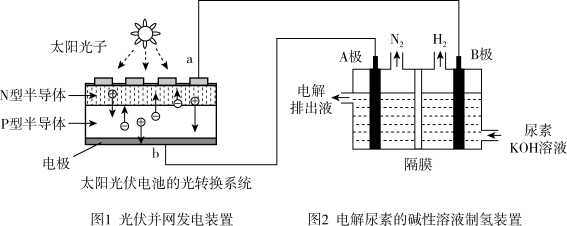
(1)图1中N型半导体为______  填“正极”或“负极”
填“正极”或“负极”
(2)该系统工作时,A极的电极反应式为______
(3)若A极产生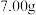
 ,则此时B极产生
,则此时B极产生______ L  标况下
标况下 。
。
 的碱性溶液制氢气的装置示意图
的碱性溶液制氢气的装置示意图 电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极
电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极 。
。
(1)图1中N型半导体为
 填“正极”或“负极”
填“正极”或“负极”
(2)该系统工作时,A极的电极反应式为
(3)若A极产生
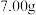
 ,则此时B极产生
,则此时B极产生 标况下
标况下 。
。
您最近一年使用:0次



