某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。请回答下列问题:
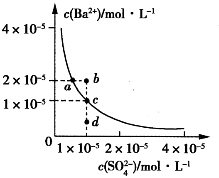
(1)下列说法正确的是__ (填序号)。
A.向BaSO4饱和溶液中加入固体Na2SO4可以由a点变到b点
B.通过蒸发可以由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)将100mL1mol•L-1H2SO4溶液加入100mL含Ba2+0.137g的溶液中充分反应后,过滤,滤液中残留的Ba2+的物质的量浓度约为___ 。
(3)若沉淀分别用100mL纯水和100mL0.01mol•L-1的H2SO4溶液洗涤,两种情况下损失的BaSO4的质量之比为__ 。

(1)下列说法正确的是
A.向BaSO4饱和溶液中加入固体Na2SO4可以由a点变到b点
B.通过蒸发可以由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)将100mL1mol•L-1H2SO4溶液加入100mL含Ba2+0.137g的溶液中充分反应后,过滤,滤液中残留的Ba2+的物质的量浓度约为
(3)若沉淀分别用100mL纯水和100mL0.01mol•L-1的H2SO4溶液洗涤,两种情况下损失的BaSO4的质量之比为
16-17高二上·湖北襄阳·阶段练习 查看更多[4]
2016-2017学年湖北省襄阳五中高二上10月月考化学试卷【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二下学期开学考试化学试题(已下线)【南昌新东方】江西省九江一中2014-2015学年高二上学期期中化学试卷(已下线)专题3 溶液中的离子反应 综合评价(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
更新时间:2020-06-14 11:22:54
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】
(1)粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质。在提纯时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是___________ 。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,lg2=0.3。通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全。试计算
①将溶液的pH调至PH=__________ 时Fe3+转化为Fe(OH)3而沉淀完全。
②若CuSO4溶液的浓度为2.2mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为__________ 。
(3)调整溶液的pH可选用下列中的____________ 。
A.NaOH(aq) B.NH3·H2O C.CuO粉末D.Cu(OH)2悬浊液E.Cu2(OH)2CO3(s)
(1)粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质。在提纯时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,lg2=0.3。通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全。试计算
①将溶液的pH调至PH=
②若CuSO4溶液的浓度为2.2mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为
(3)调整溶液的pH可选用下列中的
A.NaOH(aq) B.NH3·H2O C.CuO粉末D.Cu(OH)2悬浊液E.Cu2(OH)2CO3(s)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)已知25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。请回答下列问题:
①25℃时,若向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,混合后溶液中的c(Ag+)为________ mol·L-1,pH为________ 。
②25℃时,取一定量含有I-、Cl-的溶液,向其中滴加AgNO3溶液,当AgCl和AgI同时沉淀时,溶液中 为
为________ 。
已知:2CrO42-+2H+ Cr2O
Cr2O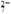 +H2O,25 ℃时,Ksp(Ag2CrO4)=9.0×10-12,Ksp(Ag2Cr2O7)=2.0×10-7,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
+H2O,25 ℃时,Ksp(Ag2CrO4)=9.0×10-12,Ksp(Ag2Cr2O7)=2.0×10-7,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是__________ 。
(3)已知:25 ℃时Ksp(Ag2CrO4)=9.0×10-12,Ksp(AgCl)=1.8×10-10,说明Ag2CrO4的溶解度________ (填“大于”“小于”或“等于”)AgCl的。
(4)25 ℃时,Mg(OH)2饱和溶液________ (填“能”或“不能”)使石蕊溶液变蓝色。(已知Ksp[Mg(OH)2]=4.0×10-12,lg 5=0.7)。
①25℃时,若向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,混合后溶液中的c(Ag+)为
②25℃时,取一定量含有I-、Cl-的溶液,向其中滴加AgNO3溶液,当AgCl和AgI同时沉淀时,溶液中
 为
为已知:2CrO42-+2H+
 Cr2O
Cr2O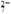 +H2O,25 ℃时,Ksp(Ag2CrO4)=9.0×10-12,Ksp(Ag2Cr2O7)=2.0×10-7,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
+H2O,25 ℃时,Ksp(Ag2CrO4)=9.0×10-12,Ksp(Ag2Cr2O7)=2.0×10-7,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是(3)已知:25 ℃时Ksp(Ag2CrO4)=9.0×10-12,Ksp(AgCl)=1.8×10-10,说明Ag2CrO4的溶解度
(4)25 ℃时,Mg(OH)2饱和溶液
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01mol/L的NaOH溶液滴定10mL0.01mol/L的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

c点时溶液中各离子浓度由大到小的顺序为___ ;
②b点时溶液中c(N2O22-)___ c(H2N2O2)(填“>”“<”或“=”);
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中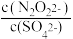 =
=___ 。
[已知KSP(Ag2SO4)=1.4×10-5、KSP(Ag2N2O2)=5.6×10-9 ]。
(3)常温下,向b mol/L醋酸钠溶液中滴加等体积的amol/L的盐酸,使溶液恰好呈中性,则醋酸的电离平衡常数=___ (用含a、b的代数式表示)
(1)常温下,用0.01mol/L的NaOH溶液滴定10mL0.01mol/L的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

c点时溶液中各离子浓度由大到小的顺序为
②b点时溶液中c(N2O22-)
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中
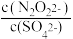 =
=[已知KSP(Ag2SO4)=1.4×10-5、KSP(Ag2N2O2)=5.6×10-9 ]。
(3)常温下,向b mol/L醋酸钠溶液中滴加等体积的amol/L的盐酸,使溶液恰好呈中性,则醋酸的电离平衡常数=
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】(1)已知25℃时,Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。25℃时,向浓度均为0.01mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__ 沉淀(填化学式),生成该沉淀的离子方程式为___ ,当两种沉淀共存时, =
=__ (保留两位有效数字)。
(2)25℃时,向0.01mol/L的MgCl2溶液中,逐滴加入浓NaOH溶液,刚好出现沉淀时,溶液的pH为____ ;当溶液中的离子浓度小于1×10−5mol/L时,认为该离子沉淀完全,当Mg2+完成沉淀时,溶液的pH为___ (忽略溶液体积的变化,已知:(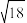 ≈4.2,
≈4.2, ≈1.3,lg2.4=0.4,lg7.7=0.9。)
≈1.3,lg2.4=0.4,lg7.7=0.9。)
(3)该温度下,反应Cu(OH)2+2H+ Cu2++2H2O的平衡常数K=
Cu2++2H2O的平衡常数K=__ 。
 =
=(2)25℃时,向0.01mol/L的MgCl2溶液中,逐滴加入浓NaOH溶液,刚好出现沉淀时,溶液的pH为
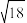 ≈4.2,
≈4.2, ≈1.3,lg2.4=0.4,lg7.7=0.9。)
≈1.3,lg2.4=0.4,lg7.7=0.9。)(3)该温度下,反应Cu(OH)2+2H+
 Cu2++2H2O的平衡常数K=
Cu2++2H2O的平衡常数K=
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】有关溶液中的计算
(1)某温度下测得0.01mol·L-1的NaOH溶液的pH为11,在该温度下,将pH=12的NaOH溶液VaL与pH=2的硫酸VbL混合。若所得混合液的pH=10,忽略体积变化,则Va∶Vb=___________ 。
(2)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
(3)常温下二元酸发生如下电离:H2A=H++HA-;HA-⇌H++A2-(Ka=1×10﹣2)。则常温下pH=10的Na2A溶液中c(A2-)是c(HA-)的___________ 倍。
(4)常温下Fe(OH)3的溶度积Ksp=1.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1.0×10-5mol·L-1时就沉淀完全,设溶液中CuSO4的浓度为3.0mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为___________ ,Fe3+完全沉淀时溶液的pH为___________ 。
(1)某温度下测得0.01mol·L-1的NaOH溶液的pH为11,在该温度下,将pH=12的NaOH溶液VaL与pH=2的硫酸VbL混合。若所得混合液的pH=10,忽略体积变化,则Va∶Vb=
(2)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=(3)常温下二元酸发生如下电离:H2A=H++HA-;HA-⇌H++A2-(Ka=1×10﹣2)。则常温下pH=10的Na2A溶液中c(A2-)是c(HA-)的
(4)常温下Fe(OH)3的溶度积Ksp=1.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1.0×10-5mol·L-1时就沉淀完全,设溶液中CuSO4的浓度为3.0mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)25℃时,某FeCl3溶液的pH=2,则由水电离产生的总c(OH-)=____________ ;用离子方程式表示FeCl3溶液用于净水的原因____________________________________ 。
(2)已知NaHSO4在水中的电离方程式NaHSO4=Na++H++SO42-。在NaHSO4溶液中c(H+)___________ c(OH-)+c(SO42-)(填“>”、“=”或“<”下同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH__________ 7。
(3)将0.02mol/LNa2SO4溶液与某浓度BaCl2溶液等体积混合,则生成BaSO4沉淀所需原BaCl2溶液的最小浓度为_________________________________ 。(已知Ksp(BaSO4)=1.1×10-10)
(4)一定温度下,测得某纯水的pH为6.5。此时水的离子积常数Kw为_______ ;若在此纯水中加一定量Ba(OH)2固体,配制成0.005mol·L-1的Ba(OH)2溶液,保持原温度,其溶液的pH为__________ 。
(2)已知NaHSO4在水中的电离方程式NaHSO4=Na++H++SO42-。在NaHSO4溶液中c(H+)
(3)将0.02mol/LNa2SO4溶液与某浓度BaCl2溶液等体积混合,则生成BaSO4沉淀所需原BaCl2溶液的最小浓度为
(4)一定温度下,测得某纯水的pH为6.5。此时水的离子积常数Kw为
您最近一年使用:0次


 的浓度为多少?
的浓度为多少?

