已知无水AlCl3遇潮湿空气即产生大量白雾,实验室可用如图所示装置制备AlCl3。
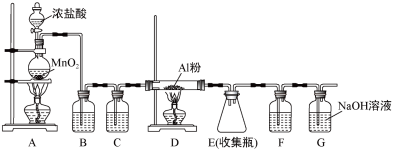
(1)装置A中发生反应的离子方程式为________________________________________
(2)装置B盛放的试剂是______ ,其作用是_______________________________ ;装置C盛放的试剂是__________ ,其作用是__________________________________
(3)装置G的作用是________________ ,G中发生反应的化学方程式是________________________________________
(4)F中盛放的试剂是______ ,其作用是___________________________________

(1)装置A中发生反应的离子方程式为
(2)装置B盛放的试剂是
(3)装置G的作用是
(4)F中盛放的试剂是
更新时间:2020-06-15 23:02:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种常见的氮氧化物,其中一种呈红棕色。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:为制备纯净干燥的气体,下表中缺少的药品是:

(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
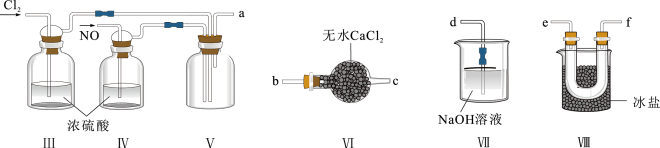
①装置连接顺序为a→____ (按气流自左向右方向,用小写字母表示)。
②为了使气体充分反应,实验中先通入Cl2,待装置Ⅴ中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是______ (回答一条即可)。
③装置Ⅴ生成NOCl的化学方程式是________ 。
④装置Ⅵ的作用为___ ,若无该装置,Ⅷ中NOCl可能发生反应的化学方程式为__ 。
(3)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:
取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为______ (用代数式表示即可)。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:为制备纯净干燥的气体,下表中缺少的药品是:

| 制备原料 | 装置Ⅰ | 装置Ⅱ | |
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | ① | 饱和食盐水 |
| 制备纯净NO | Cu | 稀硝酸 | ② |

①装置连接顺序为a→
②为了使气体充分反应,实验中先通入Cl2,待装置Ⅴ中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是
③装置Ⅴ生成NOCl的化学方程式是
④装置Ⅵ的作用为
(3)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:
取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】疫情防控中,含氯消毒剂发挥了重要作用。含氯消毒剂有多种,如 、
、 、NaClO、
、NaClO、 、
、 。某化学兴趣小组利用NaOH溶液来制备含氯消毒剂。
。某化学兴趣小组利用NaOH溶液来制备含氯消毒剂。
Ⅰ.配制一定物质的量浓度的NaOH溶液
(1)配制250 mL 1.0 mol/L NaOH溶液,需用托盘天平称取___________ g NaOH固体。配制该溶液除用到量筒、烧杯、玻璃棒外,还需要的玻璃仪器是___________ 。
(2)下列操作中,会造成所配溶液浓度偏低的是___________ 。
a.容量瓶用蒸馏水洗涤后,没有经过干燥立即使用
b.溶液未经冷却立即转移到容量瓶中定容
c.没有洗涤烧杯和玻璃棒
d.向容量瓶加水定容时眼睛俯视观察刻度线
Ⅱ.利用如图装置制备“84”消毒液

(3)实验室安全图标不仅能够提醒潜在的危险因素,还能够引导实验人员采取相应的防护措施,以下制备“84”消毒液的实验不需要标记的图标有___________ (填标号)。
(4)仪器A的名称为___________ 。
(5)装置①中二氧化锰和浓盐酸反应制取氯气的化学方程式为___________ 。
(6)装置②中盛装的试剂为___________ ,用于除去 中的HCl杂质。
中的HCl杂质。
(7)装置③中制得“84”消毒液,其有效成分是___________ (填化学式)。
(8)清洗卫生间时,“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,用离子方程式解释其原因为___________ 。
(9)含氯消毒剂中有效氯含量,能反映含氯消毒剂消毒能力的大小,其定义是每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。则NaClO的有效氯含量为___________ (保留小数点后两位)。
 、
、 、NaClO、
、NaClO、 、
、 。某化学兴趣小组利用NaOH溶液来制备含氯消毒剂。
。某化学兴趣小组利用NaOH溶液来制备含氯消毒剂。Ⅰ.配制一定物质的量浓度的NaOH溶液
(1)配制250 mL 1.0 mol/L NaOH溶液,需用托盘天平称取
(2)下列操作中,会造成所配溶液浓度偏低的是
a.容量瓶用蒸馏水洗涤后,没有经过干燥立即使用
b.溶液未经冷却立即转移到容量瓶中定容
c.没有洗涤烧杯和玻璃棒
d.向容量瓶加水定容时眼睛俯视观察刻度线
Ⅱ.利用如图装置制备“84”消毒液

(3)实验室安全图标不仅能够提醒潜在的危险因素,还能够引导实验人员采取相应的防护措施,以下制备“84”消毒液的实验不需要标记的图标有
 |  |  |  |  |
|
| ①护目镜 | ②锐器 | ③明火 | ④热烫 | ⑤排风 | ⑥洗手 |
(4)仪器A的名称为
(5)装置①中二氧化锰和浓盐酸反应制取氯气的化学方程式为
(6)装置②中盛装的试剂为
 中的HCl杂质。
中的HCl杂质。(7)装置③中制得“84”消毒液,其有效成分是
(8)清洗卫生间时,“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,用离子方程式解释其原因为
(9)含氯消毒剂中有效氯含量,能反映含氯消毒剂消毒能力的大小,其定义是每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。则NaClO的有效氯含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某校化学实验兴趣小组为了验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时认识氯气的某些性质及应用,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答下列问题。
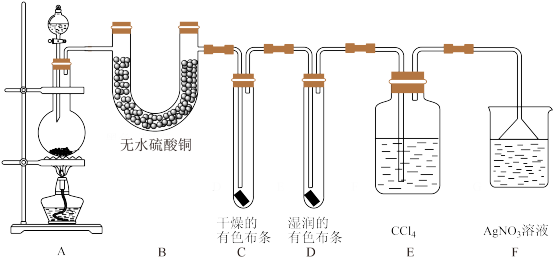
(1)若用浓盐酸与MnO2反应制取Cl2,圆底烧瓶内发生的化学反应方程式为___ 。
(2)装置B中无水硫酸铜的作用是___ ,甲同学提出在B、C之间加入一个装有___ 的干燥管,以防止对C、D中的实验造成干扰。
(3)乙同学提出,为了确保实验结论的准确性,证明通入装置F中的气体只有一种,应在E、F之间再加一个装置,装置中应放入___ (写试剂或用品名称)。
(4)若将该实验中制得的1molCl2通入足量的石灰乳中,理论上可得到次氯酸钙多少克___ ?(写出计算过程)

(1)若用浓盐酸与MnO2反应制取Cl2,圆底烧瓶内发生的化学反应方程式为
(2)装置B中无水硫酸铜的作用是
(3)乙同学提出,为了确保实验结论的准确性,证明通入装置F中的气体只有一种,应在E、F之间再加一个装置,装置中应放入
(4)若将该实验中制得的1molCl2通入足量的石灰乳中,理论上可得到次氯酸钙多少克
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学研究性学习小组拟用下列装置和药品制备无水氯化铁晶体,该物质极易水解,100℃左右时升华。请回答下列问题:
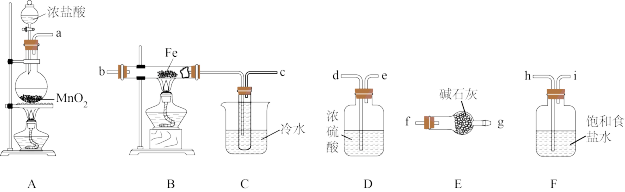
(1)不加热条件下检查A装置气密性的操作方法为_______ 。
(2)制备开始时A装置烧瓶中产生的现象为_______ 。发生反应的离子方程式为_______ 。
(3)按气流方向连接完整装置:a→_______ 。(填仪器接口字母编号)。
(4)装置F的作用是_______ 。B装置硬质玻璃管内导管口处棉花的作用是_______ 。若无E装置可能产生的后果是_______ 。
(5)本实验合理的操作步骤为_______ 。(按操作顺序选择序号)。
①添加药品
②连接仪器
③检查装置气密性
④点燃A处酒精灯
⑤点燃B处酒精灯
⑥使B中硬质玻璃管内充满黄绿色气体
(6)已知:亚铁离子与K3[Fe(SCN)6]溶液反应生成蓝色沉淀。设计实验证明装置 的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。
的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。_______ 。
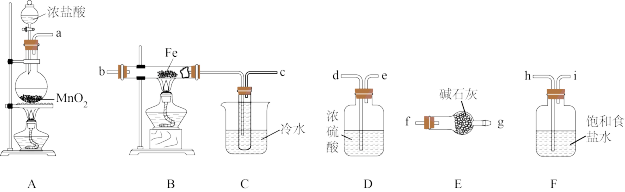
(1)不加热条件下检查A装置气密性的操作方法为
(2)制备开始时A装置烧瓶中产生的现象为
(3)按气流方向连接完整装置:a→
(4)装置F的作用是
(5)本实验合理的操作步骤为
①添加药品
②连接仪器
③检查装置气密性
④点燃A处酒精灯
⑤点燃B处酒精灯
⑥使B中硬质玻璃管内充满黄绿色气体
(6)已知:亚铁离子与K3[Fe(SCN)6]溶液反应生成蓝色沉淀。设计实验证明装置
 的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。
的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】无水氯化铝是有机化工常用的催化剂,氯化铝178 ℃时升华,极易潮解,遇水发热并产生白色烟雾。氯化铝还易溶于乙醇、氯仿和四氯化碳。实验室可用反应2Al+6HCl(g)  2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
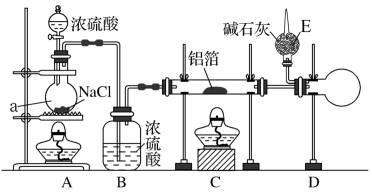
注意,盐酸极易挥发,装置A内利用此特点制备HCl气体: H2SO4(浓)+2NaCl Na2SO4+2HCl↑
Na2SO4+2HCl↑
(1)仪器a的名称____________ ,反应后a中溶液的焰色反应颜色是________
(2)以下三步操作的先后顺序为________ (填序号)。
①点燃A处酒精灯 ②点燃C处酒精灯 ③滴加A处浓硫酸
(3)E干燥管内碱石灰的作用是____________ 。
(4)若将2.67 gAlCl3溶解并配置成800 mL溶液,则溶液中c(Cl-)=___ mol·L-1
 2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
注意,盐酸极易挥发,装置A内利用此特点制备HCl气体: H2SO4(浓)+2NaCl
 Na2SO4+2HCl↑
Na2SO4+2HCl↑(1)仪器a的名称
(2)以下三步操作的先后顺序为
①点燃A处酒精灯 ②点燃C处酒精灯 ③滴加A处浓硫酸
(3)E干燥管内碱石灰的作用是
(4)若将2.67 gAlCl3溶解并配置成800 mL溶液,则溶液中c(Cl-)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】无水四氯化锡( )用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,可用下图装置制备四氯化锡。
)用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,可用下图装置制备四氯化锡。
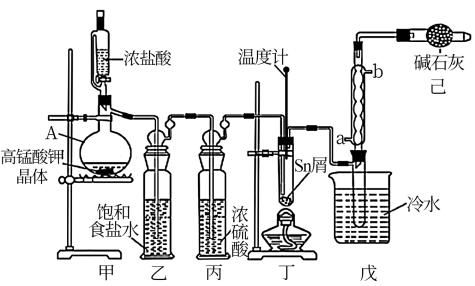
有关信息如下表:
(1)仪器A的名称为_______ ,A中发生反应的化学方程式为_______ 。
(2)将如图装置连接好,先检查装置的气密性,再慢慢滴入浓盐酸,待观察到_______ 现象后,开始加热装置丁。反应开始生成 时,需熄灭酒精灯,理由是
时,需熄灭酒精灯,理由是_______ 。
(3) 和
和 的反应产物可能会有
的反应产物可能会有 和
和 ,为防止产品中带入
,为防止产品中带入 ,除了通入过量氯气外,应控制温度在
,除了通入过量氯气外,应控制温度在_______ 范围内(填字母)。
a.114~232℃ b.232~652℃ c.652~2260℃ d.114~246℃
(4)为了确认丁中有 的生成,可选用以下
的生成,可选用以下_______ 检验(填字母)。
a.稀盐酸 b.酸性高锰酸钾溶液
c.滴有 溶液的
溶液的 溶液 d.双氧水
溶液 d.双氧水
(5)碘氧化法滴定分析产品中 (Ⅱ)的含量。准确称取
(Ⅱ)的含量。准确称取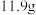 产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用
产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用 碘标准溶液滴定,滴入最后一滴,出现
碘标准溶液滴定,滴入最后一滴,出现_______ 现象时达到滴定终点,此时消耗碘标准溶液 ,则产品中
,则产品中 (Ⅱ)的质量分数为
(Ⅱ)的质量分数为_______ 。
 )用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,可用下图装置制备四氯化锡。
)用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,可用下图装置制备四氯化锡。
有关信息如下表:
化学式 |
|
|
|
熔点/℃ | 232 | 246 |
|
沸点/℃C | 2260 | 652 | 114 |
其他性质 | 银白色固体金属 | 无色晶体, (Ⅱ)易被 (Ⅱ)易被 、 、 等氧化为 等氧化为  (Ⅳ) (Ⅳ) | 无色液体,易水解 |
(2)将如图装置连接好,先检查装置的气密性,再慢慢滴入浓盐酸,待观察到
 时,需熄灭酒精灯,理由是
时,需熄灭酒精灯,理由是(3)
 和
和 的反应产物可能会有
的反应产物可能会有 和
和 ,为防止产品中带入
,为防止产品中带入 ,除了通入过量氯气外,应控制温度在
,除了通入过量氯气外,应控制温度在a.114~232℃ b.232~652℃ c.652~2260℃ d.114~246℃
(4)为了确认丁中有
 的生成,可选用以下
的生成,可选用以下a.稀盐酸 b.酸性高锰酸钾溶液
c.滴有
 溶液的
溶液的 溶液 d.双氧水
溶液 d.双氧水(5)碘氧化法滴定分析产品中
 (Ⅱ)的含量。准确称取
(Ⅱ)的含量。准确称取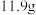 产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用
产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用 碘标准溶液滴定,滴入最后一滴,出现
碘标准溶液滴定,滴入最后一滴,出现 ,则产品中
,则产品中 (Ⅱ)的质量分数为
(Ⅱ)的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
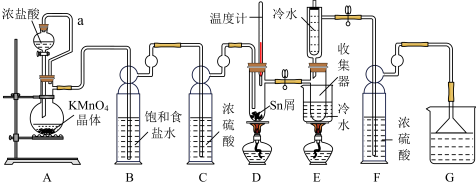
【推荐1】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点 与
与 反应制备
反应制备 ,装置如图。
,装置如图。
已知: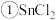 、
、 有关物理性质:
有关物理性质:
 极易水解生成
极易水解生成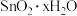 。回答下列问题:
。回答下列问题:
(1)导管a的作用是____________ ,装置A中发生反应的离子方程式为____________________ 。
(2)当观察到装置F液面上方___________ 时才开始点燃D处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是
________ ;
______
(3)若上述装置中缺少装置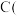 其它均相同),则D处具支试管中发生的主要副反应化学方程式为
其它均相同),则D处具支试管中发生的主要副反应化学方程式为_________________________________ 。
(4) 和锡的反应产物有
和锡的反应产物有 和
和 ,为防止产品中带入过多的
,为防止产品中带入过多的 ,可采取的措施是
,可采取的措施是____________________________________________ 。
(5)滴定分析产品中2价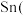 Ⅱ
Ⅱ 的含量:用分析天平称取
的含量:用分析天平称取 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用
产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 的碘标准溶液滴定至终点时消耗
的碘标准溶液滴定至终点时消耗 ,则产品中
,则产品中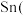 Ⅱ
Ⅱ 的质量分数为
的质量分数为___________ 。 小数点后保留2位,已知
小数点后保留2位,已知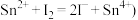
 与
与 反应制备
反应制备 ,装置如图。
,装置如图。 
已知:
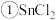 、
、 有关物理性质:
有关物理性质: | 物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
| SnCl2 | 无色晶体 | 246 | 652 |
| SnCl4 | 无色液体 | -33 | 114 |
 极易水解生成
极易水解生成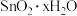 。回答下列问题:
。回答下列问题: (1)导管a的作用是
(2)当观察到装置F液面上方


(3)若上述装置中缺少装置
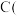 其它均相同),则D处具支试管中发生的主要副反应化学方程式为
其它均相同),则D处具支试管中发生的主要副反应化学方程式为(4)
 和锡的反应产物有
和锡的反应产物有 和
和 ,为防止产品中带入过多的
,为防止产品中带入过多的 ,可采取的措施是
,可采取的措施是(5)滴定分析产品中2价
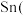 Ⅱ
Ⅱ 的含量:用分析天平称取
的含量:用分析天平称取 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用
产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用 的碘标准溶液滴定至终点时消耗
的碘标准溶液滴定至终点时消耗 ,则产品中
,则产品中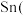 Ⅱ
Ⅱ 的质量分数为
的质量分数为 小数点后保留2位,已知
小数点后保留2位,已知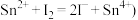
您最近一年使用:0次
【推荐2】锌灰是热镀锌厂和电解锌厂在生产过程中产生的一种副产品,主要成分为ZnO、ZnCl2,还含有SiO2、CuO、PbO和FeO。工业上利用锌灰制ZnSO4·7H2O晶体,进而获取ZnO,并探索氢电极增压还原氧化锌电解法制锌的方法,工艺流程如图所示:
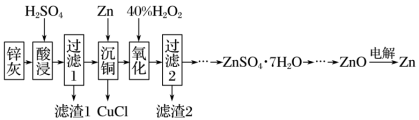
已知:Cu++Cl-=CuCl↓。回答下列问题:
(1)酸浸时,H2SO4应选用____ (填“浓硫酸”或“稀硫酸”)。
(2)滤渣1的主要成分有____ 。
(3)写出“沉铜”时的离子方程式:_____ 。
(4)“氧化”后,加入聚丙烯酰胺絮凝剂并加热搅拌,其目的是___ 。
(5)氢电极增压还原氧化锌的装置如图所示,储罐内ZnO溶解后形成Zn(OH) 离子,每溶解1molZnO需消耗
离子,每溶解1molZnO需消耗___ molKOH。电解池中的总反应离子方程式为____ 。
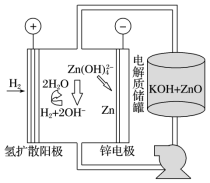
(6)该工艺废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S⇌ZnS(s)+2H+。处理后的废水中部分微粒浓度为
处理后的废水的pH=____ ,c(Zn2+)=____ 。[已知:Ksp(ZnS)=1.0×10-23,Ka1(H2S)=1.0×10-7,Ka2(H2S)=1.0×10-14,Ka(CH3COOH)=2.0×10-5]

已知:Cu++Cl-=CuCl↓。回答下列问题:
(1)酸浸时,H2SO4应选用
(2)滤渣1的主要成分有
(3)写出“沉铜”时的离子方程式:
(4)“氧化”后,加入聚丙烯酰胺絮凝剂并加热搅拌,其目的是
(5)氢电极增压还原氧化锌的装置如图所示,储罐内ZnO溶解后形成Zn(OH)
 离子,每溶解1molZnO需消耗
离子,每溶解1molZnO需消耗
(6)该工艺废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S⇌ZnS(s)+2H+。处理后的废水中部分微粒浓度为
| 微粒 | H2S | CH3COOH | CH3COO- |
| 浓度/(mol·L-1) | 0.10 | 0.05 | 0.10 |
处理后的废水的pH=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】Cu2(OH)2CO3是用途广泛的化工原料。可用电解废渣[含Cu(NO3)2、AgNO3]和纯碱为原料制备。
(1)制备CuSO4溶液

①过程Ⅰ中,分解产生的气体除NO2外,一定还含有_______ 。
②过程Ⅱ中,分离所采用的试剂是_______ 。
(2)制备Cu2(OH)2CO3
ⅰ.取Na2CO3溶液于锥形瓶中,水浴加热至适当温度。
ⅱ.将CuSO4 溶液逐滴加入到Na2CO3溶液中,产生沉淀,静置。
ⅲ.待沉淀完全沉降后,减压过滤、洗涤、干燥。
①步骤ⅰ中加热Na2CO3溶液的目的是_______ 。
②步骤ⅱ中生成Cu2(OH)2CO3的化学方程式为_______ 。
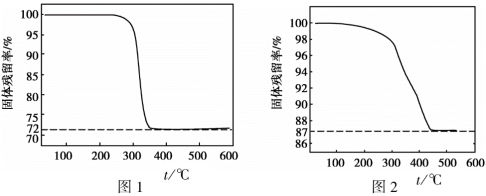
(3)设n(Na2CO3):n(CuSO4)=m,m不同时,所得产物纯度不同。通过测定固体样品的热重分析曲线(样品质量随温度变化曲线),获得固体残留率可检测样品纯度。(已知:固体残留率= ×100%)。
×100%)。
①写出Cu2(OH)2CO3分解的化学方程式_______ 。
②图1、图2分别是m = 1.2和m = 0.8时所得固体的热重分析曲线,依据下列曲线判断制备Cu2(OH)2CO3适宜的m =_______ (填“1.2”或“0.8”)。通过定量分析说明理由:_______ 。
(1)制备CuSO4溶液

①过程Ⅰ中,分解产生的气体除NO2外,一定还含有
②过程Ⅱ中,分离所采用的试剂是
(2)制备Cu2(OH)2CO3
ⅰ.取Na2CO3溶液于锥形瓶中,水浴加热至适当温度。
ⅱ.将CuSO4 溶液逐滴加入到Na2CO3溶液中,产生沉淀,静置。
ⅲ.待沉淀完全沉降后,减压过滤、洗涤、干燥。
①步骤ⅰ中加热Na2CO3溶液的目的是
②步骤ⅱ中生成Cu2(OH)2CO3的化学方程式为
(3)设n(Na2CO3):n(CuSO4)=m,m不同时,所得产物纯度不同。通过测定固体样品的热重分析曲线(样品质量随温度变化曲线),获得固体残留率可检测样品纯度。(已知:固体残留率=
 ×100%)。
×100%)。①写出Cu2(OH)2CO3分解的化学方程式
②图1、图2分别是m = 1.2和m = 0.8时所得固体的热重分析曲线,依据下列曲线判断制备Cu2(OH)2CO3适宜的m =

您最近一年使用:0次





