第IIA族元素在地壳内蕴藏较丰富,其单质和化合物用途广泛。回答下列问题:
(1)基态Ca原子M能层有_______ 个运动状态不同的电子,Mn和Ca属于同一周期,且核外最外层电子构型相同,但金属Mn的熔沸点等都比金属Ca高,原因______ 。
(2)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,Ca(ClO3)2中的阴离子空间构型是_________ ,中心原子的杂化方式为_______ 。
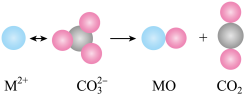
(3)碳酸盐的热分解示意图如下图所示。热分解温度:CaCO3__________ (填“高于”或“低于”)SrCO3,原因是_______ 。从成键轨道看,CO2分子内的化学键类型有________ 。
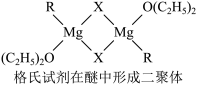
(4)格氏试剂RMgX是镁和卤代烃反应的产物,它在醚的稀溶液中以单体形式存在,在浓溶液中以二聚体存在,二聚体结构如下图所示。请在图中标出二聚体中的配位键__________ 。
(1)基态Ca原子M能层有
(2)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,Ca(ClO3)2中的阴离子空间构型是
(3)碳酸盐的热分解示意图如下图所示。热分解温度:CaCO3

(4)格氏试剂RMgX是镁和卤代烃反应的产物,它在醚的稀溶液中以单体形式存在,在浓溶液中以二聚体存在,二聚体结构如下图所示。请在图中标出二聚体中的配位键

更新时间:2020-06-17 15:57:53
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
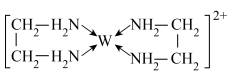
【推荐1】X、Y、Z、V、W为五种前四周期元素,其中X是短周期(除稀有气体外)原子半径最大的元素;Y与X同周期,其最高价氧化物对应的水化物呈两性;Z原子基态时2p原子轨道上有3个未成对的电子;V原子的核外电子排布式为1s22s22p63s2;W的原子序数为29,W的离子能与乙二胺(H2N—CH2—CH2—NH2)形成配离子:
回答下列问题:
(1)W原子的核外价电子排布式为___ ,该配离子中含有的化学键类型有___ (填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
(2)元素X、Y、V第一电离能由大到小的顺序是___ (用元素符号表示)。
(3)Z的氢化物的空间构型是___ ;该氢化物的沸点比甲烷的高,其主要原因是___ ;Z的另一种氢化物Z2H4分子中Z原子轨道的杂化类型是___ 。
(4)X和Cl元素构成的化合物XCl,XCl的晶胞结构如图所示,晶体中X+的配位数是___ 。每个X+周围与其紧邻的Cl-围成的几何图形为___ 。若W晶体中一个晶胞的边长为apm,则W晶体的密度为___ g/cm3(写出含a的表达式,用NA表示阿伏加 德罗常数)。


回答下列问题:
(1)W原子的核外价电子排布式为
a.配位键 b.极性键 c.离子键 d.非极性键
(2)元素X、Y、V第一电离能由大到小的顺序是
(3)Z的氢化物的空间构型是
(4)X和Cl元素构成的化合物XCl,XCl的晶胞结构如图所示,晶体中X+的配位数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
(1)基态Ti原子的核外电子排布式为_______ 。
(2)Ti的四卤化物熔点如下表所示:
TiF4熔点高于其他三种卤化物,写出TiF4的电子式_______ ;TiCl4至TiI4熔点依次升高,其原因是_______ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素钙位于元素周期表中的_______ 区,晶胞中Ti4+的配位数是_______ 。

(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH ,其晶胞如图(b)所示。有机碱CH3NH
,其晶胞如图(b)所示。有机碱CH3NH 中有配位键,提供空轨道的微粒是
中有配位键,提供空轨道的微粒是_______ ;图(a)中的Ca2+与图(b)中的_______ 空间位置相同。若图(b)中晶胞参数(边长)为anm,则晶体密度为_______ g·cm-3(列出计算式)。

(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示:
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图(a)所示,其组成元素钙位于元素周期表中的

(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH
 ,其晶胞如图(b)所示。有机碱CH3NH
,其晶胞如图(b)所示。有机碱CH3NH 中有配位键,提供空轨道的微粒是
中有配位键,提供空轨道的微粒是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】由IIA元素与VA元素所形成的化合物种类繁多,它们是探测器、激光器、微波器的重要材料。回答下列问题:
(1)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为_______ ,电子重排后的氧原子能量有所升高,原因是不符合_______ (填“泡利原理”或“洪特规则”)。
(2)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是_______ 。
(3)比较大小:键角CH4_______ (填“>”或“<”)NH3
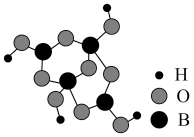
(4)如图为四硼酸根离子球棍模型,该离子符号为_______ ,其中硼原子轨道的杂化类型有_______ 。
(5)叠氮酸铵(NH4N3)是一种具有爆炸性的无色晶体。叠氮酸根(N )的空间结构为
)的空间结构为_______ ;叠氮酸铵的晶胞如图所示,其晶胞参数为a nm和0.5a nm,阿伏加德罗常数的值为NA,NH4N3的密度为_______ g·cm-3。
(1)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(2)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是
| 化学键 | B-H | B-O | B-B |
| 键能(kJ∙mol-1) | 389 | 561 | 293 |
(3)比较大小:键角CH4
(4)如图为四硼酸根离子球棍模型,该离子符号为

(5)叠氮酸铵(NH4N3)是一种具有爆炸性的无色晶体。叠氮酸根(N
 )的空间结构为
)的空间结构为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中显示出良好的应用前景。回答下列问题:
(1)下列N原子电子排布图表示的状态中,能量最低和最高的分别为__________ 、__________ 。(填标号)
A.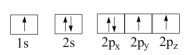 B.
B. 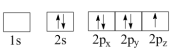
C.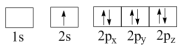 D.
D. 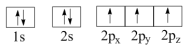
(2)N3-与Na+具有相同的电子构型,r(N3-)大于r(Na+),原因是____________________ 。
(3)Ca3(PO4)2在食品工业中用作抗结剂、营养增补剂,Ca3(PO4)2中的阴离子空间构型是__________ ,中心原子P的杂化形式为__________ 。Ca3(PO4)2中,存在__________ (填标号)。
A离子键 B.σ键 C.π键 D.氢键
(4)受民间中医启发,科研工作者发现As2O3(俗称砒霜,或写作As4O6)对白血病有明显的治疗作用。As4O6的分子结构如1所示,则在该化合物中As原子的杂化轨道数目为__________ ,As原子的第一电离能__________ (填“>”“=”或“<”)O原子的第一电离能。
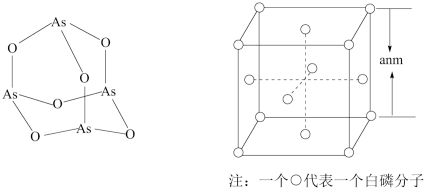
(5)白磷(P4)的晶体属于分子晶体,其晶胞结构如图所示。已知晶胞参数为anm,阿伏伽德罗常数的数值为NA,则P4的密度为__________ (列出计算式)g·cm-3。
(1)下列N原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. 
C.
 D.
D. 
(2)N3-与Na+具有相同的电子构型,r(N3-)大于r(Na+),原因是
(3)Ca3(PO4)2在食品工业中用作抗结剂、营养增补剂,Ca3(PO4)2中的阴离子空间构型是
A离子键 B.σ键 C.π键 D.氢键
(4)受民间中医启发,科研工作者发现As2O3(俗称砒霜,或写作As4O6)对白血病有明显的治疗作用。As4O6的分子结构如1所示,则在该化合物中As原子的杂化轨道数目为

(5)白磷(P4)的晶体属于分子晶体,其晶胞结构如图所示。已知晶胞参数为anm,阿伏伽德罗常数的数值为NA,则P4的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】中科院大连化学物理研究所科学家用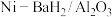 、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《NatureEnergy》杂志上。
、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《NatureEnergy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸( )是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸的晶体类型是___________ ,其分子中碳原子的杂化方式为___________ 。
(3)比较 分子(前者)和在
分子(前者)和在 中
中 (后者)分子中
(后者)分子中 的键角大小,前者
的键角大小,前者___________ 后者(填“>”、“<”或“=”),原因是___________ 。1mol 中含有σ键的物质的量为
中含有σ键的物质的量为___________ mol。
(4)亚氨基锂(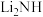 ,摩尔质量为Mg/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,
,摩尔质量为Mg/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,
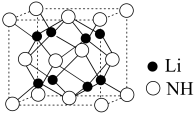
若晶胞参数为dpm,密度为ρg/cm ,则阿伏加德罗常数
,则阿伏加德罗常数
___________ mol (列出表达式)。
(列出表达式)。
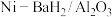 、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《NatureEnergy》杂志上。
、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《NatureEnergy》杂志上。(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(
 )是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸的晶体类型是
(3)比较
 分子(前者)和在
分子(前者)和在 中
中 (后者)分子中
(后者)分子中 的键角大小,前者
的键角大小,前者 中含有σ键的物质的量为
中含有σ键的物质的量为(4)亚氨基锂(
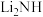 ,摩尔质量为Mg/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,
,摩尔质量为Mg/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,
若晶胞参数为dpm,密度为ρg/cm
 ,则阿伏加德罗常数
,则阿伏加德罗常数
 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
【推荐3】形形色色的物质,构成了我们这个五彩缤纷的世界。世上万物,神奇莫测,常常超乎人们按“常理"的想象。学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1)基态Ga原子的核外电子排布式是[Ar]_____________ ,基态Ga原子核外电子占据最高能级的电子云轮廓图为___________ 。
(2)硒的含氧酸有H2SeO3,H2SeO4。酸性:H2SeO3____________ H2SeO4(填“>”“<”或“=”)。SeO32的空间构型是_____________________ 。
(3)NaN3是汽车安全气囊中的主要化学成分,其阴离子的立体构型为_____________ 。写出和该阴离子互为等电子体的一种分子的结构式_______________ 。
(4)钙和铁都是第四周期元素,且原子的最外层电子数相同,铁的熔沸点远高于钙,其原因是_____ 。
(5)配体中配位原子提供孤电子对的能力与元素的电负性有关,SCN-的结构式可以表示为[S=C=N]-或[S-C≡N]-,SCN-与Fe3+、Au+和Hg2+等离子能形成配离子,N、C、S的电负性依次为3.0、2.5和2.5。SCN-中提供孤电子对的原子可能是_______ 。
(6)某离子晶体XY2的晶胞结构如图所示。
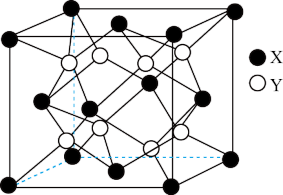
①晶体中在每个X周围与它最近且距离相等的X共有_________ 个。
②设该晶体的摩尔质量为Mg·mol-1,晶胞的密度为ρg.cm-3,阿伏加 德罗常数为NA,则晶体中两个最近的X间的距离为________ cm。
(1)基态Ga原子的核外电子排布式是[Ar]
(2)硒的含氧酸有H2SeO3,H2SeO4。酸性:H2SeO3
(3)NaN3是汽车安全气囊中的主要化学成分,其阴离子的立体构型为
(4)钙和铁都是第四周期元素,且原子的最外层电子数相同,铁的熔沸点远高于钙,其原因是
(5)配体中配位原子提供孤电子对的能力与元素的电负性有关,SCN-的结构式可以表示为[S=C=N]-或[S-C≡N]-,SCN-与Fe3+、Au+和Hg2+等离子能形成配离子,N、C、S的电负性依次为3.0、2.5和2.5。SCN-中提供孤电子对的原子可能是
(6)某离子晶体XY2的晶胞结构如图所示。

①晶体中在每个X周围与它最近且距离相等的X共有
②设该晶体的摩尔质量为Mg·mol-1,晶胞的密度为ρg.cm-3,阿伏加 德罗常数为NA,则晶体中两个最近的X间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】Mn能改善钢材热加工性能,并改善钢材的冷脆倾向,同时不显著降低钢材的塑性、冲击韧性。根据要求回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ ,
基态Mn原子能级最高的电子的电子云轮廓图形状为_______ 。
(2)Fe、Mn元素的部分电离能数据如下表:
从上表两元素部分电离能数据的比较可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,原因是
再失去一个电子难,原因是_______ 。
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物,其结构为
形成黄色的配合物,其结构为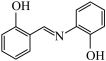 。
。
①锰试剂分子中,电负性最大的原子是_______ ,采取 杂化的原子是
杂化的原子是_______ ;
②锰试剂分子中能与 形成配位键的原子是
形成配位键的原子是_______ 。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。
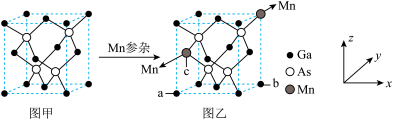
①图乙中a点和c点的原子坐标参数分别为(0,0,0)和 ,则b点的原子坐标参数为
,则b点的原子坐标参数为_______ ;
②设图甲晶体的密度为 ,设
,设 表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为
表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为_______ pm(用含 、
、 的关系式表示最简化的计算式即可)。
的关系式表示最简化的计算式即可)。
(1)
 的核外电子排布式为
的核外电子排布式为基态Mn原子能级最高的电子的电子云轮廓图形状为
(2)Fe、Mn元素的部分电离能数据如下表:
| 元素 | Fe | Mn | |
电离能/( ) ) |  | 759 | 717 |
 | 1561 | 1509 | |
 | 2957 | 3248 | |
 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,原因是
再失去一个电子难,原因是(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与
 形成黄色的配合物,其结构为
形成黄色的配合物,其结构为 。
。①锰试剂分子中,电负性最大的原子是
 杂化的原子是
杂化的原子是②锰试剂分子中能与
 形成配位键的原子是
形成配位键的原子是(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。

①图乙中a点和c点的原子坐标参数分别为(0,0,0)和
 ,则b点的原子坐标参数为
,则b点的原子坐标参数为②设图甲晶体的密度为
 ,设
,设 表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为
表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为 、
、 的关系式表示最简化的计算式即可)。
的关系式表示最简化的计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁是一种重要的过渡元素,能形成多种物质,如做染料的普鲁士蓝(化学式为KFe[Fe(CN)6])。
Ⅰ.(1)Fe2+基态核外电子排布式为__ 。
(2)在普鲁士蓝中,中心离子是__ ,配体是__ 。
(3)一定条件下,CN-可氧化为OCN-。OCN-中三种元素的第一电离能由大到小的顺序为__ ;CN-中碳原子采取sp杂化,1 mol KFe[Fe(CN)6]中含有的π键数目为__ 。
Ⅱ.(1)某工厂为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程中,消耗的原料是__ 。有关反应的化学方程式为__ 。
(2)有一溶液中含有Ag+、Fe3+、Cu2+和Al3+四种阳离子,怎样把这些阳离子以沉淀的形式一一分离出来?___ 。
(3)制氧化亚铁常用:4FeC2O4 4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。
4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。___ 。
(4)在新生代的海水里有一种铁细菌,它们摄取海水中的亚铁离子,把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉淀下来形成铁矿;这个用酶作催化剂反应的另一个反应物是CO2,它在反应后转变成有机物,可用甲醛来表示。试写出配平的离子方程式__ 。
Ⅰ.(1)Fe2+基态核外电子排布式为
(2)在普鲁士蓝中,中心离子是
(3)一定条件下,CN-可氧化为OCN-。OCN-中三种元素的第一电离能由大到小的顺序为
Ⅱ.(1)某工厂为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程中,消耗的原料是
(2)有一溶液中含有Ag+、Fe3+、Cu2+和Al3+四种阳离子,怎样把这些阳离子以沉淀的形式一一分离出来?
(3)制氧化亚铁常用:4FeC2O4
 4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。
4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。(4)在新生代的海水里有一种铁细菌,它们摄取海水中的亚铁离子,把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉淀下来形成铁矿;这个用酶作催化剂反应的另一个反应物是CO2,它在反应后转变成有机物,可用甲醛来表示。试写出配平的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碳和硫的化合物种类繁多,应用广泛。例如 是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
Ⅰ. 曾广泛用作溶剂、灭火剂。
曾广泛用作溶剂、灭火剂。
(1)基态氯原子核外电子的空间运动状态有______ 种。基态碳原子的价电子排布是否可以表示为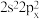 ,
,______ (填“是”或“否”),原因为______ 。
(2) 在
在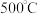 以上时可以与水反应,产生有毒的光气
以上时可以与水反应,产生有毒的光气 常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有
常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有______ (填标号)。
a. 的原子半径更大 b.
的原子半径更大 b. 键的键能更大 c.
键的键能更大 c. 键的极性更大d.
键的极性更大d. 有更多的价层轨道
有更多的价层轨道
光气分子中 的键角
的键角______ (填“大于”、“小于”或“等于”)甲醛分子中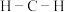 的键角,原因为
的键角,原因为______ 。
Ⅱ.硫代硫酸盐可用于矿石提取银、鞣制皮革等。
(3)硫代硫酸根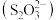 中心原子的杂化方式为
中心原子的杂化方式为______ 。硫代硫酸盐用于矿石提取银时形成 ,该配合物中提供孤电子对的原子为
,该配合物中提供孤电子对的原子为______ (填标号),原因为______ 。
a.端基硫原子 b.中心硫原子 c.氧原子
(4)某硫代硫酸盐的晶胞结构如图。 的
的
______ 。原子 的分数坐标为
的分数坐标为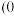 ,
, ,则原子
,则原子 的分数坐标为
的分数坐标为______ 。
 是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。Ⅰ.
 曾广泛用作溶剂、灭火剂。
曾广泛用作溶剂、灭火剂。(1)基态氯原子核外电子的空间运动状态有
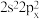 ,
,(2)
 在
在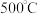 以上时可以与水反应,产生有毒的光气
以上时可以与水反应,产生有毒的光气 常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有
常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有a.
 的原子半径更大 b.
的原子半径更大 b. 键的键能更大 c.
键的键能更大 c. 键的极性更大d.
键的极性更大d. 有更多的价层轨道
有更多的价层轨道光气分子中
 的键角
的键角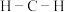 的键角,原因为
的键角,原因为Ⅱ.硫代硫酸盐可用于矿石提取银、鞣制皮革等。
(3)硫代硫酸根
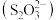 中心原子的杂化方式为
中心原子的杂化方式为 ,该配合物中提供孤电子对的原子为
,该配合物中提供孤电子对的原子为a.端基硫原子 b.中心硫原子 c.氧原子
(4)某硫代硫酸盐的晶胞结构如图。
 的
的
 的分数坐标为
的分数坐标为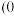 ,
, ,则原子
,则原子 的分数坐标为
的分数坐标为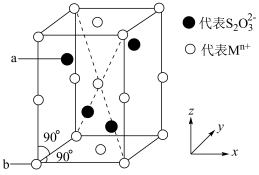
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Fe的基态原子价电子排布式为___________ 。
②Ti的基态原子共有________ 种不同能级的电子。
(2)制备 的反应为
的反应为 。
。
①上述化学方程式中 是
是___________ (“极性”或“非极性”)分子。
② 分子中所有原子均满足8电子稳定结构,
分子中所有原子均满足8电子稳定结构, 分子中
分子中 键和
键和 键的个数比为
键的个数比为___________ ,该分子的空间结构为___________ 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中 和
和 的离子半径分别为
的离子半径分别为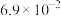 nm和
nm和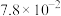 nm。则熔点:NiO
nm。则熔点:NiO___________ FeO(填“>”“<”或“=”)。
(4)镧镍合金( )具有很强的储氢能力,其晶胞结构如图,其中x=
)具有很强的储氢能力,其晶胞结构如图,其中x=___________ 。已知晶胞体积为V ,若储氢后形成
,若储氢后形成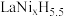 (氢进入晶胞空隙,晶胞体积不变),
(氢进入晶胞空隙,晶胞体积不变), 为阿伏加德罗常数的值,则氢在合金中的密度为
为阿伏加德罗常数的值,则氢在合金中的密度为___________  。(用含V、
。(用含V、 的代数式表示)。
的代数式表示)。 。
。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Fe的基态原子价电子排布式为
②Ti的基态原子共有
(2)制备
 的反应为
的反应为 。
。①上述化学方程式中
 是
是②
 分子中所有原子均满足8电子稳定结构,
分子中所有原子均满足8电子稳定结构, 分子中
分子中 键和
键和 键的个数比为
键的个数比为(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中
 和
和 的离子半径分别为
的离子半径分别为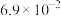 nm和
nm和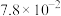 nm。则熔点:NiO
nm。则熔点:NiO(4)镧镍合金(
 )具有很强的储氢能力,其晶胞结构如图,其中x=
)具有很强的储氢能力,其晶胞结构如图,其中x= ,若储氢后形成
,若储氢后形成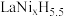 (氢进入晶胞空隙,晶胞体积不变),
(氢进入晶胞空隙,晶胞体积不变), 为阿伏加德罗常数的值,则氢在合金中的密度为
为阿伏加德罗常数的值,则氢在合金中的密度为 。(用含V、
。(用含V、 的代数式表示)。
的代数式表示)。 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别是__ 、__ (填标号)。
A.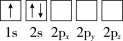 B.
B.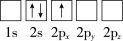
C.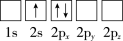 D.
D.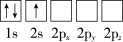
(2)r(Li+)__ r(H-),原因是___ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是__ 。中心原子的杂化形式为___ 。LiAlH4中,存在__ (填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图a的BornHaber循环计算得到。
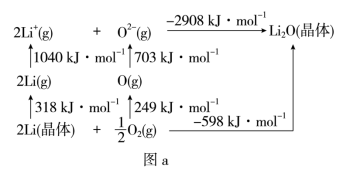
可知,Li原子的第一电离能为__ kJ·mol-1,O=O键键能为__ kJ·mol-1,Li2O晶格能为__ kJ·mol-1。
(5)Li2O具有反萤石结构,晶胞如图b所示,已知晶胞参数为0.4665nm,阿伏加 德罗常数的值为NA,则Li2O的密度为___ g·cm-3(列出计算式)。
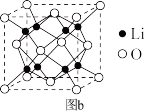
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别是
A.
 B.
B.
C.
 D.
D.
(2)r(Li+)
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图a的BornHaber循环计算得到。
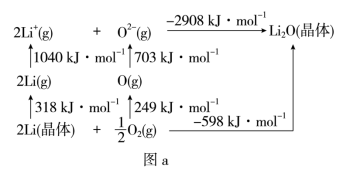
可知,Li原子的第一电离能为
(5)Li2O具有反萤石结构,晶胞如图b所示,已知晶胞参数为0.4665nm,阿伏加 德罗常数的值为NA,则Li2O的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰三位科学家,以表彰他们对锂离子电池的研究。
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______ ,中心原子的杂化形式为___ ,与阴离子互为等电子体的一种分子为_________
(2)Li2O是离子晶体,其晶格能可通过下图的Born-Haber循环计算得到。
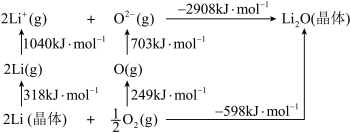
可知Li原子的第一电离能为____ kJ·mol-1,O=O键键能为_____ kJ·mol-1,Li2O晶格能为_____ kJ·mol-1
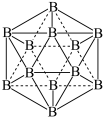
(3)硼和锂同周期,B原子核外有__ 种不同运动状态的电子。基态B原子中,能量最高的电子所占据的原子轨道的形状为____ 。晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(如下图),每个顶点为一个硼原子,每个三角形均为等边三角形。则每一个此基本结构单元由___ 个硼原子构成;若该结构单元中有2个原子为10B(其余为11B),那么该结构单元有____ 种不同类型
(4)锰的化合物也广泛应用于电池,基态锰原子的核外电子排布式为____ ,MnO的熔点(1650 ℃)比MnS的熔点(1610 ℃)高的原因是_________ ,含锰的一种磁性材料的单晶胞结构如图:
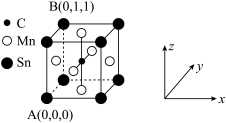
该晶胞中碳原子的原子坐标为_________
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
(2)Li2O是离子晶体,其晶格能可通过下图的Born-Haber循环计算得到。
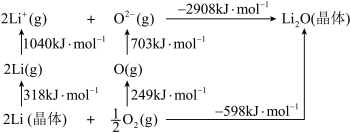
可知Li原子的第一电离能为
(3)硼和锂同周期,B原子核外有

(4)锰的化合物也广泛应用于电池,基态锰原子的核外电子排布式为

该晶胞中碳原子的原子坐标为
您最近一年使用:0次



