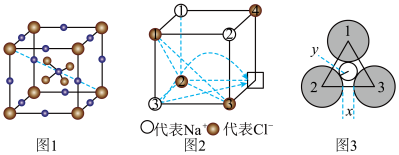
快离子导体是一类具有优良离子导电能力的固体电解质。图1(Li3SBF4)和图2是潜在的快离子导体材料的结构示意图。回答下列问题:
(1)BF3+NH3=NH3·BF3的反应过程中,形成配位键时提供电子的原子是__ ,其提供的电子所在的轨道是__ 。
(2)基态Li+、B+分别失去一个电子时,需吸收更多能量的是__ ,理由是__ 。
(3)图1所示的晶体中,锂原子处于立方体的位置__ 。若其晶胞参数为apm,则晶胞密度为___ g·cm-3(列出计算式即可)。
(4)氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中,则每一个空隙由__ 个Cl-构成,空隙的空间形状为___ 。
(5)当图2中方格内填入Na+时,恰好构成氯化钠晶胞的 ,且氯化钠晶胞参数a=564pm。温度升高时,NaCl晶体出现缺陷(如图2所示,某一个顶点没有Na+,出现空位),晶体的导电性大大增强。该晶体导电时,在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图2中箭头所示):
,且氯化钠晶胞参数a=564pm。温度升高时,NaCl晶体出现缺陷(如图2所示,某一个顶点没有Na+,出现空位),晶体的导电性大大增强。该晶体导电时,在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图2中箭头所示):
途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x,如图3)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。已知:r(Cl-)=185pm, =1.4,
=1.4, =1.7。
=1.7。
①x=__ ,y=__ ;(保留一位小数)
②迁移可能性更大的途径是__ 。

(1)BF3+NH3=NH3·BF3的反应过程中,形成配位键时提供电子的原子是
(2)基态Li+、B+分别失去一个电子时,需吸收更多能量的是
(3)图1所示的晶体中,锂原子处于立方体的位置
(4)氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中,则每一个空隙由
(5)当图2中方格内填入Na+时,恰好构成氯化钠晶胞的
 ,且氯化钠晶胞参数a=564pm。温度升高时,NaCl晶体出现缺陷(如图2所示,某一个顶点没有Na+,出现空位),晶体的导电性大大增强。该晶体导电时,在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图2中箭头所示):
,且氯化钠晶胞参数a=564pm。温度升高时,NaCl晶体出现缺陷(如图2所示,某一个顶点没有Na+,出现空位),晶体的导电性大大增强。该晶体导电时,在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图2中箭头所示):途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x,如图3)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。已知:r(Cl-)=185pm,
 =1.4,
=1.4, =1.7。
=1.7。①x=
②迁移可能性更大的途径是
更新时间:2020-07-10 13:48:03
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】稀土元素是指钪(Sc)、钇(Y)和镧系元素,共17种,位于元素周期表中第ⅢB族,均为金属元素,在工业生产中有重要的作用。回答下列问题:
(1)基态钪(Sc)元素的原子核外电子占据的轨道数目共_____ 个,钇(Y)位于元素周期表中钪(Sc)的下一周期,钇(Y)的价电子轨道表达式为_____ 。
(2)稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,有一个能提供孤电子对的原子为一齿,(羰基中的氧原子不能提供孤对电子),EDTA( )是
)是_____ 齿配位体,EDTA所含元素原子第一电离能由大到小顺序为_____ 。
(3)钪(Sc)离子在水中以稳定对称的 存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为
存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为_____ 。
(4)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。

①甘氨酸铜中铜原子的杂化类型为_____ (填“ ”或“
”或“ ”)。
”)。
②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是_____ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。铁酸钇( )的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
)的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
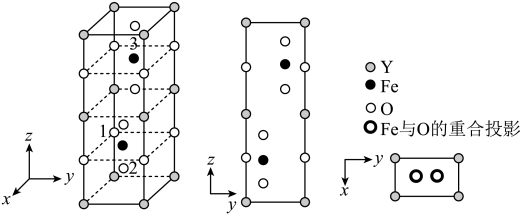
一个晶胞中有_____ 个O。已知1号O原子分数坐标为 ,2号O原子分数坐标为
,2号O原子分数坐标为 ,则3号Fe原子的分数坐标为
,则3号Fe原子的分数坐标为_____ 。
(1)基态钪(Sc)元素的原子核外电子占据的轨道数目共
(2)稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,有一个能提供孤电子对的原子为一齿,(羰基中的氧原子不能提供孤对电子),EDTA(
 )是
)是(3)钪(Sc)离子在水中以稳定对称的
 存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为
存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为(4)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。

①甘氨酸铜中铜原子的杂化类型为
 ”或“
”或“ ”)。
”)。②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。铁酸钇(
 )的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
)的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
一个晶胞中有
 ,2号O原子分数坐标为
,2号O原子分数坐标为 ,则3号Fe原子的分数坐标为
,则3号Fe原子的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】锌是一种重要的金属,锌及其化合物在生产生活中有着十分广泛的应用。
(1)基态锌原子的核外电子排布式为
_______ 。
(2)在“ ”过程中会
”过程中会_______ (填“吸收”或“释放”)能量。
(3)代森锌是一种广谱杀菌剂,广泛用于防治各种麦的锈病、马铃薯晚疫病等蔬菜病害,遇水可分解为 、
、 、
、 和
和 。代森锌的结构简式如图所示。
。代森锌的结构简式如图所示。

①代森锌中 、
、 、
、 、
、 四种元素的电负性由大到小的次序为
四种元素的电负性由大到小的次序为_______ ,C原子的杂化轨道类型为_______ 。
② 、
、 、
、 三种化合物中沸点最高的是
三种化合物中沸点最高的是 ,其主要原因是
,其主要原因是_______ 。
(4) 可用作甲醛去除剂,
可用作甲醛去除剂, 中
中 与
与 之间的配位键中提供孤电子对的成键原子是
之间的配位键中提供孤电子对的成键原子是_______ (填元素符号), 中σ键与π键的个数之比为
中σ键与π键的个数之比为_______ 。
(5)化合物 的晶胞结构如图,晶胞中部分离子的分数坐标如表所示,则
的晶胞结构如图,晶胞中部分离子的分数坐标如表所示,则 晶胞结构中位置A的微粒为
晶胞结构中位置A的微粒为_______ (填 或
或 ),一个
),一个 周围等距离且最近的
周围等距离且最近的 构成的空间构型为
构成的空间构型为_______ ;已知 晶体的密度为
晶体的密度为 ,则
,则 晶胞中的晶胞参数
晶胞中的晶胞参数
_______  (用
(用 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。

(1)基态锌原子的核外电子排布式为

(2)在“
 ”过程中会
”过程中会(3)代森锌是一种广谱杀菌剂,广泛用于防治各种麦的锈病、马铃薯晚疫病等蔬菜病害,遇水可分解为
 、
、 、
、 和
和 。代森锌的结构简式如图所示。
。代森锌的结构简式如图所示。
①代森锌中
 、
、 、
、 、
、 四种元素的电负性由大到小的次序为
四种元素的电负性由大到小的次序为②
 、
、 、
、 三种化合物中沸点最高的是
三种化合物中沸点最高的是 ,其主要原因是
,其主要原因是(4)
 可用作甲醛去除剂,
可用作甲醛去除剂, 中
中 与
与 之间的配位键中提供孤电子对的成键原子是
之间的配位键中提供孤电子对的成键原子是 中σ键与π键的个数之比为
中σ键与π键的个数之比为(5)化合物
 的晶胞结构如图,晶胞中部分离子的分数坐标如表所示,则
的晶胞结构如图,晶胞中部分离子的分数坐标如表所示,则 晶胞结构中位置A的微粒为
晶胞结构中位置A的微粒为 或
或 ),一个
),一个 周围等距离且最近的
周围等距离且最近的 构成的空间构型为
构成的空间构型为 晶体的密度为
晶体的密度为 ,则
,则 晶胞中的晶胞参数
晶胞中的晶胞参数
 (用
(用 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。
| 坐标 | x | y | z |
 |  |  |  |
 | 0 | 0 | 0 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题.

(1)E元素原子基态时的电子排布式为_________ .
(2)A2F分子中F原子的杂化类型是_________
(3)CA3极易溶于水,其原因主要是_________ ,
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为_________ ;1molC60分子中σ键的数目为_________ .

(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As_________ Se(填“>”“<”或“=”).
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是_________ 与S距离最近且等距离的S之间的距离为_________ (密度为ρg/cm3)

③二氧化硒分子的空间构型为_________ .

(1)E元素原子基态时的电子排布式为
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因主要是
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为

(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是

③二氧化硒分子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为___________ ;
(2)已知 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被
被 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为___________ ; 还可形成
还可形成 ,其中
,其中 代表
代表 。该配合物中,
。该配合物中, 模型为四面体的非金属原子共有
模型为四面体的非金属原子共有___________ 个。
(3)一种由 、
、 、
、 组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 ,晶体中
,晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如 点,
点, 点原子的分数坐标分别为
点原子的分数坐标分别为 、
、 ,则
,则 点原子的分数坐标为
点原子的分数坐标为___________ ,晶胞中 、
、 间距离
间距离
___________  。
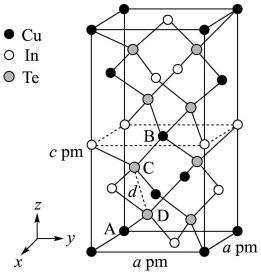
。 是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价
是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价 原子)。
原子)。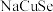 晶胞中0价
晶胞中0价 原子个数为
原子个数为___________ ,每个 晶胞完全转化为
晶胞完全转化为 晶胞,转移电子数为
晶胞,转移电子数为___________ 。
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为(2)已知
 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被
被 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为 还可形成
还可形成 ,其中
,其中 代表
代表 。该配合物中,
。该配合物中, 模型为四面体的非金属原子共有
模型为四面体的非金属原子共有(3)一种由
 、
、 、
、 组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 ,晶体中
,晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为 点,
点, 点原子的分数坐标分别为
点原子的分数坐标分别为 、
、 ,则
,则 点原子的分数坐标为
点原子的分数坐标为 、
、 间距离
间距离
 。
。
 是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价
是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价 原子)。
原子)。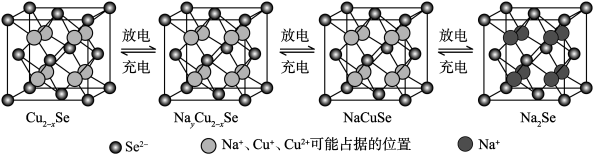
 晶胞中0价
晶胞中0价 原子个数为
原子个数为 晶胞完全转化为
晶胞完全转化为 晶胞,转移电子数为
晶胞,转移电子数为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】柔性显示材料M(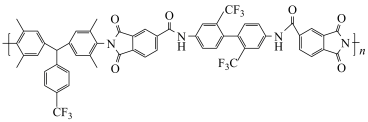 )的合成路线如下:
)的合成路线如下:
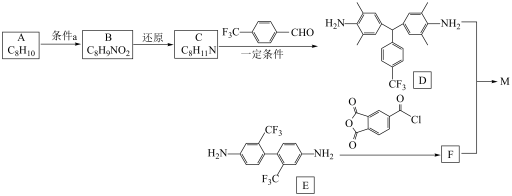
已知:①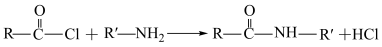
②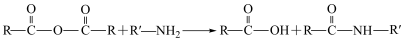
(2)C中所含官能团的名称为
(3)C生成D的反应化学方程式为
(4)E生成F的反应类型为
(5)满足下列条件的B的同分异构体有
①苯环上有三个取代基 ②能与NaOH溶液反应 ③能发生银镜反应
(6)根据合成M的反应原理推断合成T的单体结构简式,P为
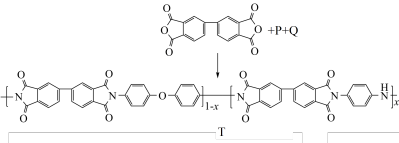
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】ⅢA族与ⅤA族元素及其化合物具有众多优良特性,可用于制作航天器等耐高温设备。回答下列问题。
(1)Al原子中电子占据的最高能层符号为_______ ,第三周期元素中第一电离能介于Al和P有_______ 种
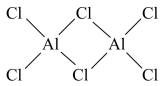
(2)AlCl3在气态时可以发生二聚,其分子式为Al2Cl6,其二聚体结构如图,请在图中以“→”表示该结构中存在的配位键。其中Cl-Al-Cl键角的大小情况是AlCl3_______ Al2Cl6(填“<”、“>”或“=”下同)原因为_______ 。
(3)咪唑结构为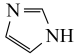 ,N原子的杂化类型为
,N原子的杂化类型为_______ ,分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为_______ 。
(4)噻唑结构与咪唑很相似,结构为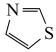 ,噻唑的熔沸点
,噻唑的熔沸点_______ 咪唑,原因是_______ 。
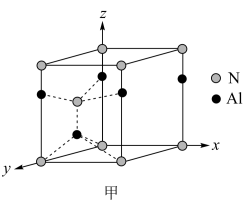
(5)氮化铝晶体是第三代半导体材料的典型代表之一,属于六方晶系,其晶胞结构如图甲所示,Al原子位于氮原子形成的_______ 空隙(填“正四面体”或“正八面体”)。已知晶胞的密度为ρ g·cm-3,两种原子半径分别为rN nm和rAl nm,阿伏加德罗常数值为NA,则该晶胞中原子的体积占晶胞体积的百分率为_______ 。(用含ρ、rN 、rAl和NA的代数式表示)
(1)Al原子中电子占据的最高能层符号为
(2)AlCl3在气态时可以发生二聚,其分子式为Al2Cl6,其二聚体结构如图,请在图中以“→”表示该结构中存在的配位键。其中Cl-Al-Cl键角的大小情况是AlCl3

(3)咪唑结构为
 ,N原子的杂化类型为
,N原子的杂化类型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则咪唑中的大π键可表示为(4)噻唑结构与咪唑很相似,结构为
 ,噻唑的熔沸点
,噻唑的熔沸点(5)氮化铝晶体是第三代半导体材料的典型代表之一,属于六方晶系,其晶胞结构如图甲所示,Al原子位于氮原子形成的

您最近一年使用:0次
【推荐1】镓、硒的单质及某些化合物(如砷化镓)是常用的半导体材料。在传统半导体材料的基础上,我国科学家又首次合成新型半导体材料——卤化物钙钛矿材料,该材料在太阳能电池、发光二极管和激光等领域有着巨大的应用前景。
回答下列问题:
(1)基态Ti的价电子排布图是__________ ,若钙原子核外电子有11种空间运动状态,则该原子处于___ (填“基态”或“激发态”)。
(2)AsCl3的分子结构与NH3类似,其中砷的杂化类型为___ ,分子空间构型为______ 。
(3)Ga可形成[Ga(NH3)4Cl2]Cl、[Ga(NH3)5Cl]Cl2、[Ga(NH3)6]Cl3等一系列配合物。
①组成该配合物的元素Ga、N、Cl的第一电离能由大到小的顺序为_______ 。
②在[Ga(NH3)4Cl2]Cl中配位数为______ ,中心体是_______ 。
(4)CaTiO3的晶胞为立方晶胞,结构如图所示。

①在晶胞中与Ti4+距离最近且相等的O2-有_____ 个。
②若最近的Ti4+和O2-之间的距离为a pm,则晶胞的密度为_______ g·cm-3(用代数式表示,NA为阿伏加德罗常数)。
回答下列问题:
(1)基态Ti的价电子排布图是
(2)AsCl3的分子结构与NH3类似,其中砷的杂化类型为
(3)Ga可形成[Ga(NH3)4Cl2]Cl、[Ga(NH3)5Cl]Cl2、[Ga(NH3)6]Cl3等一系列配合物。
①组成该配合物的元素Ga、N、Cl的第一电离能由大到小的顺序为
②在[Ga(NH3)4Cl2]Cl中配位数为
(4)CaTiO3的晶胞为立方晶胞,结构如图所示。

①在晶胞中与Ti4+距离最近且相等的O2-有
②若最近的Ti4+和O2-之间的距离为a pm,则晶胞的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】d区金属元素钛有“太空金属”“未来金属”等美誉,在航空航天、海洋产业等行业有重要作用。请回答下列问题:
(1)我国科学家用 和
和 ,制备超导材料
,制备超导材料 ,反应原理为
,反应原理为 。
。
①钛元素在元素周期表中的位置___________ ,基态钛原子的核外最高能层所含电子数___________ 。
②已知部分物质的熔沸点如下表。
 属于
属于___________ 晶体,应用所学知识解释 的熔点大于
的熔点大于 的原因
的原因___________ 。
③写出惰性电极电解 得到单质
得到单质 的化学方程式
的化学方程式___________ 。
(2) 是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子。甲、乙的水解产物化学式均为
是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子。甲、乙的水解产物化学式均为 ,但只有甲的水解产物能与草酸(
,但只有甲的水解产物能与草酸( )反应生成
)反应生成 。
。
①根据相似相溶的规律,可推断___________ (填“甲”或“乙”)在水中的溶解度较大。
② 发生水解反应的化学方程式是
发生水解反应的化学方程式是___________ 。
③ 中
中 的键角大于
的键角大于 分子中的
分子中的 键角,请结合所学知识解释原因
键角,请结合所学知识解释原因___________ 。
④查阅资料可知,甲、乙均为平面结构,画出乙的水解产物的空间结构___________ 。
(1)我国科学家用
 和
和 ,制备超导材料
,制备超导材料 ,反应原理为
,反应原理为 。
。①钛元素在元素周期表中的位置
②已知部分物质的熔沸点如下表。
 |  |  |  | |
熔点/ | 800(分解) | -25 | 714 | 2950 |
沸点/ | 700(升华) | 136.4 | 1412 | (略) |
 属于
属于 的熔点大于
的熔点大于 的原因
的原因③写出惰性电极电解
 得到单质
得到单质 的化学方程式
的化学方程式(2)
 是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子。甲、乙的水解产物化学式均为
是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子。甲、乙的水解产物化学式均为 ,但只有甲的水解产物能与草酸(
,但只有甲的水解产物能与草酸( )反应生成
)反应生成 。
。①根据相似相溶的规律,可推断
②
 发生水解反应的化学方程式是
发生水解反应的化学方程式是③
 中
中 的键角大于
的键角大于 分子中的
分子中的 键角,请结合所学知识解释原因
键角,请结合所学知识解释原因④查阅资料可知,甲、乙均为平面结构,画出乙的水解产物的空间结构
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)往硫酸铜溶液中加入氨水,先形成蓝色沉淀,继续加氨水,得到深蓝色透明溶液,后一步用离子方程式表示为_______ ;再加入乙醇,得到的深蓝色晶体为_______ 。
(2)[Cu(H2O)4]2+中存在的化学键类型有_______ 。[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______ 。其结构可用示意图表示为_______
(3)科学家通过X射线测得胆矾结构示意图可简单表示如图:
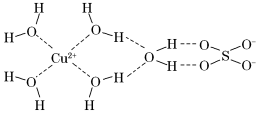
图中虚线表示的作用力为_______ 。
(4)Cu2O为红色粉末,熔点为1235℃;Cu2S呈黑色,熔点为1130℃。Cu2O的晶体类型是_______ ,熔点Cu2O>Cu2S的原因是_______ 。
(5) CuCl2和CuCl是铜的两种常见的氯化物。
①图表示的是_______ (填“CuCl2”或“CuCl”)的晶胞。

②原子坐标参数,表示晶胞内部各原子的相对位置,图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为_______ 。

(1)往硫酸铜溶液中加入氨水,先形成蓝色沉淀,继续加氨水,得到深蓝色透明溶液,后一步用离子方程式表示为
(2)[Cu(H2O)4]2+中存在的化学键类型有
(3)科学家通过X射线测得胆矾结构示意图可简单表示如图:

图中虚线表示的作用力为
(4)Cu2O为红色粉末,熔点为1235℃;Cu2S呈黑色,熔点为1130℃。Cu2O的晶体类型是
(5) CuCl2和CuCl是铜的两种常见的氯化物。
①图表示的是


②原子坐标参数,表示晶胞内部各原子的相对位置,图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】2021年7月4日,“神舟十二号”航天员圆满完成出舱任务。“神舟十二号”制作材料中包含了 、
、 、
、 、
、 等多种元素。回答下列问题:
等多种元素。回答下列问题:
(1) 元素基态原子的外围电子排布式为
元素基态原子的外围电子排布式为___________ , 、
、 、
、 三种元素的第一电离能由大到小的顺序为
三种元素的第一电离能由大到小的顺序为___________ 。
(2) 位于元素周期表的
位于元素周期表的___________ (填“ ”、“
”、“ ”、“
”、“ ”或“
”或“ ”)区,
”)区, 催化烯烃硝化反应过程中会产生
催化烯烃硝化反应过程中会产生 。键角:
。键角:
___________  (填“<”或“>”),判断依据是
(填“<”或“>”),判断依据是___________ 。
(3)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。 的一种螯合物结构如图1所示,
的一种螯合物结构如图1所示, 该配合物中通过鳌合作用形成的配位键有
该配合物中通过鳌合作用形成的配位键有___________ 个,该螯合物中 的杂化方式为
的杂化方式为___________ 。
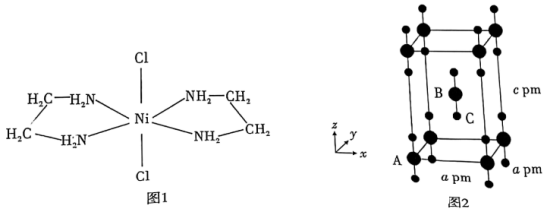
(4) 晶体属四方晶系,晶胞结构如图2所示,晶胞棱边夹角均为90°。以晶胞棱边为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如
晶体属四方晶系,晶胞结构如图2所示,晶胞棱边夹角均为90°。以晶胞棱边为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如 点原子的分数坐标为
点原子的分数坐标为 ,
, 点原子的分数坐标为
点原子的分数坐标为 。已知
。已知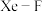 键长为
键长为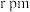 ,则
,则 点原子的分数坐标为
点原子的分数坐标为___________ ;设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 的密度为
的密度为___________  (列计算式)。
(列计算式)。
 、
、 、
、 、
、 等多种元素。回答下列问题:
等多种元素。回答下列问题:(1)
 元素基态原子的外围电子排布式为
元素基态原子的外围电子排布式为 、
、 、
、 三种元素的第一电离能由大到小的顺序为
三种元素的第一电离能由大到小的顺序为(2)
 位于元素周期表的
位于元素周期表的 ”、“
”、“ ”、“
”、“ ”或“
”或“ ”)区,
”)区, 催化烯烃硝化反应过程中会产生
催化烯烃硝化反应过程中会产生 。键角:
。键角:
 (填“<”或“>”),判断依据是
(填“<”或“>”),判断依据是(3)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。
 的一种螯合物结构如图1所示,
的一种螯合物结构如图1所示, 该配合物中通过鳌合作用形成的配位键有
该配合物中通过鳌合作用形成的配位键有 的杂化方式为
的杂化方式为
(4)
 晶体属四方晶系,晶胞结构如图2所示,晶胞棱边夹角均为90°。以晶胞棱边为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如
晶体属四方晶系,晶胞结构如图2所示,晶胞棱边夹角均为90°。以晶胞棱边为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如 点原子的分数坐标为
点原子的分数坐标为 ,
, 点原子的分数坐标为
点原子的分数坐标为 。已知
。已知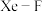 键长为
键长为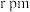 ,则
,则 点原子的分数坐标为
点原子的分数坐标为 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 的密度为
的密度为 (列计算式)。
(列计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】 、
、 是新型磁性材料的成分,设
是新型磁性材料的成分,设 为阿伏加德罗常数的值,依据其中有关元素回答问题:
为阿伏加德罗常数的值,依据其中有关元素回答问题:
(1)钕(Nd)属于镧系元素,则其在元素周期表中处于___________ 区, 的价电子排布图为
的价电子排布图为___________ 。
(2) 的立体构型为
的立体构型为___________ ;F原子核外有___________ 种不同空间运动状态的电子。
(3) 是一种还原剂,B原子的杂化方式为
是一种还原剂,B原子的杂化方式为___________ 。该物质中是否存在配位键___________ (填“是”或“否”)。
(4) 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。___________ 。
②该晶体密度为 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为___________ pm。
(5) 的制备:称取研细的
的制备:称取研细的 和
和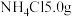 于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的
于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该反应的离子方程式
溶液。写出该反应的离子方程式___________ 。若上述实验过程中得到 ,则其中所含的
,则其中所含的 键数目为
键数目为___________ 。
(6)已知某温度下 的电离平衡常数:
的电离平衡常数: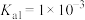 、
、 ,
,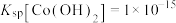 、
、 。写出该温度时向
。写出该温度时向 碳酸钠溶液中逐滴加入
碳酸钠溶液中逐滴加入 溶液,生成沉淀的离子方程式:
溶液,生成沉淀的离子方程式:___________ 。
 、
、 是新型磁性材料的成分,设
是新型磁性材料的成分,设 为阿伏加德罗常数的值,依据其中有关元素回答问题:
为阿伏加德罗常数的值,依据其中有关元素回答问题:(1)钕(Nd)属于镧系元素,则其在元素周期表中处于
 的价电子排布图为
的价电子排布图为(2)
 的立体构型为
的立体构型为(3)
 是一种还原剂,B原子的杂化方式为
是一种还原剂,B原子的杂化方式为(4)
 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。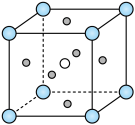
②该晶体密度为
 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为(5)
 的制备:称取研细的
的制备:称取研细的 和
和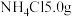 于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的
于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该反应的离子方程式
溶液。写出该反应的离子方程式 ,则其中所含的
,则其中所含的 键数目为
键数目为(6)已知某温度下
 的电离平衡常数:
的电离平衡常数: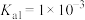 、
、 ,
,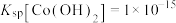 、
、 。写出该温度时向
。写出该温度时向 碳酸钠溶液中逐滴加入
碳酸钠溶液中逐滴加入 溶液,生成沉淀的离子方程式:
溶液,生成沉淀的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】2022年4月16日9时56分,“神舟十三号”载人飞船返回舱成功着陆。“神舟十三号”制作材料中包含了Cu、Ga、Ni、Xe等多种元素。回答下列问题:
(1)原子中的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 之表示,称为电子的自旋磁量子数。对于基态的Ga原子,其价电子自旋磁量子数的代数和为
之表示,称为电子的自旋磁量子数。对于基态的Ga原子,其价电子自旋磁量子数的代数和为___________ 。 Ca、Ga、Ge 三种元素的电负性由大到小的顺序为______ 。
(2)Cu位于元素周期表的___________ (填 “s”、“p”、 “d”或“ds”)区,Cu催化烯烃硝化反应过程中会产生 ,键角:
,键角:
___________  (填“> ”或“<"),判断依据是
(填“> ”或“<"),判断依据是______ 。
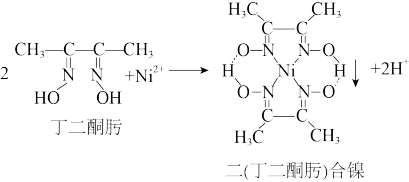
(3)N2+与丁二酮肟生成鲜红色二(丁二酮肟)合镍沉淀,该反应可用于检验Ni2+,原理如图,则丁二酮肟中碳原子的杂化轨道类型为___________ ,1 mol丁二酮肟分子中含有σ键的数目为___________ ,二 (丁二酮肟)合镍分子中存在的化学键有___________ (填字母序号)。
a.非极性键 b.π键 c.离子键 d.氢键 e.配位键
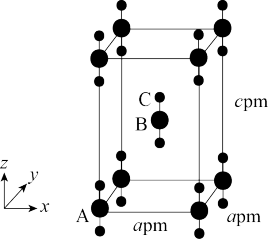
(4)XeF2晶体属四方晶系,晶胞结构如图所示,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。如图中原子A的分数坐标为(0,0,0),原子B的分数坐标为( ,
, ,
, )。已知Xe-F键长为rpm,原子C的分数坐标为
)。已知Xe-F键长为rpm,原子C的分数坐标为___________ ;设NA为阿伏加德罗常数的值,XeF2的密度为___________ g·cm-3(列计算式)。
(1)原子中的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 之表示,称为电子的自旋磁量子数。对于基态的Ga原子,其价电子自旋磁量子数的代数和为
之表示,称为电子的自旋磁量子数。对于基态的Ga原子,其价电子自旋磁量子数的代数和为(2)Cu位于元素周期表的
 ,键角:
,键角:
 (填“> ”或“<"),判断依据是
(填“> ”或“<"),判断依据是(3)N2+与丁二酮肟生成鲜红色二(丁二酮肟)合镍沉淀,该反应可用于检验Ni2+,原理如图,则丁二酮肟中碳原子的杂化轨道类型为
a.非极性键 b.π键 c.离子键 d.氢键 e.配位键

(4)XeF2晶体属四方晶系,晶胞结构如图所示,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。如图中原子A的分数坐标为(0,0,0),原子B的分数坐标为(
 ,
, ,
, )。已知Xe-F键长为rpm,原子C的分数坐标为
)。已知Xe-F键长为rpm,原子C的分数坐标为
您最近一年使用:0次



