在2L绝热密闭容器中投入2molSO2和bmolO2,下图是部分反应物随时间的变化曲线。
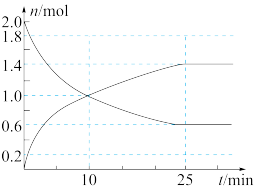
①10 min时,v(SO3)=________ 。
②反应达到平衡时,SO2的转化率为______________ 。
③下列情况能说明该反应达到化学平衡的是______________ 。
A.v(SO3)=v(SO2) B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变 D.混合气体的总物质的量不再改变

①10 min时,v(SO3)=
②反应达到平衡时,SO2的转化率为
③下列情况能说明该反应达到化学平衡的是
A.v(SO3)=v(SO2) B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变 D.混合气体的总物质的量不再改变
更新时间:2020-08-02 11:23:57
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】化学反应中既存在物质变化,又存在能量变化。
Ⅰ.氢气是未来非常理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O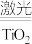 2H2+O2.制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2.制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
(1)分解海水时,_______ 能转变为_______ 能。生成的氢气用于燃料电池时,_______ 能转变为_______ 能。
(2)合成氨还需要大量的氮气为原料,工业上获得大量氮气的方法是_______ 。
Ⅱ.2SO2(g)+O2(g) ⇌2SO3(g),是工业制硫酸的主要反应之一
(3)若O2中的氧原子使用18O 进行标记,则反应一段时间后,18O存在于_______ 中。
A.O2 B.SO2 C.SO3
(4)某条件下,在2 L绝热密闭容器中投入2 mol SO2和b mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。

①10 min时,v(SO3)=_______ 。
②反应达到平衡时,SO2的转化率为_______ 。
③b的取值范围是_______ 。
④下列情况能说明该反应达到化学平衡状态的是_______ (填字母)。
A.v(SO3)=v(SO2) B.混合气体的密度保持不变
C.体系的温度不再发生改变 D.混合气体的总物质的量不再改变
Ⅰ.氢气是未来非常理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O
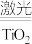 2H2+O2.制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2.制得的氢气可用于燃料电池、合成氨工业。回答下列问题:(1)分解海水时,
(2)合成氨还需要大量的氮气为原料,工业上获得大量氮气的方法是
Ⅱ.2SO2(g)+O2(g) ⇌2SO3(g),是工业制硫酸的主要反应之一
(3)若O2中的氧原子使用18O 进行标记,则反应一段时间后,18O存在于
A.O2 B.SO2 C.SO3
(4)某条件下,在2 L绝热密闭容器中投入2 mol SO2和b mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。

①10 min时,v(SO3)=
②反应达到平衡时,SO2的转化率为
③b的取值范围是
④下列情况能说明该反应达到化学平衡状态的是
A.v(SO3)=v(SO2) B.混合气体的密度保持不变
C.体系的温度不再发生改变 D.混合气体的总物质的量不再改变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在2 L密闭容器中,800 ℃时,反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表所示。
2NO2(g)体系中,n(NO)随时间的变化如下表所示。
___________ v逆(填“大于”“小于”或“等于”)。
(2)图中表示NO2变化的曲线是___________ 。用O2表示从0~2 s内该反应的平均速率v=___________ 。
(3)下列能说明该反应已经达到平衡状态的是___________ (填字母,下同)。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
(4)下列能使该反应的反应速率增大的是___________ 。
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效的催化剂
 2NO2(g)体系中,n(NO)随时间的变化如下表所示。
2NO2(g)体系中,n(NO)随时间的变化如下表所示。| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
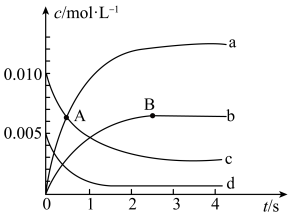
(2)图中表示NO2变化的曲线是
(3)下列能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
(4)下列能使该反应的反应速率增大的是
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效的催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO 2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:
2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2 s内的平均反应速率v(N2)=___________ 。
(2)达到平衡时NO的转化率为___________ 。
(3)若上述反应在密闭恒容容器中进行,判断该反应达到平衡的依据为___________(填字母)。
 2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:
2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L−1 | 1.00×10−3 | 4.50×10−4 | 2.50×10−4 | 1.50×10−4 | 1.00×10−4 | 1.00×10−4 |
| c(CO)/mol·L−1 | 3.60×10−3 | 3.05×10−3 | 2.85×10−3 | 2.75×10−3 | 2.70×10−3 | 2.70×10−3 |
(1)前2 s内的平均反应速率v(N2)=
(2)达到平衡时NO的转化率为
(3)若上述反应在密闭恒容容器中进行,判断该反应达到平衡的依据为___________(填字母)。
| A.c(N2)不随时间改变 | B.气体的密度不随时间改变 |
| C.压强不随时间改变 | D.单位时间内消耗2 mol NO的同时生成1 mol N2 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】中国首次实现了利用二氧化碳人工合成淀粉,为全球的“碳达峰”、“碳中和”起到重大的支撑作用。其中最关键的一步是以 为原料制
为原料制 。在某
。在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:
Ⅰ.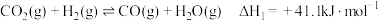
Ⅱ.

Ⅲ.
(1)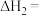
___________  。
。
(2) 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比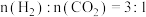 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
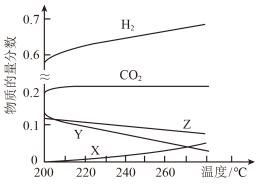
图中Y代表___________ (填化学式)。
(3)我国科研人员研究出在 催化剂上
催化剂上 氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为___________ 。分析在反应气中加入少量的水能够提升甲醇产率的可能原因是___________ 。

(4)恒压下, 和
和 以物质的量之比
以物质的量之比 投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。___________

 为原料制
为原料制 。在某
。在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:Ⅰ.
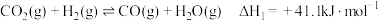
Ⅱ.


Ⅲ.

(1)
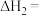
 。
。(2)
 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比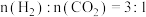 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
图中Y代表
(3)我国科研人员研究出在
 催化剂上
催化剂上 氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
(4)恒压下,
 和
和 以物质的量之比
以物质的量之比 投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某化学科研小组研究在其他条件不变时,改变某一条件对某类反应[aA(g)+bB(g)⇌cC(g)]的化学平衡的影响,得到图像(图中p表示压强,T表示温度,n表示物质的量,α表示转化率)
反应Ⅰ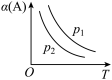 反应Ⅱ
反应Ⅱ
分析图像象,回答下列问题:
(1)在反应I中,若 >
> ,则该反应的正反应为
,则该反应的正反应为__________ (填“放热”或“吸热”)反应,且为气体分子数__________ (填“减小”或“增大”)的反应;若此反应能自发进行,则必须满足的条件是__________
(2)在反应Ⅱ中,
__________ (填“>”,“<”或“=”) ,该反应的正反应为
,该反应的正反应为__________ (填“放热”或“吸热”)反应。
反应Ⅰ
 反应Ⅱ
反应Ⅱ
分析图像象,回答下列问题:
(1)在反应I中,若
 >
> ,则该反应的正反应为
,则该反应的正反应为(2)在反应Ⅱ中,

 ,该反应的正反应为
,该反应的正反应为
您最近一年使用:0次
【推荐3】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
①A、B两点对应的压强大小关系是PA_______ PB(填“>、<、=”)。
②在压强为P2时B、C两点的正反应速率大小关系是______________
③下列叙述能说明上述反应已达到化学平衡状态的是__________
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1℃时,H2的平衡转化率为__________ (计算出结果),再加入1.0 mol CO后重新到达平衡,则CO的转化率___________ (填“增大”、“不变”或“减小”)。
(3) 在压强为P1、温度为T1℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)________ v(逆)(填“>”、“<”或“=”)。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。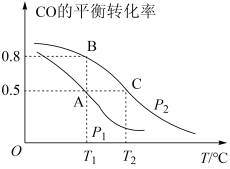
①A、B两点对应的压强大小关系是PA
②在压强为P2时B、C两点的正反应速率大小关系是
③下列叙述能说明上述反应已达到化学平衡状态的是
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1℃时,H2的平衡转化率为
(3) 在压强为P1、温度为T1℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
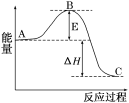
【推荐1】2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ/mol.
2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ/mol.
请回答下列问题:
(1)图中A、C分别表示___ 、___ ,E的大小对该反应的反应热有无影响?____ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?___ ,理由是____ 。
(2)图中ΔH=___ kJ/mol.
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:____ 。
(4)如果反应速率v(SO2)为0.05mol/(L·min),则v(O2)=___ mol/(L·min)、v(SO3)=____ mol/(L·min)。
(5)已知单质硫的燃烧热为296kJ/mol,计算由S(s)生成3molSO3(g)的ΔH(要求计算过程)。____
 2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ/mol.
2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ/mol.
请回答下列问题:
(1)图中A、C分别表示
(2)图中ΔH=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
(4)如果反应速率v(SO2)为0.05mol/(L·min),则v(O2)=
(5)已知单质硫的燃烧热为296kJ/mol,计算由S(s)生成3molSO3(g)的ΔH(要求计算过程)。
您最近一年使用:0次
【推荐2】2SO2(g)+O2(g) 2SO3(g)反应过程中能量的变化如图所示。已知1 mol SO2(g)与0.5 mol O2(g)反应生成1 mol SO3(g)的ΔH=-99 kJ·mol-1。
2SO3(g)反应过程中能量的变化如图所示。已知1 mol SO2(g)与0.5 mol O2(g)反应生成1 mol SO3(g)的ΔH=-99 kJ·mol-1。

请回答下列问题:
(1)图中A点、C点的数值分别表示________ 、______ ,E的大小对该反应的反应热________ (填“有”或“无”)影响。
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点________ (填“升高”或“降低”),理由是____ 。
(3)图中ΔH=________ kJ·mol-1。
 2SO3(g)反应过程中能量的变化如图所示。已知1 mol SO2(g)与0.5 mol O2(g)反应生成1 mol SO3(g)的ΔH=-99 kJ·mol-1。
2SO3(g)反应过程中能量的变化如图所示。已知1 mol SO2(g)与0.5 mol O2(g)反应生成1 mol SO3(g)的ΔH=-99 kJ·mol-1。
请回答下列问题:
(1)图中A点、C点的数值分别表示
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点
(3)图中ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】一密封体系中发生反应:N2+3H2 2NH3 ΔH<0,
2NH3 ΔH<0,
①以下图1、图2均表示该反应在t1时达到平衡,在t2时改变某条件发生变化的曲线。

试判断,图1中t2时改变的条件是______________ ;图2中t2时改变的条件是______________ 。
②下图是某一时间段中反应速率与反应进程的曲线关系图:
下列各时间段时,氨的百分含量最高的是__________ 。

A.t0~t1B.t2~t3C.t3~t4D.t5~t6
③工业生产中提高合成氨反应的反应速率和产率的具体措施是:_______________________________________________________
A.降低温度 B. 增大压强 C. 降低压强
D. 循环利用和不断补充氮气 E. 及时移出氨气
 2NH3 ΔH<0,
2NH3 ΔH<0,①以下图1、图2均表示该反应在t1时达到平衡,在t2时改变某条件发生变化的曲线。

试判断,图1中t2时改变的条件是
②下图是某一时间段中反应速率与反应进程的曲线关系图:
下列各时间段时,氨的百分含量最高的是

A.t0~t1B.t2~t3C.t3~t4D.t5~t6
③工业生产中提高合成氨反应的反应速率和产率的具体措施是:
A.降低温度 B. 增大压强 C. 降低压强
D. 循环利用和不断补充氮气 E. 及时移出氨气
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
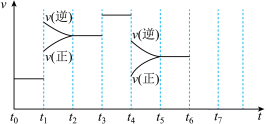
【推荐1】在一密闭容器中发生反应N2+3H2=2NH3 ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
回答下列问题:
(1)处于平衡状态的时间段是___________ (填字母,下同)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻___________ ;t3时刻___________ ;t4时刻___________ 。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是___________ 。
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线______ 。

回答下列问题:
(1)处于平衡状态的时间段是
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线
您最近一年使用:0次
【推荐2】可逆反应在某体积为5L的密闭容器中进行,在从0﹣3分钟各物质的量的变化情况如图所示(A,B,C均为气体)
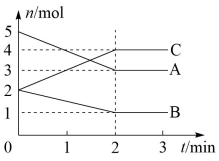
(1)该反应的化学方程式为______________ ;
(2)从开始至2 min,C的平均反应速率为__________ ;
(3)2 min时,A的转化率为________ ;
(4)1~2min和2~3min这两个时间段中,反应限度最大的时间段为___________ ;
(5)1min时,v(正)_______ v(逆),2 min时,v(正)_______ v(逆) (填“>或“<”或“=”);
(6)恒温恒容下,N2(g)+3H2(g) 2NH3(g),达到平衡的标志有
2NH3(g),达到平衡的标志有_______________ 。
A.3v正(H2)=2v逆(NH3) B.混合气体总质量不在随时间变化 C.容器内的压强不再随时间而变化 D.N2、H2、NH3的浓度之比为1:2:3 E.单位时间生成nmolN2,同时消耗3nmolH2 F.断开一个N≡N键的同时有6个N—H键生成

(1)该反应的化学方程式为
(2)从开始至2 min,C的平均反应速率为
(3)2 min时,A的转化率为
(4)1~2min和2~3min这两个时间段中,反应限度最大的时间段为
(5)1min时,v(正)
(6)恒温恒容下,N2(g)+3H2(g)
 2NH3(g),达到平衡的标志有
2NH3(g),达到平衡的标志有A.3v正(H2)=2v逆(NH3) B.混合气体总质量不在随时间变化 C.容器内的压强不再随时间而变化 D.N2、H2、NH3的浓度之比为1:2:3 E.单位时间生成nmolN2,同时消耗3nmolH2 F.断开一个N≡N键的同时有6个N—H键生成
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
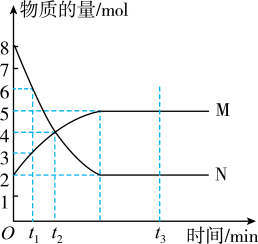
(1)此反应的化学方程式中a/b=___________ ;
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为_________________ ;
(3) N的平衡转化率为_______________ ;
(4)下列叙述中能说明上述反应达到平衡状态的是___________ (填字母)。
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:
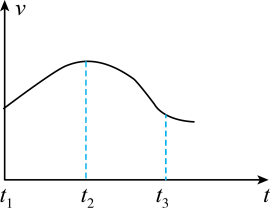
实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是_______ ,t2~t3速率变化的主要原因是______ 。
(2)实验②放出氢气的量减少的原因是___________________ (用离子方程式表示)。
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a或b作答。a.若不正确,请说明原因_____________________________________ 。b.若正确,则写出实验③中原电池的正极电极反应式_______________________ 。
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中a/b=
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3) N的平衡转化率为
(4)下列叙述中能说明上述反应达到平衡状态的是
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:

实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是
(2)实验②放出氢气的量减少的原因是
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a或b作答。a.若不正确,请说明原因
您最近一年使用:0次



