电化学在我们的生产生活中占有越来越重要的地位。
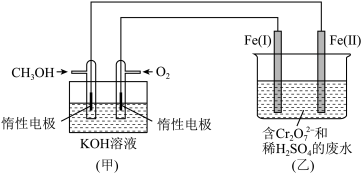
(1)燃料电池是一种绿色环保、高效的化学电源。则上图甲池中负极反应式为________ 。
(2)用甲醇燃料电池电解2L,1mol/L硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体89.6L,则电路中共转移_________ mol电子。
(3)利用电化学原理,模拟工业电解法来处理含 废水,如上图所示。
废水,如上图所示。
①阳极的电极反应式为______________ 。
②电解过程中溶液中发生的反应离子方程式为______________ 。
③向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Kgp=c(Cr3+).c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Kgp=c(Cr3+).c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至______________ 。

(1)燃料电池是一种绿色环保、高效的化学电源。则上图甲池中负极反应式为
(2)用甲醇燃料电池电解2L,1mol/L硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体89.6L,则电路中共转移
(3)利用电化学原理,模拟工业电解法来处理含
 废水,如上图所示。
废水,如上图所示。①阳极的电极反应式为
②电解过程中溶液中发生的反应离子方程式为
③向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s)
 Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Kgp=c(Cr3+).c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Kgp=c(Cr3+).c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
更新时间:2020-08-06 17:20:50
|
相似题推荐
【推荐1】硫单质及其化合物在工农业生产中有着吸要的应用.
(l)已知:2SO2(g)+O2═2SO3(g)△H=-196.6kJ•mol-1,2NO(g)+O2═2NO2(g)△H=-113.0kJ•mol-1.则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H= _________;
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料.已知As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O.当生成H3AsO4的物质的量为0.6mol,反应中转移电子的数目为_________。
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS-、S2-的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出),滴加过程中,溶液中微位浓度大小关系正确的是_________ (填字母)。

A.c(Na+)=c(H2S)+c(HS-)+2c(S2-)
B.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
C.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
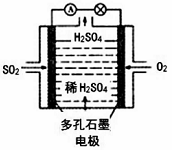
(4)某学习小组以SO2为原料,采用电化学方法制取硫酸。该小组设计的原电池原理如图2所示.写出该电池负极的电极反应式_________;
(5)难溶物ZnS遇CuSO4认溶液会慢慢转化为铜蓝(CuS)。若转化后溶液中c(Zn2+)=3.0×10-2mol•L-1,则c(Cu2+)=" _________" mol•L-1〔已知Ksp(CuS)=1.0×10-36,Ksp(ZnS)=1.0×10-24
(l)已知:2SO2(g)+O2═2SO3(g)△H=-196.6kJ•mol-1,2NO(g)+O2═2NO2(g)△H=-113.0kJ•mol-1.则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H= _________;
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料.已知As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O.当生成H3AsO4的物质的量为0.6mol,反应中转移电子的数目为_________。
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS-、S2-的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出),滴加过程中,溶液中微位浓度大小关系正确的是_________ (填字母)。

A.c(Na+)=c(H2S)+c(HS-)+2c(S2-)
B.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
C.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
(4)某学习小组以SO2为原料,采用电化学方法制取硫酸。该小组设计的原电池原理如图2所示.写出该电池负极的电极反应式_________;

(5)难溶物ZnS遇CuSO4认溶液会慢慢转化为铜蓝(CuS)。若转化后溶液中c(Zn2+)=3.0×10-2mol•L-1,则c(Cu2+)=" _________" mol•L-1〔已知Ksp(CuS)=1.0×10-36,Ksp(ZnS)=1.0×10-24
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图。已知:
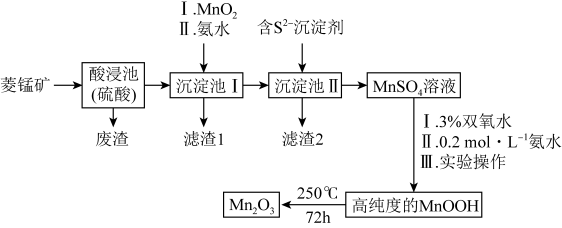
①25℃时相关物质的Ksp见下表。
②氢氧化氧锰(MnOOH)难溶于水和碱性溶液;“沉淀池I”的条件下,Co2+不能被二氧化锰氧化。
(1)Mn元素位于元素周期表第_______ 周期第_______ 族。
(2)向“沉淀池I”中加入MnO2,MnO2的作用是_______ ;“滤渣2”的主要成分是_______ (填化学式)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“III.实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为_______ 。
(5)高纯度的MnOOH转化为Mn2O3的化学方程式为_______ 。
(6)在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为_______ (当溶液中某离子浓度c≤1.0×10-5mol·L-1时,可认为该离子沉淀完全)。

①25℃时相关物质的Ksp见下表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)Mn元素位于元素周期表第
(2)向“沉淀池I”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“III.实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
(5)高纯度的MnOOH转化为Mn2O3的化学方程式为
(6)在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】从钒铬锰矿渣(主要成分为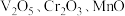 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下:
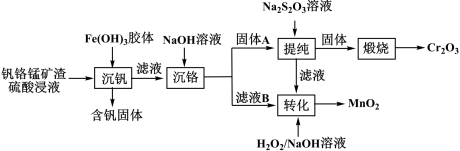
已知: 较大时,二价锰
较大时,二价锰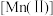 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:
(1) 元素在周期表中的位置是
元素在周期表中的位置是___________ 。
(2)常温下,各种形态五价钒粒子总浓度的对数 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中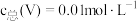 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为___________ (填化学式)。
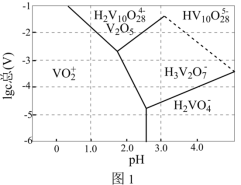
(3)某温度下,Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与pH关系如图2,“沉铬”过程最佳pH为_____ (填标号);
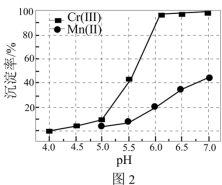
a.4.0 b.5.0 c.6.0
在该条件下滤液B中
______  [
[ 近似为
近似为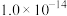 ,
, 的
的 近似为
近似为 ]。
]。
(4)“转化”过程中生成 的离子方程式为
的离子方程式为_________ 。
(5)“提纯”过程中 的作用为
的作用为________ 。
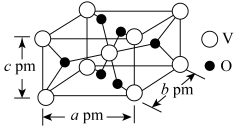
(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为_______ g•cm-3 (列出计算式即可)。
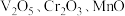 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下:
已知:
 较大时,二价锰
较大时,二价锰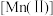 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:(1)
 元素在周期表中的位置是
元素在周期表中的位置是(2)常温下,各种形态五价钒粒子总浓度的对数
 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中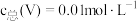 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为
(3)某温度下,Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与pH关系如图2,“沉铬”过程最佳pH为

a.4.0 b.5.0 c.6.0
在该条件下滤液B中

 [
[ 近似为
近似为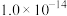 ,
, 的
的 近似为
近似为 ]。
]。(4)“转化”过程中生成
 的离子方程式为
的离子方程式为(5)“提纯”过程中
 的作用为
的作用为(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为

您最近一年使用:0次
【推荐1】中科院一项新研究成果实现了甲烷高效生产乙烯,其反应为:2CH4(g)⇌C2H4(g)+2H2(g) ΔH>0
(1)已知相关物质的燃烧热如表,完成热化学方程式:2CH4(g)⇌C2H4(g)+2H2(g) ΔH=__ 。
(2)温度为T1℃时,向1 L的恒容反应器中充入2 mol CH4,仅发生上述反应,反应0~15 min CH4的物质的量随时间变化如图1,实验测得10~15 min时H2的浓度为1.6 mol/L。
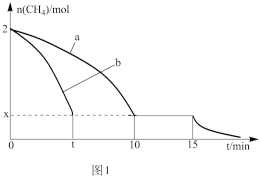
①若图1中曲线a、b分别表示在T1℃时,使用等质量的两种不同的催化剂时,达到平衡过程中n(CH4)变化曲线,判断:催化剂a_____ b(填“优于”或“劣于”)。
②在15 min时改变反应条件,导致n(CH4)发生变化(见图1),则改变的条件可能是:_____ (任答一条即可)。
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),其中k正、k逆为速率常数仅与温度有关,温度为 时,k正与k逆的比值为
时,k正与k逆的比值为______ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数v正_______ v逆(填“>”、“=”或“<”),判断的理由是_________ 。
(4)科研人员设计了甲烷燃料电池并用于电解(如图2)。电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。
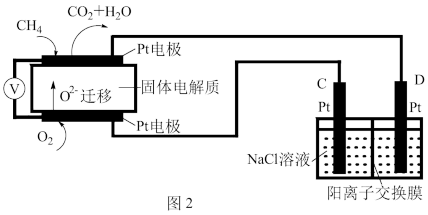
①图中C处的Pt为_______ (填“阴”或“阳”)极。
②该电池工作时负极的电极反应式为________ 。
③用该电池电解饱和食盐水,一段时间后收集到标准状况下气体总体积为112 mL,则阴极区所得溶液在25℃时pH=_______ (假设电解前后NaCl溶液的体积均为500 mL)。
| 物质 | 燃烧热(kJ/mol) |
| 氢气 | 285.8 |
| 甲烷 | 890.3 |
| 乙烯 | 1411.5 |
(1)已知相关物质的燃烧热如表,完成热化学方程式:2CH4(g)⇌C2H4(g)+2H2(g) ΔH=
(2)温度为T1℃时,向1 L的恒容反应器中充入2 mol CH4,仅发生上述反应,反应0~15 min CH4的物质的量随时间变化如图1,实验测得10~15 min时H2的浓度为1.6 mol/L。

①若图1中曲线a、b分别表示在T1℃时,使用等质量的两种不同的催化剂时,达到平衡过程中n(CH4)变化曲线,判断:催化剂a
②在15 min时改变反应条件,导致n(CH4)发生变化(见图1),则改变的条件可能是:
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),其中k正、k逆为速率常数仅与温度有关,温度为
 时,k正与k逆的比值为
时,k正与k逆的比值为(4)科研人员设计了甲烷燃料电池并用于电解(如图2)。电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。

①图中C处的Pt为
②该电池工作时负极的电极反应式为
③用该电池电解饱和食盐水,一段时间后收集到标准状况下气体总体积为112 mL,则阴极区所得溶液在25℃时pH=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】Ⅰ.天然气开采过程会产生大量含硫废水(硫元素的主要存在形式为H2S),可采用Na2SO3氧化法对其进行处理。
(1)下列事实中,能够比较氢硫酸与亚硫酸的酸性强弱的是___________(填标号)。
Ⅱ.已知:氧化还原反应可拆分为氧化、还原两个半反应,电极电势分别表示为 和
和 ,电势差
,电势差 。如
。如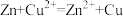 的
的 。两组电对的电势差越大,反应的自发程度越大。
。两组电对的电势差越大,反应的自发程度越大。
(2)各电对的电极电势与产物浓度的关系如图所示,将体系中自发程度最大的反应记为ⅰ,反应ⅰ的离子方程式为___________ 。
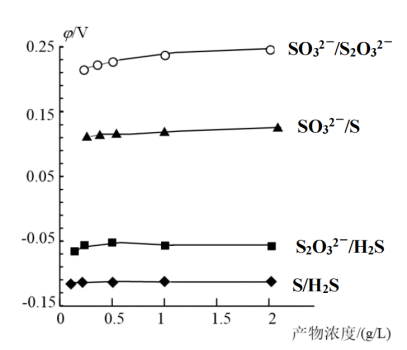
各微粒的相对能量如下表:
已知反应ⅰ为放热反应,当有 发生反应ⅰ时,释放的能量为
发生反应ⅰ时,释放的能量为___________ kJ。(用含字母的代数式表示)
(3)25℃时,向浓度为0.68g/L的H2S溶液中加入一定量Na2SO3固体,在不同pH下的H2S去除率随时间变化如图所示。

①实际生产中采取 的去除条件,而不选择更低pH的原因为
的去除条件,而不选择更低pH的原因为___________ 。
② 时,前
时,前 的去除速率
的去除速率
___________  ;实际生产中反应时间选择
;实际生产中反应时间选择 而不是更长,其原因为
而不是更长,其原因为___________ 。
III.硫化氢—空气质子交换膜燃料电池实现了发电、环保的有效结合,已知:
 。
。
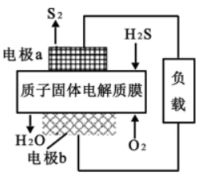
(4)电极b上发生的电极反应为:___________ 。
(5)标准状况下,每11.2 L H2S参与反应,有___________ mol H+ 经固体电解质膜进入正极区。
(1)下列事实中,能够比较氢硫酸与亚硫酸的酸性强弱的是___________(填标号)。
| A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| B.氢硫酸的导电能力低于亚硫酸 |
| C.常温下,0.10mol/L的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| D.氢硫酸的还原性强于亚硫酸 |
Ⅱ.已知:氧化还原反应可拆分为氧化、还原两个半反应,电极电势分别表示为
 和
和 ,电势差
,电势差 。如
。如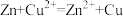 的
的 。两组电对的电势差越大,反应的自发程度越大。
。两组电对的电势差越大,反应的自发程度越大。(2)各电对的电极电势与产物浓度的关系如图所示,将体系中自发程度最大的反应记为ⅰ,反应ⅰ的离子方程式为

各微粒的相对能量如下表:
 |  | S(s) |  |  | 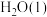 | |
| 相对能量/kJ/mol | a | b | 0 | c | d | e |
 发生反应ⅰ时,释放的能量为
发生反应ⅰ时,释放的能量为(3)25℃时,向浓度为0.68g/L的H2S溶液中加入一定量Na2SO3固体,在不同pH下的H2S去除率随时间变化如图所示。

①实际生产中采取
 的去除条件,而不选择更低pH的原因为
的去除条件,而不选择更低pH的原因为②
 时,前
时,前 的去除速率
的去除速率
 ;实际生产中反应时间选择
;实际生产中反应时间选择 而不是更长,其原因为
而不是更长,其原因为III.硫化氢—空气质子交换膜燃料电池实现了发电、环保的有效结合,已知:

 。
。
(4)电极b上发生的电极反应为:
(5)标准状况下,每11.2 L H2S参与反应,有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】(1)合成氨反应的热化学方程式:N2(g)+3H2(g)=2NH3(g)ΔH=-92.2 kJ·mol-1
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2 kJ的热量,则在反应混合物中要投放N2的物质的量的取值范围为________ mol。
(2)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:负极的电极反应式:__________ ,正极的电极反应式:__________ 。
(3)如图是一个电解过程示意图。
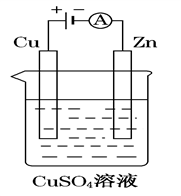
①锌片上发生的电极反应式是:_______________
②假设使用肼-空气燃料电池作为该过程中的电源,锌片质量变化为64 g,则肼-空气燃料电池理论上消耗标准状况下的空气__________ L(假设空气中氧气体积分数为20%)。
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2 kJ的热量,则在反应混合物中要投放N2的物质的量的取值范围为
(2)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:负极的电极反应式:
(3)如图是一个电解过程示意图。

①锌片上发生的电极反应式是:
②假设使用肼-空气燃料电池作为该过程中的电源,锌片质量变化为64 g,则肼-空气燃料电池理论上消耗标准状况下的空气
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】甲醇是一种重要的化工原料,工业上可用CO和H2合成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)  CH3OH(g) ΔH = -90.8 kJ·mol-1
CH3OH(g) ΔH = -90.8 kJ·mol-1
(1)某研究小组,在温度和容器的容积保持不变时,研究该反应是否达到平衡状态,以下五位同学对平衡状态的描述正确的是__________ 。
A.甲:H2的消耗速率等于CH3OH的生成速率
B.乙:容器内的压强保持不变
C.丙:容器内气体的密度保持不变
D.丁:容器中气体的平均摩尔质量保持不变
(2)若在一定温度下、容积为2L的密闭容器中,投入2 mol CO、4 mol H2,保持恒温、恒容,测得反应达到平衡时H2转化率为75%,求平衡时CH3OH的浓度=__________ mol/L
(3)已知在298K、101kPa下:甲醇的燃烧热化学方程式为:
CH3OH(l)+ 3/2 O2(g)= CO2(g)+ 2H2O(l) ΔH= -725.8 kJ·mol-1;
CO的燃烧热化学方程式为:CO(g)+ 1/2 O2(g)= CO2(g) ΔH= -283 kJ·mol-1;
H2O (g) === H2O(l) ΔH= -44 kJ·mol-1
请写出甲醇不完全燃烧生成一氧化碳和水蒸气的热化学方程式__________ 。
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)
①该电池中通入甲醇的是电源的__________ (填正、负)极,若KOH溶液足量,则写出电池总反应的离子方程式__________ 。
②若电解质溶液中KOH的物质的量为0.5mol,当有0.5mol甲醇参与反应时,产物恰好为KHCO3时,该电池的负极反应式为__________ ,所得溶液中各种离子的物质的量浓度由大到小的顺序是__________ 。
 CH3OH(g) ΔH = -90.8 kJ·mol-1
CH3OH(g) ΔH = -90.8 kJ·mol-1(1)某研究小组,在温度和容器的容积保持不变时,研究该反应是否达到平衡状态,以下五位同学对平衡状态的描述正确的是
A.甲:H2的消耗速率等于CH3OH的生成速率
B.乙:容器内的压强保持不变
C.丙:容器内气体的密度保持不变
D.丁:容器中气体的平均摩尔质量保持不变
(2)若在一定温度下、容积为2L的密闭容器中,投入2 mol CO、4 mol H2,保持恒温、恒容,测得反应达到平衡时H2转化率为75%,求平衡时CH3OH的浓度=
(3)已知在298K、101kPa下:甲醇的燃烧热化学方程式为:
CH3OH(l)+ 3/2 O2(g)= CO2(g)+ 2H2O(l) ΔH= -725.8 kJ·mol-1;
CO的燃烧热化学方程式为:CO(g)+ 1/2 O2(g)= CO2(g) ΔH= -283 kJ·mol-1;
H2O (g) === H2O(l) ΔH= -44 kJ·mol-1
请写出甲醇不完全燃烧生成一氧化碳和水蒸气的热化学方程式
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)
①该电池中通入甲醇的是电源的
②若电解质溶液中KOH的物质的量为0.5mol,当有0.5mol甲醇参与反应时,产物恰好为KHCO3时,该电池的负极反应式为
您最近一年使用:0次
【推荐2】为减少碳氧化物的排放,工业上可回收 和
和 合成甲醇(
合成甲醇( )。
)。
(1)利用 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:
反应Ⅰ
反应Ⅱ
控制 和
和 初始投料比为
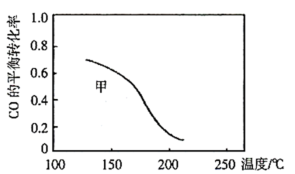
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
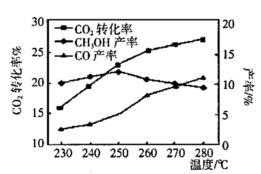
①反应Ⅰ能自发的反应条件:______ 。(填“低温”、“高温”、“任何温度”)
②由图可知温度升高 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是______ 。
③由图可知获取 最适宜的温度是
最适宜的温度是______ 。
④控制 和
和 初始投料比为
初始投料比为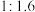 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为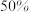 ,甲醇选择性为
,甲醇选择性为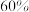 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是______ 。(甲醇的选择性:转化的 中生成甲醇的百分比)
中生成甲醇的百分比)
(2)利用 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:
反应Ⅲ
其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是______ 。
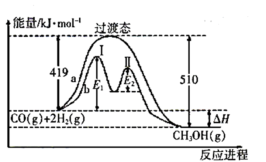
A. 上述反应的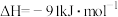
B. 反应正反应的活化能为
反应正反应的活化能为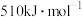
C. 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D. 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E. 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入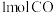 和
和 ,向乙中加入
,向乙中加入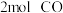 和
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线______ 。
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式______ 。
 和
和 合成甲醇(
合成甲醇( )。
)。(1)利用
 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:反应Ⅰ

反应Ⅱ

控制
 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
①反应Ⅰ能自发的反应条件:
②由图可知温度升高
 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是③由图可知获取
 最适宜的温度是
最适宜的温度是④控制
 和
和 初始投料比为
初始投料比为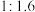 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为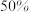 ,甲醇选择性为
,甲醇选择性为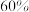 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是 中生成甲醇的百分比)
中生成甲醇的百分比)(2)利用
 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:反应Ⅲ

其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是

A. 上述反应的
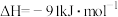
B.
 反应正反应的活化能为
反应正反应的活化能为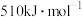
C.
 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应D.
 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E.
 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入
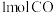 和
和 ,向乙中加入
,向乙中加入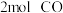 和
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】Ⅰ.甲醇是一种重要的化工原料,具有开发和应用的广阔前景。如图所示,其中甲池的总反应式为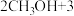
 ,完成下列问题:
,完成下列问题:
(1)甲池燃料电池的负极反应方程式为_______ 。
(2)甲池中消耗112mL(标准状况) ,此时乙池中溶液的体积为400mL,该溶液
,此时乙池中溶液的体积为400mL,该溶液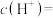
_______ 。
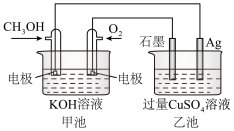
(3)若以该甲醇燃料电池为电源,用石墨做电极电解200mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),电路中转移的电子的物质的量是_______ mol。
Ⅱ.二氧化氯是一种安全稳定、高效低毒的消毒剂,工业上有多种制备方法。回答问题:
方法一:亚氯酸钠与氯气反应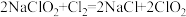 ,氯气由氯碱工业制得,如图1。
,氯气由氯碱工业制得,如图1。
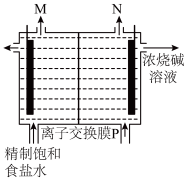
(4)P是_______ (填“阳”或“阴”)离子交换膜。
(5)写出图1总反应的化学方程式_______ 。
方法二:惰性电极电解氯化铵和盐酸,原理如图2。
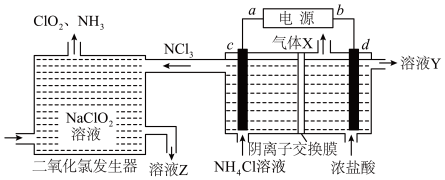
(6)图2中“气体X”是_______ (写化学式)。
(7)c的电极反应式为_______ 。
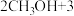
 ,完成下列问题:
,完成下列问题:(1)甲池燃料电池的负极反应方程式为
(2)甲池中消耗112mL(标准状况)
 ,此时乙池中溶液的体积为400mL,该溶液
,此时乙池中溶液的体积为400mL,该溶液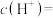

(3)若以该甲醇燃料电池为电源,用石墨做电极电解200mL含有如下离子的溶液。
| 离子 |  |  |  | 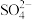 |
c/ | 0.25 | 1 | 1 | 0.25 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),电路中转移的电子的物质的量是
Ⅱ.二氧化氯是一种安全稳定、高效低毒的消毒剂,工业上有多种制备方法。回答问题:
方法一:亚氯酸钠与氯气反应
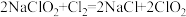 ,氯气由氯碱工业制得,如图1。
,氯气由氯碱工业制得,如图1。
(4)P是
(5)写出图1总反应的化学方程式
方法二:惰性电极电解氯化铵和盐酸,原理如图2。

(6)图2中“气体X”是
(7)c的电极反应式为
您最近一年使用:0次
【推荐1】使用可再生能源,如太阳能、潮汐能等产生的电能,通过电化学的方式将二氧化碳转化为高附加值的化学产品,如甲烷、乙烯、乙醇等是一种非常有前景的课题。
请回答下列问题:
(1)已知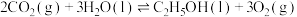
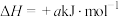 ,则
,则 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为____________ 。若已知 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为 ,
, 转化为乙醇的原理为
转化为乙醇的原理为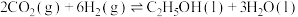

__________  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
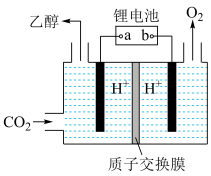
(2)以锂电池为电源,其电池总反应为 ,可将
,可将 转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g
转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g ,理论上会生成标准状况下
,理论上会生成标准状况下 的体积为
的体积为___________ L,装置中产生乙醇的电极反应式为__________________ ,若给锂电池充电,锂电池阳极的电极反应式为__________ 。
(3)若采用乙醇燃料电池作为电源探究氢氧化钾的制备和粗铜的精炼,装置如图所示。

①甲装置中左侧 电极的电极反应式为
电极的电极反应式为___________________ ,若9.2g乙醇参与反应,乙装置中铁电极上产生___________  气体。
气体。
②乙装置中X为阳离子交换膜,已知饱和氯化钾溶液中含有的溶质为1 ,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为
,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为___________ g。
请回答下列问题:
(1)已知
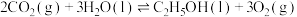
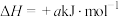 ,则
,则 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为 ,
, 转化为乙醇的原理为
转化为乙醇的原理为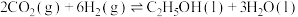

 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(2)以锂电池为电源,其电池总反应为
 ,可将
,可将 转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g
转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g ,理论上会生成标准状况下
,理论上会生成标准状况下 的体积为
的体积为
(3)若采用乙醇燃料电池作为电源探究氢氧化钾的制备和粗铜的精炼,装置如图所示。

①甲装置中左侧
 电极的电极反应式为
电极的电极反应式为 气体。
气体。②乙装置中X为阳离子交换膜,已知饱和氯化钾溶液中含有的溶质为1
 ,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为
,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。回答下列问题:
I.以尿素为原料在一定条件下发生反应: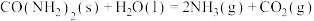
 。
。 与氮氧化物反应生成环境友好产物的反应过程与能量关系如图所示。
与氮氧化物反应生成环境友好产物的反应过程与能量关系如图所示。
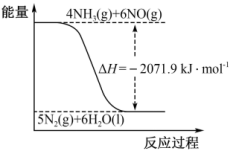
(1)尿素在一定条件下将氮的氧化物还原为氮气的热化学方程式为___________ 。
(2)当(1)中反应放出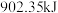 能量时,转移电子的物质的量为
能量时,转移电子的物质的量为___________ 。
II.图甲是一种利用微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成对环境友好物质的装置,同时利用此装置的电能在铁片上镀铜。
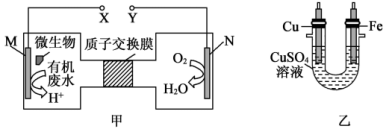
(3)铁电极应与______ 极(填“X”或“Y”)相连,H+应向______ 极(填“M”或者“N”)做定向移动。
(4)M极发生的电极反应式为_______ ;若铜片上的质量减少1.92g,则甲装置中消耗CO(NH2)2,的质量为_______ g。
(5)常温下,若将铁电极换成石墨电极并与Y极相连,则当电路中通过0.01mol电子时,铜电极发生的电极反应式为______ ,此时溶液的pH=_______ (此时溶液体积为100mL)。
I.以尿素为原料在一定条件下发生反应:
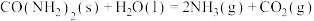
 。
。 与氮氧化物反应生成环境友好产物的反应过程与能量关系如图所示。
与氮氧化物反应生成环境友好产物的反应过程与能量关系如图所示。
(1)尿素在一定条件下将氮的氧化物还原为氮气的热化学方程式为
(2)当(1)中反应放出
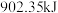 能量时,转移电子的物质的量为
能量时,转移电子的物质的量为II.图甲是一种利用微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成对环境友好物质的装置,同时利用此装置的电能在铁片上镀铜。

(3)铁电极应与
(4)M极发生的电极反应式为
(5)常温下,若将铁电极换成石墨电极并与Y极相连,则当电路中通过0.01mol电子时,铜电极发生的电极反应式为
您最近一年使用:0次
【推荐3】镍镉电池是应用广泛的二次电池,其总反应为: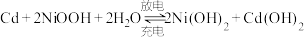 ,制造密封式镍镉电池的部分工艺如下:
,制造密封式镍镉电池的部分工艺如下:
Ⅰ. 的制备
的制备
以硫酸镍( )为原料制备
)为原料制备 的主要过程如下图所示。制备过程中,降低
的主要过程如下图所示。制备过程中,降低 沉淀速率,可以避免沉淀团聚,提升电池性能。
沉淀速率,可以避免沉淀团聚,提升电池性能。
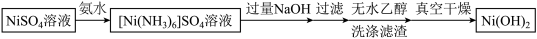
(1)制备过程中,需先加氨水,再加过量NaOH,请分析:
①先加氨水的目的是___________ 。
②用化学平衡移动原理分析加入NaOH需过量的原因是___________ 。
(2)用无水乙醇代替水洗涤滤渣的优点是___________ (答出1条即可)。
Ⅱ.镍镉电池的组装
主要步骤:①将 和
和 固定,中间以隔膜隔开(如图所示);②将多组上述结构串联;③向电池中注入KOH溶液;④密封。
固定,中间以隔膜隔开(如图所示);②将多组上述结构串联;③向电池中注入KOH溶液;④密封。

(3)下列对镍镉电池组装和使用的分析正确的是___________ (填字母序号)。
a.密封镍镉电池可以避免KOH变质
b.镍电极为电池的负极,镉电极为电池的正极
c.电池组装后,应先充电,再使用
Ⅲ.过度充电的保护
电池充电时,若 和
和 耗尽后继续充电,会造成安全隐患,称为过度充电。制造电池时,在镉电极加入过量的
耗尽后继续充电,会造成安全隐患,称为过度充电。制造电池时,在镉电极加入过量的 可对电池进行过度充电保护,该方法称为镉氧循环法。
可对电池进行过度充电保护,该方法称为镉氧循环法。
(4) 耗尽后继续充电,镉电极上生成的物质为
耗尽后继续充电,镉电极上生成的物质为___________ 。
(5)已知:①隔膜可以透过阴离子和分子;② 可以与Cd发生反应生成
可以与Cd发生反应生成 。请结合两个电极上的电极反应式说明用镉氧循环法实现过度充电保护的原理:
。请结合两个电极上的电极反应式说明用镉氧循环法实现过度充电保护的原理:___________ 。
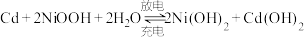 ,制造密封式镍镉电池的部分工艺如下:
,制造密封式镍镉电池的部分工艺如下:Ⅰ.
 的制备
的制备以硫酸镍(
 )为原料制备
)为原料制备 的主要过程如下图所示。制备过程中,降低
的主要过程如下图所示。制备过程中,降低 沉淀速率,可以避免沉淀团聚,提升电池性能。
沉淀速率,可以避免沉淀团聚,提升电池性能。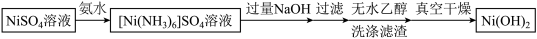
(1)制备过程中,需先加氨水,再加过量NaOH,请分析:
①先加氨水的目的是
②用化学平衡移动原理分析加入NaOH需过量的原因是
(2)用无水乙醇代替水洗涤滤渣的优点是
Ⅱ.镍镉电池的组装
主要步骤:①将
 和
和 固定,中间以隔膜隔开(如图所示);②将多组上述结构串联;③向电池中注入KOH溶液;④密封。
固定,中间以隔膜隔开(如图所示);②将多组上述结构串联;③向电池中注入KOH溶液;④密封。
(3)下列对镍镉电池组装和使用的分析正确的是
a.密封镍镉电池可以避免KOH变质
b.镍电极为电池的负极,镉电极为电池的正极
c.电池组装后,应先充电,再使用
Ⅲ.过度充电的保护
电池充电时,若
 和
和 耗尽后继续充电,会造成安全隐患,称为过度充电。制造电池时,在镉电极加入过量的
耗尽后继续充电,会造成安全隐患,称为过度充电。制造电池时,在镉电极加入过量的 可对电池进行过度充电保护,该方法称为镉氧循环法。
可对电池进行过度充电保护,该方法称为镉氧循环法。(4)
 耗尽后继续充电,镉电极上生成的物质为
耗尽后继续充电,镉电极上生成的物质为(5)已知:①隔膜可以透过阴离子和分子;②
 可以与Cd发生反应生成
可以与Cd发生反应生成 。请结合两个电极上的电极反应式说明用镉氧循环法实现过度充电保护的原理:
。请结合两个电极上的电极反应式说明用镉氧循环法实现过度充电保护的原理:
您最近一年使用:0次



