(1)反应A+3B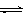 2C+2D在四种不同情况下的反应速率分别为:
2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol·L-1·s-1;②v(B)=0.6mol·L-1·s-1;
③v(C)=0.4mol·L-1·s-1;④v(D)=0.45mol·L-1·min-1。
该反应进行的快慢顺序为__ 。
(2)在密闭容器中进行可逆反应,A与B反应生成C,速率分别为:v1、v2、v3(mol·L-1·s-1),且v1、v2、v3之间有如下关系:v2=3v1,v3=2v1,则此反应的化学方程式表示为__ 。
(3)下列各项可以证明2HI(g)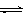 H2(g)+I2(g)已经达到平衡状态的是
H2(g)+I2(g)已经达到平衡状态的是__ 。
①单位时间内生成nmolI2的同时生成nmolHI;
②一个H—H键断裂的同时有两个H—I键断裂;
③百分组成ω(HI)=ω(H2)时;
④反应速率v(H2)=v(I2)=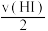 时;
时;
⑤c(H2)∶c(I2)∶c(HI)=1∶1∶2时;
⑥温度和体积一定,容器内压强不再变化时;
⑦温度和压强一定,混合气体的密度不再变化时;
⑧温度和体积一定,混合气体的颜色不再变化时。
(4)已知反应2HI(g)=H2(g)+I2(g)ΔH=11kJ·mol-1。1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为__ kJ。
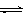 2C+2D在四种不同情况下的反应速率分别为:
2C+2D在四种不同情况下的反应速率分别为:①v(A)=0.15mol·L-1·s-1;②v(B)=0.6mol·L-1·s-1;
③v(C)=0.4mol·L-1·s-1;④v(D)=0.45mol·L-1·min-1。
该反应进行的快慢顺序为
(2)在密闭容器中进行可逆反应,A与B反应生成C,速率分别为:v1、v2、v3(mol·L-1·s-1),且v1、v2、v3之间有如下关系:v2=3v1,v3=2v1,则此反应的化学方程式表示为
(3)下列各项可以证明2HI(g)
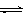 H2(g)+I2(g)已经达到平衡状态的是
H2(g)+I2(g)已经达到平衡状态的是①单位时间内生成nmolI2的同时生成nmolHI;
②一个H—H键断裂的同时有两个H—I键断裂;
③百分组成ω(HI)=ω(H2)时;
④反应速率v(H2)=v(I2)=
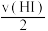 时;
时;⑤c(H2)∶c(I2)∶c(HI)=1∶1∶2时;
⑥温度和体积一定,容器内压强不再变化时;
⑦温度和压强一定,混合气体的密度不再变化时;
⑧温度和体积一定,混合气体的颜色不再变化时。
(4)已知反应2HI(g)=H2(g)+I2(g)ΔH=11kJ·mol-1。1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
更新时间:2020-09-14 16:10:27
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)  2NO2(g) ΔH,随温度升高,混合气体的颜色变深。
2NO2(g) ΔH,随温度升高,混合气体的颜色变深。
回答下列问题:
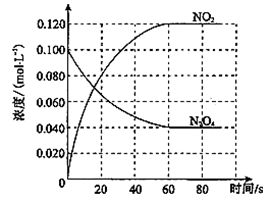
(1)反应的ΔH_____ 0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,平均反应速率v(NO2)为________ mol·L-1·s-1,反应的平衡常数K为(数值)__________ 。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4) 以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。则T__________ 100℃(填“大于”或“小于”)。
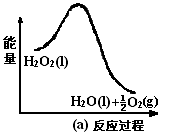
(3)利用图(a)和(b)中的信息,按图(b)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的_________ (填“深”或“浅”),其原因是__________________ 。

 2NO2(g) ΔH,随温度升高,混合气体的颜色变深。
2NO2(g) ΔH,随温度升高,混合气体的颜色变深。
回答下列问题:
(1)反应的ΔH
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4) 以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。则T
(3)利用图(a)和(b)中的信息,按图(b)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的


您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2(含有杂质MnO和MnCO3)制取纯MnO2的流程如下:

请回答下列问题:
(1)为加快酸浸速率可采取的措施有______________________________________ (答两点)。酸浸过程中稀硫酸可否用盐酸代替,回答并说明理由_________________________ 。
(2)操作X的名称是____________ 。氧化过程反应的离子方程式是________________ 。
(3)加热条件下Cl2与NaOH溶液反应,其氧化产物和还原产物的物质的量之比为________ 。
(4)酸浸过程中得到的溶液所含主要溶质为____________ ,电解该溶液也可制得MnO2和H2,写出该电解过程中阳极的电极反应式________________________________ 。
(5)MnO2常用作某些化学反应的催化剂。下图为2H2O2=2H2O+O2↑反应过程中的能量变化示意图,下列说法正确的是__________ 。
a.该反应为吸热反应,热效应为△H
b.反应历程b有催化剂参加
c.有催化剂时,该反应的活化能为E1+E2
d.改变催化剂,可改变该反应的活化能

请回答下列问题:
(1)为加快酸浸速率可采取的措施有
(2)操作X的名称是
(3)加热条件下Cl2与NaOH溶液反应,其氧化产物和还原产物的物质的量之比为
(4)酸浸过程中得到的溶液所含主要溶质为
(5)MnO2常用作某些化学反应的催化剂。下图为2H2O2=2H2O+O2↑反应过程中的能量变化示意图,下列说法正确的是

a.该反应为吸热反应,热效应为△H
b.反应历程b有催化剂参加
c.有催化剂时,该反应的活化能为E1+E2
d.改变催化剂,可改变该反应的活化能
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲烷水蒸气重整制取的合成气可用于熔融碳酸盐燃料电池。
(1)制取合成气的反应为CH4(g)+H2O(g) CO(g)+3H2(g)H =+206 kJ/mol。
CO(g)+3H2(g)H =+206 kJ/mol。
向体积为2 L密闭容器中,按n(H2O)∶n(CH4)=1投料:
a.保持温度为T1时,测得CH4(g)的浓度随时间变化曲线如图1所示。
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,CH4的转化率随反应温度的变化如图2所示。
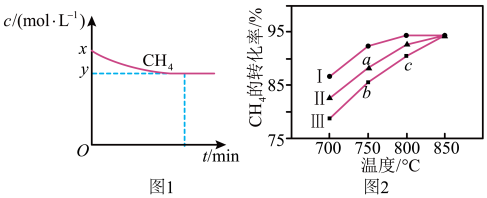
①结合图1,写出反应达平衡的过程中的能量变化:______ kJ。
②在图1中画出:起始条件相同,保持温度为T2(T2> T1)时, c(CH4)随时间的变化曲线______ 。
③根据图2判断:
ⅰ. a点所处的状态不是化学平衡状态,理由是_______ 。
ⅱ. CH4的转化率:c>b,原因是________ 。
(2)熔融碳酸盐燃料电池的结构示意图如下。

①电池工作时,熔融碳酸盐中CO32-移向________ (填“电极A”或“电极B”)
②写出正极上的电极反应:________ 。
(3)若不考虑副反应,1 kg甲烷完全转化所得到的合成气全部用于燃料电池中,外电路通过的电子的物质的量最大为_____ mol。
(1)制取合成气的反应为CH4(g)+H2O(g)
 CO(g)+3H2(g)H =+206 kJ/mol。
CO(g)+3H2(g)H =+206 kJ/mol。向体积为2 L密闭容器中,按n(H2O)∶n(CH4)=1投料:
a.保持温度为T1时,测得CH4(g)的浓度随时间变化曲线如图1所示。
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,CH4的转化率随反应温度的变化如图2所示。

①结合图1,写出反应达平衡的过程中的能量变化:
②在图1中画出:起始条件相同,保持温度为T2(T2> T1)时, c(CH4)随时间的变化曲线
③根据图2判断:
ⅰ. a点所处的状态不是化学平衡状态,理由是
ⅱ. CH4的转化率:c>b,原因是
(2)熔融碳酸盐燃料电池的结构示意图如下。

①电池工作时,熔融碳酸盐中CO32-移向
②写出正极上的电极反应:
(3)若不考虑副反应,1 kg甲烷完全转化所得到的合成气全部用于燃料电池中,外电路通过的电子的物质的量最大为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如下图。

(1)丙烷脱氢制丙烯的过程中。恒压时向原料气中掺入高温水蒸气,则K(主反应)_______ (填“增大”、“减小”或不变”,下同),转化率α(C3H8)_______ 。温度升高,副反应更容易发生的主要原因是_______ 。
(2)先以丙烯制丙烯腈,再用丙烯腈在阴极电合成已二腈(弱酸环境),总反应式:2CH2=CH-CN+H2O=NC(CH2)4CN+1/2O2↑,则阳极电极反应式:_______ 。
II.在2.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应:CH4(g)+2NO2(g)⇌CO2(g)+N2(g)+2H2O(g) △H<0,温度为T1和T2下,反应时间(t)与容器内甲烷物质的量数据见下表:
(3)计算T1、0~2min内NO2的平均反应速率v(NO2)=_______ mol·L-1·min-1,温度T2下的平衡常数K=_______ mol·L-1(若提供的数据不足以计算,填“无法确定”)。
(4)在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,不同温度下,NO2的转化率随温度的变化如下图。c点_______ (填“是”或“不是”)反应达平衡的点。


(1)丙烷脱氢制丙烯的过程中。恒压时向原料气中掺入高温水蒸气,则K(主反应)
(2)先以丙烯制丙烯腈,再用丙烯腈在阴极电合成已二腈(弱酸环境),总反应式:2CH2=CH-CN+H2O=NC(CH2)4CN+1/2O2↑,则阳极电极反应式:
II.在2.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应:CH4(g)+2NO2(g)⇌CO2(g)+N2(g)+2H2O(g) △H<0,温度为T1和T2下,反应时间(t)与容器内甲烷物质的量数据见下表:
| 时间(t/min) | 0 | 2 | 4 | 6 | 10 | 12 |
| T1,甲烷物质的量 | 0.10 | 0.082 | 0.068 | 0.060 | 0.045 | 0.045 |
| T2,甲烷物质的量 | 0.10 | 0.080 | 0.065 | 0.055 | 0.050 | _ |
(4)在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,不同温度下,NO2的转化率随温度的变化如下图。c点

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】CO2的资源化利用能有效减少碳排放充分利用碳资源。
I.CO2合成甲醇(CH3OH)
该反应包括下列两步:
反应I CO2(g)+H2(g) CO(g)+ H2O(g) △H1=+40.9 kJ/mol
CO(g)+ H2O(g) △H1=+40.9 kJ/mol
反应II CO2(g)+3H2(g) CH3OH(g)+ H2O(g) △H2=+49.5 kJ/mol
CH3OH(g)+ H2O(g) △H2=+49.5 kJ/mol
(1)由CO与H2合成CH3OH(g)的热化学方程式为_______ 。
(2)在一定温度下,向体积为2 L的恒容密闭容器中充入3molH2和1molCO2,控制条件仅发生反应I,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:_______ 。
②在平衡后,再向容器中加入2mol CO2(g)和2mol CH3OH(g)则平衡向_______ 移动。(填“正反应方向”“逆反应方向”或“不移动”)。
(3)在光电催化下CO2可以合成甲醇,原理如图所示。阴极的电极反应式为_______ 。
控制反应条件,同时发生反应Ⅰ、反应Ⅱ和反应Ⅲ,可以合成二甲醚(CH3OCH3)。
反应Ⅲ 2CH3OH(g) CH3OCH3(g)+H2O(g) △H=-24.5 kJ/mol
CH3OCH3(g)+H2O(g) △H=-24.5 kJ/mol
在压强30 MPa、 =4时, CO2的平衡转化率、CO的选择性和CH3OCH3的选择性随温度变化情况如图所示(X的选择性=
=4时, CO2的平衡转化率、CO的选择性和CH3OCH3的选择性随温度变化情况如图所示(X的选择性= )
)_______ (填“A”、“B”或“C”)。
(5)当温度超过290℃,曲线B随温度升高而增大的原因是_______ 。
I.CO2合成甲醇(CH3OH)
该反应包括下列两步:
反应I CO2(g)+H2(g)
 CO(g)+ H2O(g) △H1=+40.9 kJ/mol
CO(g)+ H2O(g) △H1=+40.9 kJ/mol反应II CO2(g)+3H2(g)
 CH3OH(g)+ H2O(g) △H2=+49.5 kJ/mol
CH3OH(g)+ H2O(g) △H2=+49.5 kJ/mol(1)由CO与H2合成CH3OH(g)的热化学方程式为
(2)在一定温度下,向体积为2 L的恒容密闭容器中充入3molH2和1molCO2,控制条件仅发生反应I,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
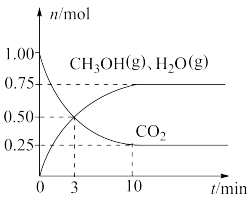
②在平衡后,再向容器中加入2mol CO2(g)和2mol CH3OH(g)则平衡向
(3)在光电催化下CO2可以合成甲醇,原理如图所示。阴极的电极反应式为

控制反应条件,同时发生反应Ⅰ、反应Ⅱ和反应Ⅲ,可以合成二甲醚(CH3OCH3)。
反应Ⅲ 2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H=-24.5 kJ/mol
CH3OCH3(g)+H2O(g) △H=-24.5 kJ/mol在压强30 MPa、
 =4时, CO2的平衡转化率、CO的选择性和CH3OCH3的选择性随温度变化情况如图所示(X的选择性=
=4时, CO2的平衡转化率、CO的选择性和CH3OCH3的选择性随温度变化情况如图所示(X的选择性= )
)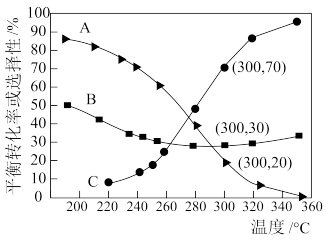
(5)当温度超过290℃,曲线B随温度升高而增大的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。
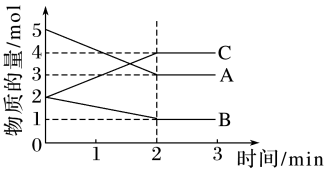
(1)该反应的化学方程式为___________ 。
(2)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是___________ (填序号)。
①降低温度 ②加入催化剂 ③增大容器体积 ④移走部分A ⑤恒容时,充入氦气
(3)一定温度下,氧化铁可与一氧化碳发生反应:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)。在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成单质铁11.2g。10min内v(CO)=___________ 。
(4)下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是___________(填字母)。
(5)在2Z(g)+Y(g) 3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是
3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是___________ (填字母)。
a.v(Z)正=2v(Y)逆
b.容器内压强保持不变
c.混合气体的平均摩尔质量保持不变
d.容器内混合气体的密度保持不变
e.Z的物质的量分数不变
(6)工业上利用CO2和H2合成甲醇,催化反应为3H2(g)+CO2(g) CH3OH(g)+H2O(g),在一恒温恒容密闭容器中充入3molH2和1molCO2进行上述反应,测得CO2(g)和CH3OH(g)浓度随时间变化如下图。
CH3OH(g)+H2O(g),在一恒温恒容密闭容器中充入3molH2和1molCO2进行上述反应,测得CO2(g)和CH3OH(g)浓度随时间变化如下图。

①从0min到3min,v(H2)=___________ mol·L-1·min-1
②反应前的压强与平衡时的压强之比为___________ 。
③下列表述正确的是___________ (填字母)。
A.第3分钟时v正(CH3OH)小于第10分钟时v逆(CH3OH)
B.混合气体的平均相对分子质量不随时间的变化而变化,反应达到平衡状态
C.达到平衡时CO2的转化率为75%
D.平衡混合气体中CO2(g)和H2(g)的质量之比是22:1

(1)该反应的化学方程式为
(2)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂 ③增大容器体积 ④移走部分A ⑤恒容时,充入氦气
(3)一定温度下,氧化铁可与一氧化碳发生反应:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)。在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成单质铁11.2g。10min内v(CO)=
(4)下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是___________(填字母)。
| A.v(H2)=0.1mol/(L∙min) | B.v(N2)=0.1mol/(L∙min) |
| C.v(NH3)=0.15mol/(L∙min) | D.v(N2)=0.002mol/(L∙s) |
 3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是
3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是a.v(Z)正=2v(Y)逆
b.容器内压强保持不变
c.混合气体的平均摩尔质量保持不变
d.容器内混合气体的密度保持不变
e.Z的物质的量分数不变
(6)工业上利用CO2和H2合成甲醇,催化反应为3H2(g)+CO2(g)
 CH3OH(g)+H2O(g),在一恒温恒容密闭容器中充入3molH2和1molCO2进行上述反应,测得CO2(g)和CH3OH(g)浓度随时间变化如下图。
CH3OH(g)+H2O(g),在一恒温恒容密闭容器中充入3molH2和1molCO2进行上述反应,测得CO2(g)和CH3OH(g)浓度随时间变化如下图。
①从0min到3min,v(H2)=
②反应前的压强与平衡时的压强之比为
③下列表述正确的是
A.第3分钟时v正(CH3OH)小于第10分钟时v逆(CH3OH)
B.混合气体的平均相对分子质量不随时间的变化而变化,反应达到平衡状态
C.达到平衡时CO2的转化率为75%
D.平衡混合气体中CO2(g)和H2(g)的质量之比是22:1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】接触法制硫酸工艺中,其主反应是在恒容、温度为450 ℃ 并有催化剂存在的条件下进行:2SO2(g)+O2(g) 2SO3(g) △H=﹣190 kJ/mol
2SO3(g) △H=﹣190 kJ/mol
①下列描述中能说明上述反应已达平衡的是________ 。
a.v(O2)正=2v(SO3)逆
b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化
d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=________ mol•L﹣1•min﹣1,若继续通入0.40 mol SO2和0.20 molO2则平衡________ 移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________ mol<n(SO3)<________ mol。
 2SO3(g) △H=﹣190 kJ/mol
2SO3(g) △H=﹣190 kJ/mol ①下列描述中能说明上述反应已达平衡的是
a.v(O2)正=2v(SO3)逆
b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化
d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组开展模拟工业合成氨的制备实验,在2 L密闭容器内,T ℃时发生反应:N2(g)+3H2(g)=2NH3(g),在体系中,n(N2)随时间的变化如下表:
(1)上述反应在第5 min时,N2的转化率(已反应的浓度与起始浓度的比例,用百分数表示)为___________ %;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=___________ ;
(3)T ℃时,在4个均为2 L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为___________ (用字母填空,下同);
a.v(NH3)=0.05 mol ·L-1·min-1 b.v(H2)=0.005 mol·L-1·s-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.01 mol·L-1·min-1
(4)下列表述能作为上述实验中可逆反应达到化学平衡状态的标志是___________ ;
a.反应速率v(N2)︰v(H2)︰v(NH3)=1︰3︰2 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2 f.v(N2)消耗=2 v(NH3)消耗
g.单位时间内3 mol H—H键断裂的同时2 mol N—H键也断裂
(5)下列措施不能使上述化学反应速率加快的是___________ 。
a.及时分离出NH3气体 b.适当升高温度
c.增大N2的浓度 d.选择高效催化剂
(6)写出实验室用固固加热法制备氨气的化学方程式:______
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5 min时,N2的转化率(已反应的浓度与起始浓度的比例,用百分数表示)为
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=
(3)T ℃时,在4个均为2 L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为
a.v(NH3)=0.05 mol ·L-1·min-1 b.v(H2)=0.005 mol·L-1·s-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.01 mol·L-1·min-1
(4)下列表述能作为上述实验中可逆反应达到化学平衡状态的标志是
a.反应速率v(N2)︰v(H2)︰v(NH3)=1︰3︰2 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2 f.v(N2)消耗=2 v(NH3)消耗
g.单位时间内3 mol H—H键断裂的同时2 mol N—H键也断裂
(5)下列措施不能使上述化学反应速率加快的是
a.及时分离出NH3气体 b.适当升高温度
c.增大N2的浓度 d.选择高效催化剂
(6)写出实验室用固固加热法制备氨气的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知:反应aA(g)+bB(g)⇌cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。经测定前4s内v(C)=0.05mol•L-1•s-1,则该反应的化学方程式为_____ .
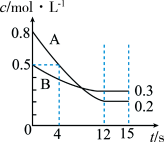
(2)锌与盐酸反应过程中,如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是_____ (填字母)
A.CH3COONa B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
(3)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是_____ (填序号)。写出该装置正极的电极反应_____ 。若构建原电池④时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为_____ 。

(4)氢氧燃料电池,是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)氢氧燃料电池;
①如果是碱性燃料电池则负极反应方程式是:_____ ;
②如果是酸性燃料电池则正极反应方程式是:_____ 。

(2)锌与盐酸反应过程中,如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是
A.CH3COONa B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
(3)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是

(4)氢氧燃料电池,是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)氢氧燃料电池;
①如果是碱性燃料电池则负极反应方程式是:
②如果是酸性燃料电池则正极反应方程式是:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
I.利用反应:6NO2+8NH3 7N2+12H2O处理NO2。
7N2+12H2O处理NO2。
II.一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)⇌SO3(g)+NO(g) -Q。
III.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)⇌CH3OH(g)。
(1)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min内,平均反应速率v(NO2)=_______ 。
(2)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是_______ (选填编号)。
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
(3)如果II中反应的平衡常数K值变大,该反应_______ (选填编号)。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
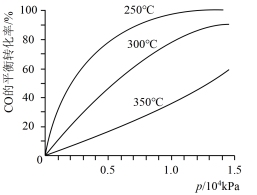
(4)对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应是_______ 反应(填“放热”或“吸热“)。实际生产条件控制在250℃、1.3×104KPa左右,简述选择此压强的理由:_______ 。
(5)向已酸化的FeCl3溶液中逐滴加入Na2S溶液,有浅黄色沉淀生成,溶液逐渐变为浅绿色。写出该反应的离子方程式_______ 。
(6)0.1mol/L的NaHSO3溶液中c(H+)>c(OH-),若往溶液中加入氨水至中性,则c(Na+)_______ c( )+c(
)+c( )+c(H2SO3)(填“>”、“<”或“=”)。往0.1mol/L的Na2SO3溶液加入少量Na2SO3固体,完全溶解后溶液中c(Na+):c(
)+c(H2SO3)(填“>”、“<”或“=”)。往0.1mol/L的Na2SO3溶液加入少量Na2SO3固体,完全溶解后溶液中c(Na+):c( )的比值
)的比值_______ (填“变大”、“变小”或“保持不变”)。
I.利用反应:6NO2+8NH3
 7N2+12H2O处理NO2。
7N2+12H2O处理NO2。II.一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)⇌SO3(g)+NO(g) -Q。
III.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)⇌CH3OH(g)。
(1)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min内,平均反应速率v(NO2)=
(2)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
(3)如果II中反应的平衡常数K值变大,该反应
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(4)对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应是

(5)向已酸化的FeCl3溶液中逐滴加入Na2S溶液,有浅黄色沉淀生成,溶液逐渐变为浅绿色。写出该反应的离子方程式
(6)0.1mol/L的NaHSO3溶液中c(H+)>c(OH-),若往溶液中加入氨水至中性,则c(Na+)
 )+c(
)+c( )+c(H2SO3)(填“>”、“<”或“=”)。往0.1mol/L的Na2SO3溶液加入少量Na2SO3固体,完全溶解后溶液中c(Na+):c(
)+c(H2SO3)(填“>”、“<”或“=”)。往0.1mol/L的Na2SO3溶液加入少量Na2SO3固体,完全溶解后溶液中c(Na+):c( )的比值
)的比值
您最近一年使用:0次
【推荐2】甲醇是一种重要的有机化工原料。
(1)已知:
①C2H4(g)+H2O(g)→C2H5OH(g) ΔH1=-45.5 kJ/mol
②2CH3OH(g)→CH3OCH3(g)+H2O(g) ΔH2=-23.9 kJ/mol
③C2H5OH(g)→CH3OCH3(g) ΔH3=+50.7 kJ/mol
请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:__________ 。
(2)合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
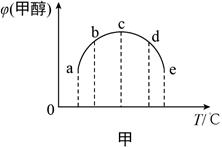
①温度升高甲醇的体积分数增大的原因是__________ .
②根据图象判断ΔH__________ (填“>”、“<”或“=”)0。
(3)为了研究甲醇转化为二甲醚的反应条件,某研究与小组在三个体积均为1.0 L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=-23.9 kJ/mol。
CH3OCH3(g)+H2O(g) ΔH2=-23.9 kJ/mol。
①T1温度下该反应的平衡常数K=__________ ;反应温度T1__________ T2(填“大于”或“小于”。)
②容器Ⅱ中a=__________ 。
③下列说法能说明反应达到平衡状态的是__________ (填字母)。
A.容器中气体压强不再变化
B.用CH3OH和CH3OCH3表示的反应速率之比为2:1
C.混合气体的密度不变
D.容器内CH3OH和CH3OCH3的浓度之比为2:1
E.混合气体中c(CH3OCH3)不变
(1)已知:
①C2H4(g)+H2O(g)→C2H5OH(g) ΔH1=-45.5 kJ/mol
②2CH3OH(g)→CH3OCH3(g)+H2O(g) ΔH2=-23.9 kJ/mol
③C2H5OH(g)→CH3OCH3(g) ΔH3=+50.7 kJ/mol
请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:
(2)合成甲醇的反应为:CO(g)+2H2(g)
 CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
①温度升高甲醇的体积分数增大的原因是
②根据图象判断ΔH
(3)为了研究甲醇转化为二甲醚的反应条件,某研究与小组在三个体积均为1.0 L的恒容密闭容器中发生反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH2=-23.9 kJ/mol。
CH3OCH3(g)+H2O(g) ΔH2=-23.9 kJ/mol。| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | T1 | 0.20 | 0.080 | 0.080 |
| Ⅱ | T1 | 0.40 | A | a |
| Ⅲ | T2 | 0.20 | 0.090 | 0.090 |
①T1温度下该反应的平衡常数K=
②容器Ⅱ中a=
③下列说法能说明反应达到平衡状态的是
A.容器中气体压强不再变化
B.用CH3OH和CH3OCH3表示的反应速率之比为2:1
C.混合气体的密度不变
D.容器内CH3OH和CH3OCH3的浓度之比为2:1
E.混合气体中c(CH3OCH3)不变
您最近一年使用:0次
【推荐3】工业生产中常常产生硫的氧化物和氮的氧化物,对环境产生重大影响,为减少对环境的污染,科学工作者采用“O3氧化法”和“光催化氧化法”对工业烟气脱硫、脱硝,原理如下。回答下列问题:
I.O3氧化法
(1)用O3氧化烟气中的SO2时,体系中存在以下反应:
a)SO2(g)+O3(g)⇌SO3(g)+O2(g) △H1=-241.6kJ/mol K1
b)2O3(g)⇌3O2(g) △H2=-286.6kJ/mol K2
c)2SO2(g)+O2(g)⇌2SO3(g) △H3 K3
根据盖斯定律,△H3=_______ ,K3=_______ (用含K1、K2的式子表示)。
(2)在密闭容器中充入1molN2O4和1molO3,发生以下反应:
d)N2O4(g)⇌2NO2(g) △H4=+57kJ/mol
e)N2O4(g)+O3(g)⇌N2O5(g)+O2(g) △H5
不同压强(P)下,N2O4平衡转化率α(N2O4)随反应温度(T)的变化关系如图1所示。_______ 0(填“>”或“<”),若缩小体积增大压强,B点可能向_______ 点移动(填“A”或“C”)。
②下列有关该反应体系的说法正确的是_______ (填标号)。
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在n(NO2)+n(N2O4)+n(N2O5)>1mol
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大N2O4的浓度,反应d的正反应速率增大,e的正反应速率减小
③某温度下,t分钟后达到平衡,此时N2O4的物质的量分数为1/3,且NO2与O2的物质的量分数相等,v(O2)=_______ mol/min
Ⅱ.光催化氧化法
光照条件下,催化剂TiO2表面产生电子(e-)和空穴(h+)。电子与O2作用生成离子自由基(·O ),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO
),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO 。变化过程如图2所示。
。变化过程如图2所示。_______ 。
(4)已知该过程中生成的HNO2可继续与·OH发生反应:HNO2+2·OH=H++NO +H2O;该反应可分两步进行,请补充反应i:
+H2O;该反应可分两步进行,请补充反应i:
i:_______ ;
ii.NO2+·OH=H++NO 。
。
I.O3氧化法
(1)用O3氧化烟气中的SO2时,体系中存在以下反应:
a)SO2(g)+O3(g)⇌SO3(g)+O2(g) △H1=-241.6kJ/mol K1
b)2O3(g)⇌3O2(g) △H2=-286.6kJ/mol K2
c)2SO2(g)+O2(g)⇌2SO3(g) △H3 K3
根据盖斯定律,△H3=
(2)在密闭容器中充入1molN2O4和1molO3,发生以下反应:
d)N2O4(g)⇌2NO2(g) △H4=+57kJ/mol
e)N2O4(g)+O3(g)⇌N2O5(g)+O2(g) △H5
不同压强(P)下,N2O4平衡转化率α(N2O4)随反应温度(T)的变化关系如图1所示。

②下列有关该反应体系的说法正确的是
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在n(NO2)+n(N2O4)+n(N2O5)>1mol
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大N2O4的浓度,反应d的正反应速率增大,e的正反应速率减小
③某温度下,t分钟后达到平衡,此时N2O4的物质的量分数为1/3,且NO2与O2的物质的量分数相等,v(O2)=
Ⅱ.光催化氧化法
光照条件下,催化剂TiO2表面产生电子(e-)和空穴(h+)。电子与O2作用生成离子自由基(·O
 ),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO
),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO 。变化过程如图2所示。
。变化过程如图2所示。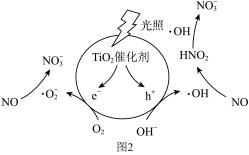
(4)已知该过程中生成的HNO2可继续与·OH发生反应:HNO2+2·OH=H++NO
 +H2O;该反应可分两步进行,请补充反应i:
+H2O;该反应可分两步进行,请补充反应i:i:
ii.NO2+·OH=H++NO
 。
。
您最近一年使用:0次



