O3在水中易分解.一定条件下,起始浓度均为0.0216mol/L的O3溶液,在不同的pH、温度下,发生分解反应,测得O3浓度减少一半所需的时间(t)如表所示:
下列判断不正确的是( )
| 3.0 | 4.0 | 5.0 | 6.0 | |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
下列判断不正确的是( )
| A.实验表明,升高温度能加快O3的分解速率 |
| B.pH增大能加速O3分解,表明OH﹣可以对O3的分解起催化作用 |
| C.在30℃、pH=4.0时,O3的分解速率为1.00×10﹣4mol/(L•min) |
| D.据表中的规律可推知,O3在下列条件下的分解速率v(40℃、pH=3.0)>v(30℃、pH=7.0) |
19-20高一·贵州贵阳·期末 查看更多[6]
贵州省贵阳十四中2019-2020学年高一下学期期末考试化学试题山东省淄博市沂源县第二中学2020-2021学年高一下学期期中考试化学试题山东省淄博市2021-2022学年高一下学期期中考试化学试题(已下线)【2022】【高一下】【杭师大附】【期中考】【高中化学】【洪翔峰收集】山东省新泰市第一中学东校2022-2023学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【期中考】【杭师大附中】【高中化学】【张明涛收集】
更新时间:2020-09-28 07:07:35
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验方案中,能达到实验目的的是
| 选项 | 实验方案. | 实验目的 |
| A | 将SO2和CO2分别通入水中达到饱和,用pH计立即测定溶液的pH,比较pH大小 | 确定亚硫酸和碳酸的酸性强弱 |
| B | 将CO2和SO2气体分别通入BaCl2溶液中 | 鉴别CO2和SO2气体 |
| C | 将SO2通入NaHCO3溶液后,将混合气体依次通入酸性KMnO4溶液、品红溶液、澄清石灰水 | 验证非金属性:S>C |
| D | 相同条件下,在两个试管中各加入3 mL6%的H2O2溶液,再向H2O2溶液中分别滴入1 mL H2O和1 mL FeCl3溶液,观察并比较H2O2的分解速率 | 探究催化剂对H2O2分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】我国科学家提出了由CO2和CH4直接转化为CH3COOH的催化反应进程,该进程如图所示。下列说法错误的是
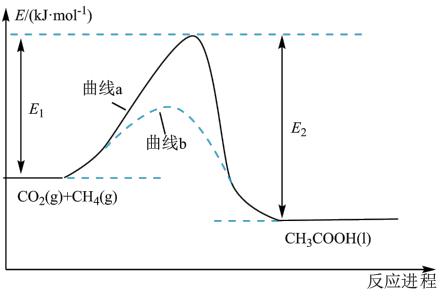

| A.该反应是放热反应 | B.曲线a的活化能大于曲线b |
| C.上述化学工艺符合绿色化学要求 | D.醋酸溶液中存在1个电离平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定条件下合成乙烯: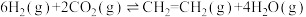 。已知其它条件不变时,温度对
。已知其它条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
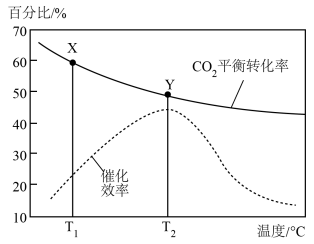
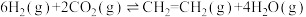 。已知其它条件不变时,温度对
。已知其它条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
A.平衡常数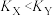 | B.反应速率: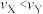 |
C.所含总能量: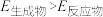 | D.经过相同时间后得到乙烯的量:X>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度下,将等物质的量的气体A、B混合于1L的密闭容器中,发生如下反应:A(g)+3B(g)⇌2C(g)+xD(g)。经2min后测得C的浓度为0.5mol/L,B的物质的量分数为25%,以D表示2min内的平均反应速率v(D)=0.25mol/L·min),下列说法正确的是
| A.2min时,v(A)=0.125mol/L·min |
| B.2min时,B的物质的量为0.75mol |
| C.x=1 |
| D.反应前后容器内气体的压强之比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1.下列判断错误的是
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1.下列判断错误的是
 xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1.下列判断错误的是
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1.下列判断错误的是| A.x=1 |
| B.2 min内A的反应速率为0.3 mol·L-1·min-1 |
| C.初始压强和平衡时压强比为10: 9 |
| D.B的转化率为50% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】探究草酸(H2C2O4)的性质,室温下进行以下两组实验:(已知:室温下,H2C2O4的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5)
下列有关实验说法正确的是( )
| 实验 | 装置 | 试剂a |
| ① |  | 0.1mol·L-1NaOH溶液VmL |
| ② | 0.01mol·L-1酸性KMnO4溶液mL |
| A.若实验①中V=2,则混合后溶液中:c(C2O42-)>c(H2C2O4) |
| B.若实验①中V=4,则混合后溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-) |
| C.实验②反应的离子方程式为5C2O42-+16H++2MnO4-=2Mn2++10CO2↑+8H2O |
| D.若实验②测得KMnO4溶液的褪色时间为40s,则这段时间内的平均反应速率v(KMnO4)=2.5×10-4mol•L-1•s-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如题所示。已知:O3的起始浓度为0.0216 mol/L。下列说法正确的是


| A.O3可漂白有机色素,这体现O3的强还原性 |
| B.O3可以消毒杀菌,故对人体百利而无一害 |
C.在30℃、pH=4.0条件下,O3的分解速率为 |
| D.根据表中规律:①40℃、pH=3.0;②10℃、pH=4.0;③30℃、pH=7.0,分解速率关系为:③>①>② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关热化学方程式N2O4(g) 2NO2(g) ΔH=+57 kJ·mol-1说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1说法正确的是
 2NO2(g) ΔH=+57 kJ·mol-1说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1说法正确的是| A.升高体系温度正反应速率增大,逆反应速率也增大 |
| B.若容器体积不变,气体密度不变时说明该反应已经达到化学平衡状态 |
| C.温度不变,向平衡后的容器中再加入少量N2O4,平衡常数K值变大 |
| D.增大体系的压强,平衡右移,同时提高N2O4的反应速率和转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各组物质反应,反应刚开始时,放出 的速率最大的是
的速率最大的是
 的速率最大的是
的速率最大的是| 编号 | 金属(粉末状) | 酸的浓度 | 酸的体积 | 反应起始温度 |
| A | 0.1 mol Zn | 3mol·L  | 10 mL | 30℃ |
| B | 0.1 mol Fe | 3mol·L  | 10 mL | 30℃ |
| C | 0.1 mol Zn | 6mol·L  | 10 mL | 30℃ |
| D | 0.1 mol Zn | 3mol·L HCl HCl | 10 mL | 30℃ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列做法,不能使Zn+2HCl = ZnCl2 + H2↑的反应速率增大的是
| A.增大盐酸的浓度 | B.降低温度 |
| C.用锌粉代替锌粒 | D.滴加少量CuCl2溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某小组利用硫代硫酸钠溶液与稀硫酸反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,探究反应条件对速率的影响,下列有关说法不正确的是
| 选项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | x |
| ③ | 50 | 10 | 0.1 | 5 | 0.2 | 5 |
| A.可通过产生浑浊的时间判断反应的快慢 |
| B.①②两组实验可探究Na2S2O3浓度对反应速率的影响,则x=5 |
| C.①③两组实验可探究温度对反应速率的影响 |
| D.实验结束后,有少量S附着在试管上,可以用水冲洗干净 |
您最近一年使用:0次

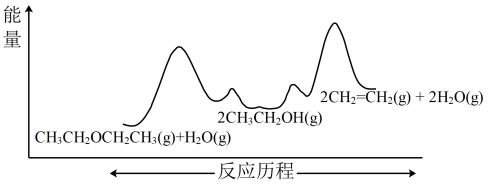
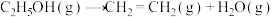
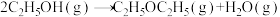
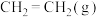 比
比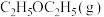 更稳定
更稳定 大于反应①的
大于反应①的


