为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50 mL密度为1.1 g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如下图所示。
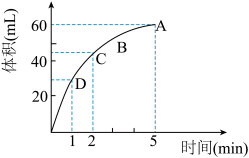
请依图回答下列问题:
(1)放出一半气体所需要的时间为_________________ ;
(2)A、B、C、D各点反应速率快慢的顺序是__________________ ;
(3)在5min后,收集到的气体体积不再增加,原因是______________________ ;
(4)过氧化氢溶液的初始物质的量浓度为__________ mol•L-1(保留两位有效数字)。
(5)在2L的密闭容器中充入一定量的SO3 气体,在一定温度和催化剂作用下,发生反应:2SO3 2SO2+O2,4min时达平衡状态,测得n(O2)=0.8mol,n(SO3)=6.4mol。求:氧气的生成速率v(O2)
2SO2+O2,4min时达平衡状态,测得n(O2)=0.8mol,n(SO3)=6.4mol。求:氧气的生成速率v(O2)_______ mol/(L·min),SO3的转化率______ ,此温度下平衡常数K=_______ 。

请依图回答下列问题:
(1)放出一半气体所需要的时间为
(2)A、B、C、D各点反应速率快慢的顺序是
(3)在5min后,收集到的气体体积不再增加,原因是
(4)过氧化氢溶液的初始物质的量浓度为
(5)在2L的密闭容器中充入一定量的SO3 气体,在一定温度和催化剂作用下,发生反应:2SO3
 2SO2+O2,4min时达平衡状态,测得n(O2)=0.8mol,n(SO3)=6.4mol。求:氧气的生成速率v(O2)
2SO2+O2,4min时达平衡状态,测得n(O2)=0.8mol,n(SO3)=6.4mol。求:氧气的生成速率v(O2)
更新时间:2020-10-08 08:16:21
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】H2O2是一种绿色消毒剂,在公共卫生事业中发挥了重要的作用。已知反应:H2O2 (l)= H2O(1) + O2(g) △H=-98 kJ/mol,K= 2.88×1020。回答问题:
O2(g) △H=-98 kJ/mol,K= 2.88×1020。回答问题:
(1)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是_______ 。
(2)纯H2O2 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2 剧烈分解:H2O2(l)=H2O(g)+ O2(g),放出大量气体,驱动火箭升空。每消耗 34g H2O2,理论上
O2(g),放出大量气体,驱动火箭升空。每消耗 34g H2O2,理论上______ (填“放出”或“吸收”)热量________ 98 kJ(填“大于”、“小于”或“等于”)。
(3)纯H2O2 相对稳定,实验表明在 54℃下恒温贮存2周,浓度仍能保持99%,原因是 H2O2 分解反应的_______ (填编号)。
a.ΔH比较小 b.K不够大 c.速率比较小 d.活化能比较大
(4)铜单质不溶于稀硫酸,向铜和稀硫酸的混合物中加入3% H2O2 溶液,可观察到铜溶解,溶液变蓝,实验室测得6.4g铜溶解放出24.258KJ热量,写出该反应的热化学方程式_______ 。
(5)向 H2O2 稀溶液中滴加数滴含 Mn2+的溶液,即有气泡快速逸出,反应中 Mn2+起______ 作用。某组实验数据如下:
0-30 min H2O2 反应的平均速率 v=_____ mol /(L·min) 。
 O2(g) △H=-98 kJ/mol,K= 2.88×1020。回答问题:
O2(g) △H=-98 kJ/mol,K= 2.88×1020。回答问题:(1)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
(2)纯H2O2 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2 剧烈分解:H2O2(l)=H2O(g)+
 O2(g),放出大量气体,驱动火箭升空。每消耗 34g H2O2,理论上
O2(g),放出大量气体,驱动火箭升空。每消耗 34g H2O2,理论上(3)纯H2O2 相对稳定,实验表明在 54℃下恒温贮存2周,浓度仍能保持99%,原因是 H2O2 分解反应的
a.ΔH比较小 b.K不够大 c.速率比较小 d.活化能比较大
(4)铜单质不溶于稀硫酸,向铜和稀硫酸的混合物中加入3% H2O2 溶液,可观察到铜溶解,溶液变蓝,实验室测得6.4g铜溶解放出24.258KJ热量,写出该反应的热化学方程式
(5)向 H2O2 稀溶液中滴加数滴含 Mn2+的溶液,即有气泡快速逸出,反应中 Mn2+起
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| c(H2O2)/mol /L | 0.70 | 0.49 | 0.35 | 0.25 | 0.17 | 0.12 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】苯乙烯是生产塑料与合成橡胶的重要原料。CO2氧化乙苯脱氢制苯乙烯的反应为:
反应I: (g)+CO2(g)
(g)+CO2(g)
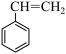 (g)+H2O(g)+CO(g) △H1
(g)+H2O(g)+CO(g) △H1
反应II: (g)
(g)
 (g)+H2(g) △H2
(g)+H2(g) △H2
反应III:CO2(g)+H2(g)=CO(g)+H2O(g) △H3=+41.2kJ•mol-1
回答下列问题:
(1)已知部分物质的燃烧热数据如表,利用表中数据计算△H2=_______ kJ•moL-1(用a、b、c表示)。
(2)下列关于反应I~III的说法正确的是_______ (填标号)。
(3)在催化剂MxOy作用下,CO2氧化乙苯脱氢制苯乙烯可能存在如图所示反应机理:
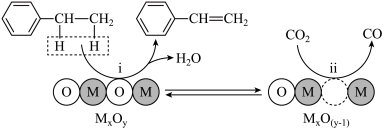
该机理可表示为以下两个反应,请补充反应ii。
i: (g)+MxOy(s)→
(g)+MxOy(s)→ (g)+MxO(y-1)(s)+H2O(g);
(g)+MxO(y-1)(s)+H2O(g);
ii:_______ 。
(4)常压下,乙苯和CO2经催化剂吸附后才能发生上述反应I。控制投料比[n(CO2)∶n(乙苯)]分别为1:1、5:1和10:1,并在催化剂作用下发生反应,乙苯平衡转化率与反应温度的关系如图所示:

①乙苯平衡转化率相同时,投料比越高,对应的反应温度越_______ (填“高”或“低”)。
②相同温度下,投料比远大于10:1时,乙苯的消耗速率明显下降,可能的原因是:i.乙苯的浓度过低;ii._______ 。
③850K时,反应经tmin达到图中P点所示状态,若初始时乙苯的物质的量为nmol,则v(苯乙烯)=______ mol•min-1。
(5)700K时,向恒容密闭容器中加入过量CaCO3和一定量乙苯,一定条件下发生反应I,初始和平衡时容器内压强分别为p1kPa和p2kPa,则平衡时苯乙烯的分压为_______ kPa(以含有p1、p2、p的代数式表示)。[已知:①混合气体中某组分的分压等于总压与该气体物质的量分数之积;以平衡分压代替平衡浓度进行计算,可得反应的分压平衡常数Kp。②CaCO3(s)=CaO(s)+CO2(g) Kp=pkPa]
反应I:
 (g)+CO2(g)
(g)+CO2(g)
 (g)+H2O(g)+CO(g) △H1
(g)+H2O(g)+CO(g) △H1反应II:
 (g)
(g)
 (g)+H2(g) △H2
(g)+H2(g) △H2反应III:CO2(g)+H2(g)=CO(g)+H2O(g) △H3=+41.2kJ•mol-1
回答下列问题:
(1)已知部分物质的燃烧热数据如表,利用表中数据计算△H2=
| 物质 | 乙苯 | 苯乙烯 | 氢气 |
| 燃烧热用焓变表示(kJ•mol-1) | -a | -b | -c |
| A.及时分离出水蒸气,有利于提高平衡混合物中苯乙烯的含量 |
| B.n(CO2)∶n(CO)保持恒定时,说明反应I达到化学平衡状态 |
| C.其他条件相同,反应II分别在恒容和恒压条件下进行,前者乙苯的平衡转化率更高 |
| D.反应III正反应的活化能小于逆反应的活化能 |

该机理可表示为以下两个反应,请补充反应ii。
i:
 (g)+MxOy(s)→
(g)+MxOy(s)→ (g)+MxO(y-1)(s)+H2O(g);
(g)+MxO(y-1)(s)+H2O(g);ii:
(4)常压下,乙苯和CO2经催化剂吸附后才能发生上述反应I。控制投料比[n(CO2)∶n(乙苯)]分别为1:1、5:1和10:1,并在催化剂作用下发生反应,乙苯平衡转化率与反应温度的关系如图所示:

①乙苯平衡转化率相同时,投料比越高,对应的反应温度越
②相同温度下,投料比远大于10:1时,乙苯的消耗速率明显下降,可能的原因是:i.乙苯的浓度过低;ii.
③850K时,反应经tmin达到图中P点所示状态,若初始时乙苯的物质的量为nmol,则v(苯乙烯)=
(5)700K时,向恒容密闭容器中加入过量CaCO3和一定量乙苯,一定条件下发生反应I,初始和平衡时容器内压强分别为p1kPa和p2kPa,则平衡时苯乙烯的分压为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g) =CO2(g) △H= - 393.51 kJ/mol
B(s)+O2(g)=CO2(g) △H= - 395.41 kJ/mol
则两种同素异形体中较稳定的是(填"A"或"B")___________________ 。
(2)工业上用H2和Cl2反应制HCl,各键能数据为:H – H:436 kJ/mol;Cl-Cl:243 kJ/mol;H-Cl:431 kJ/mol,该反应的热化学方程式是_____________________ 。
(3)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,已知l gCH4气体与O2气体反应生成CO气体和H2气体放2.25 kJ热量。
①写出相应热化学方程式______________ 。
②用甲烷制备合成气还可以发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2= +216kJ/mol。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。若x=0.2时,反应①放出的能量为____ kJ;若x=____ 时, 反应①与②放出(或吸收)的总能量为0。
(4)一定温度下,将3 mol A气体和l mol B气体通入一容积固定为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为
xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为_________ ; x为___________ 。可以作为达到平衡状态的标志是______________ 。
A.单位时间内生成n mol B的同时生成3n molA
B.混合气体的压强不变
C.混合气体的颜色不再改变(C为有色气体)
D.混合气体的密度不变
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g) =CO2(g) △H= - 393.51 kJ/mol
B(s)+O2(g)=CO2(g) △H= - 395.41 kJ/mol
则两种同素异形体中较稳定的是(填"A"或"B")
(2)工业上用H2和Cl2反应制HCl,各键能数据为:H – H:436 kJ/mol;Cl-Cl:243 kJ/mol;H-Cl:431 kJ/mol,该反应的热化学方程式是
(3)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,已知l gCH4气体与O2气体反应生成CO气体和H2气体放2.25 kJ热量。
①写出相应热化学方程式
②用甲烷制备合成气还可以发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2= +216kJ/mol。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。若x=0.2时,反应①放出的能量为
(4)一定温度下,将3 mol A气体和l mol B气体通入一容积固定为2 L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为
xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为A.单位时间内生成n mol B的同时生成3n molA
B.混合气体的压强不变
C.混合气体的颜色不再改变(C为有色气体)
D.混合气体的密度不变
您最近一年使用:0次
【推荐1】能源与信息、材料被称为现代社会发展的三大支柱。请回答下列问题。
(1)请判断,甲图②中的温度___________ (填“升高”或“降低”)。反应过程___________ (填“①”或“②”)的能量变化可用图乙表示。

(2)氢气被公认为是21世纪代替矿物燃料的理想能源, 氢气燃烧时放出
氢气燃烧时放出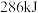 热量,而每千克汽油燃烧时放出的热量为
热量,而每千克汽油燃烧时放出的热量为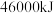 。试据此分析氢气作为能源代替汽油的优势
。试据此分析氢气作为能源代替汽油的优势___________ 。
(3)甲烷可消除 的污染,其反应为
的污染,其反应为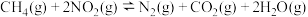 。在
。在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入 和
和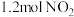 ,测得
,测得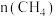 随时间变化的有关实验数据见下表。
随时间变化的有关实验数据见下表。
①组别 中,反应开始至
中,反应开始至 ,
,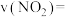
___________  。
。
②由实验数据可知实验控制的温度:T1______ T2 (填“ ”“
”“ ”或“
”或“ ”)。
”)。
③一定条件下,能说明该反应进行到最大限度的是___________ (填序号)。
a.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
b. 的浓度为0
的浓度为0
c.体系内物质的平均相对分子质量保持不变
d. 体系内气体的密度保持不变
(4) 、
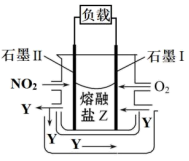
、 和熔融
和熔融 可制作燃料电池,其原理如图该电池在使用过程中石墨Ⅱ电极上生成氧化物
可制作燃料电池,其原理如图该电池在使用过程中石墨Ⅱ电极上生成氧化物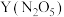 ,则石墨Ⅰ电极是
,则石墨Ⅰ电极是___________ (填“正极”或“负极”),电流从___________ (填“石墨Ⅰ”或“石墨Ⅱ”,下同)经导线流向___________ 。
(1)请判断,甲图②中的温度

(2)氢气被公认为是21世纪代替矿物燃料的理想能源,
 氢气燃烧时放出
氢气燃烧时放出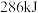 热量,而每千克汽油燃烧时放出的热量为
热量,而每千克汽油燃烧时放出的热量为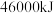 。试据此分析氢气作为能源代替汽油的优势
。试据此分析氢气作为能源代替汽油的优势(3)甲烷可消除
 的污染,其反应为
的污染,其反应为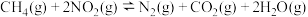 。在
。在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入 和
和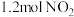 ,测得
,测得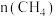 随时间变化的有关实验数据见下表。
随时间变化的有关实验数据见下表。| 组别 | 温度 | 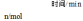 | 0 | 10 | 20 | 40 | 50 |
 |  | 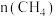 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
 |  | 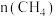 | 0.50 | 0.30 | 0.18 | 0.15 | 0.15 |
①组别
 中,反应开始至
中,反应开始至 ,
,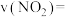
 。
。②由实验数据可知实验控制的温度:T1
 ”“
”“ ”或“
”或“ ”)。
”)。③一定条件下,能说明该反应进行到最大限度的是
a.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化b.
 的浓度为0
的浓度为0c.体系内物质的平均相对分子质量保持不变
d. 体系内气体的密度保持不变
(4)
 、
、 和熔融
和熔融 可制作燃料电池,其原理如图该电池在使用过程中石墨Ⅱ电极上生成氧化物
可制作燃料电池,其原理如图该电池在使用过程中石墨Ⅱ电极上生成氧化物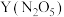 ,则石墨Ⅰ电极是
,则石墨Ⅰ电极是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】三氯化铬(CrCl3)为紫色单斜晶体,熔点为83℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化,工业上主要用作媒染剂和催化剂。
(1)某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示,其中锥形瓶内装有CCl4,其沸点为76.8℃。
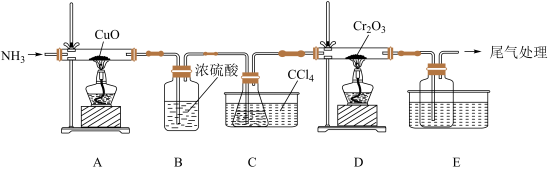
实验前先加热装置A,产生气体的化学方程式:___________ ,实验过程中需持续产生该气体,该气体的作用为___________ 。
(2)三价铬离子能形成多种配位化合物,配合物[Cr(NH3)3(H2O)2Cl]2+中元素电负性由大到小的顺序___________ 。
(3)装置D中还会生成光气(COCl2),D中反应的化学方程式为___________ 。
(4)该实验装置有设计不合理的地方,请写出改进方法:___________ (写一点即可)
(5)为进一步探究CrCl3的性质,某同学取试管若干支,分别加入10滴0.1 mol∙L−1 CrCl3溶液,并用4滴2 mol∙L−1 H2SO4酸化,再分别加入不同滴数的0.1 mol∙L−1KMnO4溶液,并在不同的温度下进行实验,反应现象记录于表中。
①浓度对反应的影响
CrCl3与KMnO4在常温下反应,观察不到Cr2O 离子的橙色,甲同学认为其中一个原因是Cr2O
离子的橙色,甲同学认为其中一个原因是Cr2O 离子的橙色被MnO
离子的橙色被MnO 离子的紫红色掩盖,另一种可能的原因是
离子的紫红色掩盖,另一种可能的原因是___________ ,所以必须将反应液加热至沸腾 后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
②CrCl3与KMnO4的用量对反应的影响
对表中数据进行分析,在上述反应条件下,欲将Cr3+氧化为Cr2O ,CrCl3与KMnO4最佳用量比为
,CrCl3与KMnO4最佳用量比为___________ 。这与由反应10Cr3+ + 6MnO + 11H2O
+ 11H2O Cr2O
Cr2O + 6Mn2+ + 22H+ 所推断得到的用量比不符,你推测的原因是
+ 6Mn2+ + 22H+ 所推断得到的用量比不符,你推测的原因是___________ 。
(1)某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示,其中锥形瓶内装有CCl4,其沸点为76.8℃。

实验前先加热装置A,产生气体的化学方程式:
(2)三价铬离子能形成多种配位化合物,配合物[Cr(NH3)3(H2O)2Cl]2+中元素电负性由大到小的顺序
(3)装置D中还会生成光气(COCl2),D中反应的化学方程式为
(4)该实验装置有设计不合理的地方,请写出改进方法:
(5)为进一步探究CrCl3的性质,某同学取试管若干支,分别加入10滴0.1 mol∙L−1 CrCl3溶液,并用4滴2 mol∙L−1 H2SO4酸化,再分别加入不同滴数的0.1 mol∙L−1KMnO4溶液,并在不同的温度下进行实验,反应现象记录于表中。
| KMnO4的用量 (滴数) | 在不同温度下的反应现象 | |
| 25℃ | 90~100℃ | |
| 1 | 紫红色 | 蓝绿色溶液 |
| 2~9 | 紫红色 | 黄绿色溶液,且随KMnO4滴数增加,黄色成分增多 |
| 10 | 紫红色 | 澄清的橙黄色溶液 |
| 11~23 | 紫红色 | 橙黄色溶液,有棕褐色沉淀,且随KMnO4滴数增加,沉淀增多 |
| 24~25 | 紫红色 | 紫红色溶液,有较多的棕褐色沉淀 |
CrCl3与KMnO4在常温下反应,观察不到Cr2O
 离子的橙色,甲同学认为其中一个原因是Cr2O
离子的橙色,甲同学认为其中一个原因是Cr2O 离子的橙色被MnO
离子的橙色被MnO 离子的紫红色掩盖,另一种可能的原因是
离子的紫红色掩盖,另一种可能的原因是 后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。②CrCl3与KMnO4的用量对反应的影响
对表中数据进行分析,在上述反应条件下,欲将Cr3+氧化为Cr2O
 ,CrCl3与KMnO4最佳用量比为
,CrCl3与KMnO4最佳用量比为 + 11H2O
+ 11H2O Cr2O
Cr2O + 6Mn2+ + 22H+ 所推断得到的用量比不符,你推测的原因是
+ 6Mn2+ + 22H+ 所推断得到的用量比不符,你推测的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硼是第IIIA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(B2H6)是最简单的硼烷。可以在乙醚介质中使用LiAlH4(离子化合物)还原BCl3获得,LiAlH4的电子式是___________ ,制备乙硼烷的化学方程式为___________ 。
(2)工业利用硼矿石(2MgO•B2O3)制备单质B并联产轻质MgO的流程如下:

硼酸(H3BO3)的溶解度
回答下列问题:
①为了加快硼矿石与Na2CO3溶液和CO2的反应速率,可以采取的措施有___________ (填一种)。
②操作1是___________ ,整过流程中可循环利用的物质是___________ 。
③制备B发生反应的化学方程式是___________ ,过程中易生成金属硼化物杂质。该杂质的化学式是___________ 。
(3)硼酸(H3BO3)是一元弱酸,在溶液中能电离生成[B(OH)4]-,硼酸的电离方程式为___________ ;室温时测得0.1000 mol•L-1硼酸溶液的pH=5.18,硼酸的电离常数Ka=___________
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(B2H6)是最简单的硼烷。可以在乙醚介质中使用LiAlH4(离子化合物)还原BCl3获得,LiAlH4的电子式是
(2)工业利用硼矿石(2MgO•B2O3)制备单质B并联产轻质MgO的流程如下:

硼酸(H3BO3)的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 80 |
| 溶解度/g | 2.77 | 3.65 | 4.87 | 6.77 | 8.90 | 23.54 |
①为了加快硼矿石与Na2CO3溶液和CO2的反应速率,可以采取的措施有
②操作1是
③制备B发生反应的化学方程式是
(3)硼酸(H3BO3)是一元弱酸,在溶液中能电离生成[B(OH)4]-,硼酸的电离方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
(1)甲醇脱氢法可制备甲醛,反应方程式为CH3OH⇌HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,该反应为____ 反应。

②下列方法中能加快反应速率的是___ (填字母)。
a.使用催化剂 b.升高温度 c.降低反应物浓度
(2)甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为___ (填“正”或“负”)极,在电极b上发生的反应类型为___ 反应。(填“氧化”或“还原”)

②探测仪工作时,电子从__ 极流出(填“a”或“b”),总反应方程式为____ 。
(1)甲醇脱氢法可制备甲醛,反应方程式为CH3OH⇌HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,该反应为

②下列方法中能加快反应速率的是
a.使用催化剂 b.升高温度 c.降低反应物浓度
(2)甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为

②探测仪工作时,电子从
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】结合所学内容回答下列问题:
Ⅰ.某实验小组以H2O2的分解为例,研究浓度、催化剂、温度对化学反应速率的影响,按照如下方案设计实验。
(1)实验①和②的目的是研究_______________ 对反应速率的影响。
(2)实验③和④测得生成氧气的体积随时间变化的关系如下图所示。

分析上图能够得出的实验结论是________________________________________________ 。
(3)实验⑤和⑥是研究温度相差10℃对反应速率的影响,请在上面表格空白处补齐对应的内容_________ 。
Ⅱ.某温度时,在2L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(4)反应开始至2 min,Z的平均反应速率____________ 。
(5)保持容器容积不变,在第2min时改变下列条件时,化学反应速率的变化是:
①向其中充入1 molX气体,化学反应速率_______ (填 “加快”“减慢”或“不变”,下同);
②向其中充入1 mol N2(g) (N2不参加反应),化学反应速率_______________ ;
③同时加入0.9molX、0.7molY 和0.2molZ,化学反应速率________________ 。
Ⅰ.某实验小组以H2O2的分解为例,研究浓度、催化剂、温度对化学反应速率的影响,按照如下方案设计实验。
| 实验编号 | 反应物 | 催化剂 | 温度 |
| ① | 10 mL 2% H2O2溶液 | 无 | 20℃ |
| ② | 10 mL 5% H2O2溶液 | 无 | 20℃ |
| ③ | 10 mL 5% H2O2溶液 | 1-2滴1 mol/LFeCl3溶液 | 20℃ |
| ④ | 10 mL 5% H2O2溶液 | 无 | 20℃ |
| ⑤ | 10 mL 5% H2O2溶液 | ||
| ⑥ | 无 | 20℃ |
(2)实验③和④测得生成氧气的体积随时间变化的关系如下图所示。

分析上图能够得出的实验结论是
(3)实验⑤和⑥是研究温度相差10℃对反应速率的影响,请在上面表格空白处补齐对应的内容
Ⅱ.某温度时,在2L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(4)反应开始至2 min,Z的平均反应速率
(5)保持容器容积不变,在第2min时改变下列条件时,化学反应速率的变化是:
①向其中充入1 molX气体,化学反应速率
②向其中充入1 mol N2(g) (N2不参加反应),化学反应速率
③同时加入0.9molX、0.7molY 和0.2molZ,化学反应速率
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”,某小组设计了如下方案:先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
(1)已知H2C2O4与KMnO4反应产生MnSO4和CO2。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4)∶n(KMnO4)≥________ 。
(2)探究温度对反应速率影响的实验编号是___________ (填编号,下同),探究反应物浓度对反应速率影响的实验编号是____________ 。
(3)不同温度下c(MnO4-)随反应时间t的变化曲线如图所示,判断T1_________ T2(填“>”或“<”)

| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)已知H2C2O4与KMnO4反应产生MnSO4和CO2。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4)∶n(KMnO4)≥
(2)探究温度对反应速率影响的实验编号是
(3)不同温度下c(MnO4-)随反应时间t的变化曲线如图所示,判断T1

您最近一年使用:0次
【推荐1】氢能作为一种清洁高效的二次能源,在未来能源格局中发挥着重要作用。
已知:常温下,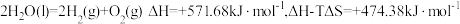 。
。
(1)将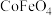 负载在
负载在 上,产氧温度在1200℃,产氢温度在1000℃时,可顺利实现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑温度变化对反应
上,产氧温度在1200℃,产氢温度在1000℃时,可顺利实现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑温度变化对反应 的影响。
的影响。
第Ⅰ步: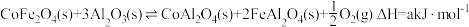
第Ⅱ步: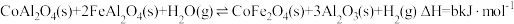
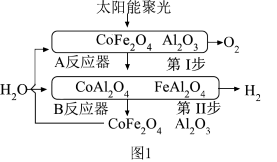
①a+b___________ 285.84(填“>”“<”或“=”)
②第Ⅱ步反应的 分别为正、逆反应速率常数,仅与温度有关。1000℃时,在体积为1L的B反应器中加入
分别为正、逆反应速率常数,仅与温度有关。1000℃时,在体积为1L的B反应器中加入 发生上述反应测得
发生上述反应测得 和
和 物质的量浓度随时间的变化如图2所示,则60min内,
物质的量浓度随时间的变化如图2所示,则60min内,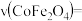
___________ g/min (保留2位小数)。a点时
___________ (填最简整数比);
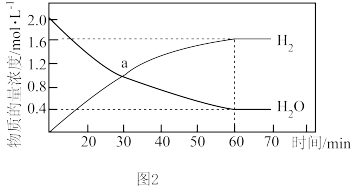
平衡时,体系压强为10kPa,则Kp=___________ 。
(2)一氧化碳与氢气的反应历程如图,其中吸附在催化剂表面上的物种用*标注。
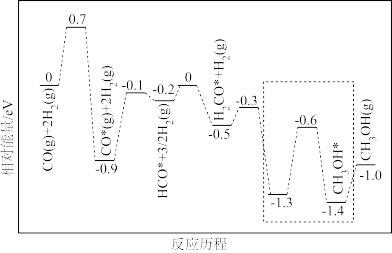
①该反应历程中控速步骤的能垒为___________ eV。
②写出虚线框内发生的化学反应方程式___________ 。
(3)热力学铜氯循环制氢法分电解、水解、热解三步进行。
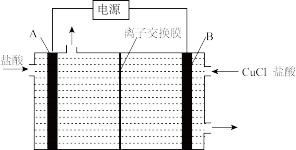
电解:
水解: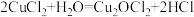
热解: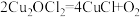
已知:CuCl为白色固体,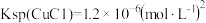 。
。
电解装置如图所示,则A为___________ 极(填“阳”或“阴”),B极电极反应为___________ 。
已知:常温下,
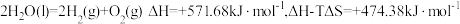 。
。(1)将
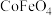 负载在
负载在 上,产氧温度在1200℃,产氢温度在1000℃时,可顺利实现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑温度变化对反应
上,产氧温度在1200℃,产氢温度在1000℃时,可顺利实现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑温度变化对反应 的影响。
的影响。第Ⅰ步:
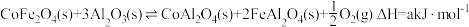
第Ⅱ步:
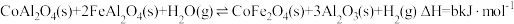

①a+b
②第Ⅱ步反应的
 分别为正、逆反应速率常数,仅与温度有关。1000℃时,在体积为1L的B反应器中加入
分别为正、逆反应速率常数,仅与温度有关。1000℃时,在体积为1L的B反应器中加入 发生上述反应测得
发生上述反应测得 和
和 物质的量浓度随时间的变化如图2所示,则60min内,
物质的量浓度随时间的变化如图2所示,则60min内,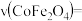
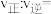

平衡时,体系压强为10kPa,则Kp=
(2)一氧化碳与氢气的反应历程如图,其中吸附在催化剂表面上的物种用*标注。

①该反应历程中控速步骤的能垒为
②写出虚线框内发生的化学反应方程式
(3)热力学铜氯循环制氢法分电解、水解、热解三步进行。

电解:

水解:
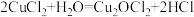
热解:
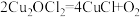
已知:CuCl为白色固体,
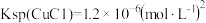 。
。电解装置如图所示,则A为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】在一个容积不变的密闭容器中发生如下反应:CO(g)+H2O(g)  CO2(g)+ H2(g),其平衡常数(K)和温度(t)的关系如下表所示。
CO2(g)+ H2(g),其平衡常数(K)和温度(t)的关系如下表所示。
请填写下列空白。
(1)该反应的平衡常数表达式为K=___________ ;该反应为___________ 反应。(填“吸热”或“放热”)
(2)在700℃时,向容器中充入1 mol CO、3 mol H2O,保持温度不变,反应达到平衡后,其平衡常数___________ 1.67(填“大于”“小于”或“等于”)。
(3)800℃时,某时刻反应混合物中CO、H2O、CO2、H2的浓度分别为1mol/L、1mol/L、2mol/L、 2mol/L。此时上述反应平衡移动方向为___________ 。(填“正反应方向” “逆反应方向”或“不移动”)
(4)若题(3)的体系达平衡状态时,CO的物质的浓度为___________ mol/L
 CO2(g)+ H2(g),其平衡常数(K)和温度(t)的关系如下表所示。
CO2(g)+ H2(g),其平衡常数(K)和温度(t)的关系如下表所示。| t/℃ | 700 | 800 | 1000 | 1200 |
| K | 1.67 | 1.0 | 0.58 | 0.38 |
请填写下列空白。
(1)该反应的平衡常数表达式为K=
(2)在700℃时,向容器中充入1 mol CO、3 mol H2O,保持温度不变,反应达到平衡后,其平衡常数
(3)800℃时,某时刻反应混合物中CO、H2O、CO2、H2的浓度分别为1mol/L、1mol/L、2mol/L、 2mol/L。此时上述反应平衡移动方向为
(4)若题(3)的体系达平衡状态时,CO的物质的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】空间站内搭载萨巴蒂尔装置将 转化为
转化为 ,再通过电解水装置回收氧元素.其系统原理如图:
,再通过电解水装置回收氧元素.其系统原理如图:
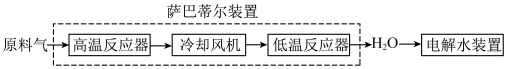
萨巴蒂尔装置内发生反应为
反应Ⅰ: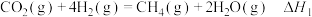
反应Ⅱ: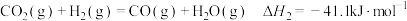
(1)已知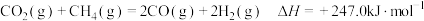 ,则
,则
_________ .
(2)在“高温反应器”中以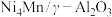 为催化剂,一段时间内不同温度
为催化剂,一段时间内不同温度 转化率如图.已知反应Ⅰ的速率方程:
转化率如图.已知反应Ⅰ的速率方程: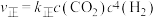 ,
, .
.
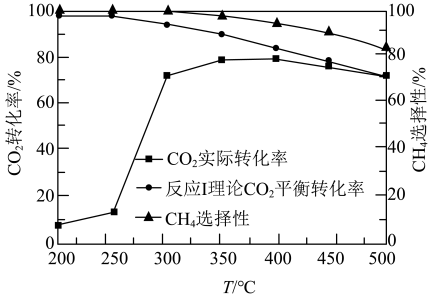
①250℃前, 实际转化率随温度变化不大的主要原因是
实际转化率随温度变化不大的主要原因是___________ .
②300℃时
__________ 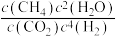 (填“>”“<”或“=”).
(填“>”“<”或“=”).
③达到平衡后,升高温度, 增大的倍数
增大的倍数_________  增大的倍数(填“>”“<”或“=”).
增大的倍数(填“>”“<”或“=”).
(3)在“低温反应器”中达平衡时,各组分物质的量分数随温度变化如图.已知原料气中含有 及
及 .
.
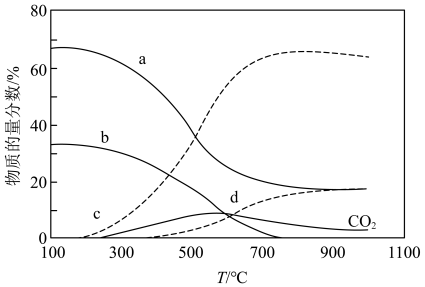
① 物质的量分数随温度变化的曲线为
物质的量分数随温度变化的曲线为____________ (填标号).
②300~500℃, 物质的量分数随温度升高而上升的原因是
物质的量分数随温度升高而上升的原因是___________ .
③某温度下达平衡时,总压为 ,剩余
,剩余 和
和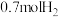 ,则反应Ⅰ的
,则反应Ⅰ的 为
为___________ (列出计算式, 为以分压表示的平衡常数,分压=总压×物质的量分数);
为以分压表示的平衡常数,分压=总压×物质的量分数);
此时氧元素的回收率为____________ [回收率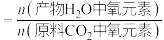 ].
].
(4)从平衡与速率角度分析萨巴蒂尔装置采用高温和低温反应器串联的优点是___________ .
 转化为
转化为 ,再通过电解水装置回收氧元素.其系统原理如图:
,再通过电解水装置回收氧元素.其系统原理如图:
萨巴蒂尔装置内发生反应为
反应Ⅰ:
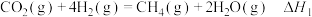
反应Ⅱ:
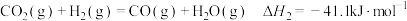
(1)已知
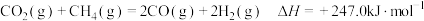 ,则
,则
(2)在“高温反应器”中以
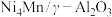 为催化剂,一段时间内不同温度
为催化剂,一段时间内不同温度 转化率如图.已知反应Ⅰ的速率方程:
转化率如图.已知反应Ⅰ的速率方程: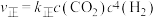 ,
, .
.
①250℃前,
 实际转化率随温度变化不大的主要原因是
实际转化率随温度变化不大的主要原因是②300℃时

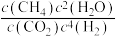 (填“>”“<”或“=”).
(填“>”“<”或“=”).③达到平衡后,升高温度,
 增大的倍数
增大的倍数 增大的倍数(填“>”“<”或“=”).
增大的倍数(填“>”“<”或“=”).(3)在“低温反应器”中达平衡时,各组分物质的量分数随温度变化如图.已知原料气中含有
 及
及 .
.
①
 物质的量分数随温度变化的曲线为
物质的量分数随温度变化的曲线为②300~500℃,
 物质的量分数随温度升高而上升的原因是
物质的量分数随温度升高而上升的原因是③某温度下达平衡时,总压为
 ,剩余
,剩余 和
和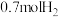 ,则反应Ⅰ的
,则反应Ⅰ的 为
为 为以分压表示的平衡常数,分压=总压×物质的量分数);
为以分压表示的平衡常数,分压=总压×物质的量分数);此时氧元素的回收率为
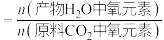 ].
].(4)从平衡与速率角度分析萨巴蒂尔装置采用高温和低温反应器串联的优点是
您最近一年使用:0次



