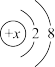已知1-20号元素中A、B、C、D、E、F、G元素原子质子数依次增大,A的某种同位素可用于考古测定文物年代;C最外层电子数是次外层的3倍;D的阳离子是同周期元素形成的阳离子中半径最大的,E的阳离子为同周期中最小的;F最高正价与最低负价代数和为6;G的原子核外K、M层电子数之和等于L、N层电子数之和,试推断:
(1)元素的名称:B_______ D______ G在周期表中的位置_____
(2)写出含有10个中子的C元素的原子符号________
(3)B、E、F、G形成的简单离子的半径由大到小排序__________ (用元素符号表示)
(4)在A、B元素各自形成的氢化物中,稳定性较差的氢化物的化学式为____ ,原因为是_____ ;其氢化物中沸点较高的化学式为________ ,原因是______ 。
(5)C可与氢元素形成四核18电子的物质,其电子式为______ ,含有的化学键类型_____ 。
(6)E的最高价氧化物对应的水化物可与G的最高价氧化物对应的水化物发生反应的离子方程式为____ 。
(7)D与周期表中非金属性最强的元素可形成化合物X,用电子式表示X的形成过程_______ 。
(1)元素的名称:B
(2)写出含有10个中子的C元素的原子符号
(3)B、E、F、G形成的简单离子的半径由大到小排序
(4)在A、B元素各自形成的氢化物中,稳定性较差的氢化物的化学式为
(5)C可与氢元素形成四核18电子的物质,其电子式为
(6)E的最高价氧化物对应的水化物可与G的最高价氧化物对应的水化物发生反应的离子方程式为
(7)D与周期表中非金属性最强的元素可形成化合物X,用电子式表示X的形成过程
18-19高一下·内蒙古·期中 查看更多[1]
(已下线)内蒙古第一机械制造(集团)有限公司第一中学2018-2019高一下学期期中考试化学试卷
更新时间:2019-05-24 11:12:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有X、Y、Z、T、W五种短周期元素,原子序数依次增大。X与T同主族,且X元素与其它元素不在同一周期。Y、Z在同周期中处于相邻位置,它们的单质在通常状况下均为无色气体。W原子的最外层电子数是核外电子层数的2倍。请回答:
(1)Z在周期表中的位置为_______________ 。
(2)写出X与Z形成的10电子阴离子的化学式___________ 。
(3)W的一种氧化物具有漂白性,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式____________________________ 。
(4)化合物T2Z2的电子式为____________ ,其阴阳离子个数比为______________ 。
(1)Z在周期表中的位置为
(2)写出X与Z形成的10电子阴离子的化学式
(3)W的一种氧化物具有漂白性,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式
(4)化合物T2Z2的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)z在元素周期表中的位置是_______ 。
(2)写出化合物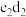 的电子式:
的电子式:_______ ,将少量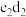 投入水中,剧烈反应,写出反应的化学方程式:
投入水中,剧烈反应,写出反应的化学方程式:_______ 。
(3)g与h的简单氢化物的稳定性由强到弱的顺序为_______ (用化学式表示)。
(4)d、e、f、g这四种元素分别形成的简单离子,离子半径由小到大的顺序是_______ (用离子符号表示)。
(5)e和f两元素相比较,金属性较强的是_______ (填元素符号),请设计一个实验验证该结论(简要描述实验步骤和现象):_______ 。

(1)z在元素周期表中的位置是
(2)写出化合物
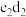 的电子式:
的电子式: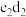 投入水中,剧烈反应,写出反应的化学方程式:
投入水中,剧烈反应,写出反应的化学方程式:(3)g与h的简单氢化物的稳定性由强到弱的顺序为
(4)d、e、f、g这四种元素分别形成的简单离子,离子半径由小到大的顺序是
(5)e和f两元素相比较,金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数_____ ; ②第3周期元素的最高化合价____ ;
③F-、 Na+ 、Mg2+、Al3+的离子半径___ ;

(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是________________________ 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为_________ ,B的化学式是_______ 。
③Z与Y形成的稳定化合物的电子式为__________ 。
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:________________________________ ;该反应中转移的电子数目为______ 。
①ⅡA族元素的最外层电子数
③F-、 Na+ 、Mg2+、Al3+的离子半径

(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为
③Z与Y形成的稳定化合物的电子式为
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】几种主族元素在周期表中的位置如下,根据上表回答下列问题:
(1)⑥元素的简单氢化物是______________________ (填化学式)。
(2)①③⑦三种元素原子半径由大到小的顺序是_______________ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为______ ,该元素在周期表中的位置是______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_________ (填化学式),①与水反应的化学方程式为________________ 。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是______ (填字母,下同)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是______ 。(填A或B或C)
A. B.
B.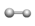 C.
C.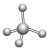
族 周期 | IA | 0 | ||||||
1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ⑤ | ⑥ | ||||||
3 | ① | ③ | ⑦ | |||||
4 | ② | ⑧ |
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是
A.
 B.
B.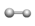 C.
C.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,根据表中8种元素,用元素符号等化学用语填空。
(1)①~⑧元素中,金属性最强的是___________  写元素符号
写元素符号 。
。
(2)①~⑧元素中,画出最稳定的元素的原子结构示意图___________ 。
(3)②、③、⑥所形成的简单离子,其半径由大到小的顺序是___________  写离子符号
写离子符号 。
。
(4)将 铁粉和氧化铁的混合物中加入
铁粉和氧化铁的混合物中加入 的稀硫酸,恰好完全反应,放出氢气
的稀硫酸,恰好完全反应,放出氢气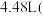 标准状况
标准状况 反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
①发生的化学反应中有一个属于化合反应,写出其离子方程式___________ 。
②混合物中氧化铁是___________ g。
③原稀硫酸的物质的量浓度___________  。
。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 写元素符号
写元素符号 。
。(2)①~⑧元素中,画出最稳定的元素的原子结构示意图
(3)②、③、⑥所形成的简单离子,其半径由大到小的顺序是
 写离子符号
写离子符号 。
。(4)将
 铁粉和氧化铁的混合物中加入
铁粉和氧化铁的混合物中加入 的稀硫酸,恰好完全反应,放出氢气
的稀硫酸,恰好完全反应,放出氢气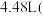 标准状况
标准状况 反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:①发生的化学反应中有一个属于化合反应,写出其离子方程式
②混合物中氧化铁是
③原稀硫酸的物质的量浓度
 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知X、Y、Z、W、Q是原子序数依次增大的前四周期元素。X原子核外有6种不同运动状态的电子;Y基态原子中s电子总数与p电子总数相等;Z最高价氧化物对应水化物的碱性在同周期元素中最强;W基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反。
(1)基态X原子中电子占据的最高能级的原子轨道形状为_______ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为_______ 。
(2)Y、Z、W的简单离子半径由大到小的顺序为_______ 。(用离子符号表示)
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为_______ 。
②检验溶液中是否含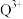 离子的试剂是
离子的试剂是_______ (填化学式),现象为_______ 。
③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是_______ (填字母序号)。
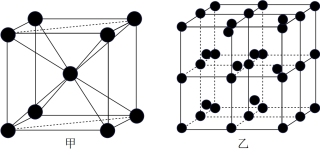
A.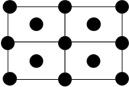 B.
B.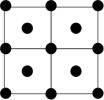 C.
C.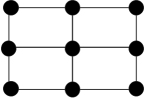 D.
D.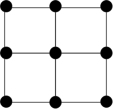
(1)基态X原子中电子占据的最高能级的原子轨道形状为
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态X原子,其核外电子自旋磁量子数的代数和为(2)Y、Z、W的简单离子半径由大到小的顺序为
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为
②检验溶液中是否含
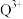 离子的试剂是
离子的试剂是③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是

A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。A、B、C、D、E五种元素的电负性分别为2.1,3.5,1.5,2.5,0.8,请回答下列问题:
(1)A是_______ ,B是_______ ,C是_______ ,D是_______ ,E是_______ (用化学符号填空,下同)。
(2)由电负性判断,以上五种元素中金属性最强的是_______ ,非金属性最强的是_______ 。
(3)当B与A、C、D分别形成化合物时,B显_______ 价(填“正”或“负”或“零”,下同),其他元素显_______ 价。
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是_______ (填化学式)。
(1)A是
(2)由电负性判断,以上五种元素中金属性最强的是
(3)当B与A、C、D分别形成化合物时,B显
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知a、b、c、d、e、f均为短周期主族元素,且它们的原子序数依次增大。a、b在元素周期表中处于相邻的位置,b和e同主族,c在同周期主族元素中原子半径最大,a、d的最外层电子数之和等于d的次外层电子数,e的最外层电子数是电子层数的2倍。请回答下列问题:
(1)f在元素周期表中的位置是___________ 。
(2)b、c、e的简单离子的半径由大到小的顺序为___________ (用具体微粒符号表示)。a、e、f的最高价氧化物对应的水化物中酸性最强的是___________ (填化学式)。
(3)a的气态氢化物与其最高价氧化物对应的水化物反应,生成的化合物中所含的化学键类型有:___________ 。
(4)加热条件下,b的单质与c的单质的反应产物的电子式为___________ 。
(5)d、f组成的化合物为M,c的最高价氧化物对应的水化物为N,M的溶液与足量N的溶液反应的离子方程式为___________ 。
(6)b、e组成的离子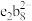 具有强氧化性,向含
具有强氧化性,向含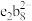 的盐溶液中滴入
的盐溶液中滴入 溶液,混合溶液会变紫红色。写出反应的离子方程式:
溶液,混合溶液会变紫红色。写出反应的离子方程式:___________ 。
(1)f在元素周期表中的位置是
(2)b、c、e的简单离子的半径由大到小的顺序为
(3)a的气态氢化物与其最高价氧化物对应的水化物反应,生成的化合物中所含的化学键类型有:
(4)加热条件下,b的单质与c的单质的反应产物的电子式为
(5)d、f组成的化合物为M,c的最高价氧化物对应的水化物为N,M的溶液与足量N的溶液反应的离子方程式为
(6)b、e组成的离子
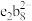 具有强氧化性,向含
具有强氧化性,向含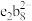 的盐溶液中滴入
的盐溶液中滴入 溶液,混合溶液会变紫红色。写出反应的离子方程式:
溶液,混合溶液会变紫红色。写出反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素及其化合物知识在工农业生产、生活中被广泛使用,造福人类。
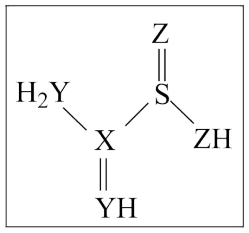
I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为___________ ,该漂白剂所含元素非金属性最强的元素是在元素周期表中的位置为___________ 。
(2)下列说法错误的是___________(选填序号)。
Ⅱ.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为___________ 。图中该氢化物转化为甲的化学方程式___________ 。化合物丁中Y元素的质量分数为___________ %。
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为___________ 。该氢化物与丙的浓溶液反应,出现淡黄色浑浊且有刺激性气体放出。每生成1摩尔沉淀时,转移的电子数目为___________ 。

I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为
(2)下列说法错误的是___________(选填序号)。
| A.原子半径:X>Y>Z | B.简单气态氢化物稳定性:Y<Z |
| C.沸点:H2Z<H2S | D.该化合物中所有原子均为8电子稳定结构 |
Ⅱ.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到淡黄色固态化合物,D的M层电子数为K层电子数的3倍.试根据以上叙述回答:
(1)写出元素名称:A_____ D_____ ;
(2)画出D的原子结构示意图____________ ;
(3)用电子式表示化合物C2D的形成过程___________________ .
(1)写出元素名称:A
(2)画出D的原子结构示意图
(3)用电子式表示化合物C2D的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有四种元素A、B、C、D,其中B2-离子与C+离子核外都有二个电子层,B原子的质子数与C原子的质子数之和等于D原子的质子数,A原子失去一个电子后变成一个质子,试回答:
(1)A、B、C、D的元素符号分别为_______ 、______ 、_______ 、_______ 。
(2)B2-的电子式为_________ ,D原子的原子结构示意图为__________ ,C+离子的结构示意图为____________ 。
(3)写出与C+具有相同电子数的五种分子(化学式):________ 、______ 、______ 、________ 、_________ 。
(1)A、B、C、D的元素符号分别为
(2)B2-的电子式为
(3)写出与C+具有相同电子数的五种分子(化学式):
您最近一年使用:0次