(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数_____ ; ②第3周期元素的最高化合价____ ;
③F-、 Na+ 、Mg2+、Al3+的离子半径___ ;

(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是________________________ 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为_________ ,B的化学式是_______ 。
③Z与Y形成的稳定化合物的电子式为__________ 。
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:________________________________ ;该反应中转移的电子数目为______ 。
①ⅡA族元素的最外层电子数
③F-、 Na+ 、Mg2+、Al3+的离子半径

(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为
③Z与Y形成的稳定化合物的电子式为
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:
10-11高一·江苏泰州·期中 查看更多[1]
(已下线)2011-2012学年江苏省泰州中学高三化学期中化学试卷
更新时间:2016-12-09 02:19:11
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.现有下列4种重要的有机物:
① ②
② ③
③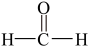 ④
④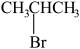
请回答:
(1)能与苯酚缩合成高分子化合物的是__________ 。(填序号)。
(2)能使酸性高锰酸钾溶液褪色的是__________ 。(填序号)。
(3)写出④在一定条件下发生消去反应的化学方程式__________ 。
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌_____ 。(填“锌块”或“铜块”)
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是______ 。(用离子方程式表示)
(3)自来水常用氯气杀菌消毒,Cl2+H2O⇌HCl+HClO,要增大HClO的浓度,可以加入下列物质中的__________ 。
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH−)=______ mol·L-1。
①
 ②
② ③
③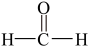 ④
④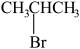
请回答:
(1)能与苯酚缩合成高分子化合物的是
(2)能使酸性高锰酸钾溶液褪色的是
(3)写出④在一定条件下发生消去反应的化学方程式
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是
(3)自来水常用氯气杀菌消毒,Cl2+H2O⇌HCl+HClO,要增大HClO的浓度,可以加入下列物质中的
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH−)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】T℃下的某溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示。请回答下列问题:
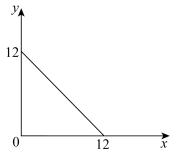
(1)此温度下,水的离子积Kw=________ ,则T________ 25(填“ ”“
”“ ”或
”或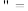 )。
)。
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示:
假设溶液混合前后的体积变化忽略不计,则a=________ ,实验②中由水电离产生的c(OH-)=________ mol/L。
(3)在此温度下,将0.1mol/L的NaHSO4溶液与0.1mol/L的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
①按丁方式混合后,所得溶液显________ 性(填“酸”“碱”或“中”)。
②写出按乙方式混合后,反应的离子方程式:________ 。
③按甲方式混合后,所得溶液的pH为________ 。
(4)在25℃下,将amol/L的NaCN溶液与0.01mol/L的盐酸等体积混合,反应后测得溶液pH=7,则a________ (填“ ”“
”“ ”或“
”或“ ”)0.01。
”)0.01。

(1)此温度下,水的离子积Kw=
 ”“
”“ ”或
”或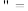 )。
)。(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示:
| 实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则a=
(3)在此温度下,将0.1mol/L的NaHSO4溶液与0.1mol/L的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
| 甲 | 乙 | 丙 | 丁 | |
| 0.1mol/L的Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
| 0.1mol/L NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显
②写出按乙方式混合后,反应的离子方程式:
③按甲方式混合后,所得溶液的pH为
(4)在25℃下,将amol/L的NaCN溶液与0.01mol/L的盐酸等体积混合,反应后测得溶液pH=7,则a
 ”“
”“ ”或“
”或“ ”)0.01。
”)0.01。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)某温度(t℃)时,水的离子积KW=1×10-12mol2•L-2,则该温度_______ 。(填“>”、“<”或“=”)25℃,其理由是_______ 。
(2)该温度下,c水(H+)=1×10﹣7mol•L﹣1的溶液中只存在NaOH溶质,则由H2O电离出来的c水(OH—)=_______ mol•L﹣1。
(3)实验室用Zn和稀硫酸反应制取H2,反应时溶液中水的电离平衡_______ (填“向左”、“向右”或“不”,下同)移动;在新制氯水中加入少量NaCl固体,水的电离平衡_______ 移动。
(4)25℃时,0.1mol•L﹣1的下列4种溶液,水电离出的c水(H+)由大到小的关系是_______ 。(填序号)
①盐酸 ②H2SO4 ③NaOH ④Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度_______ pH=10的Ba(OH)2溶液中水的电离程度(填“大于”、“等于”或 “小于”)。
(1)某温度(t℃)时,水的离子积KW=1×10-12mol2•L-2,则该温度
(2)该温度下,c水(H+)=1×10﹣7mol•L﹣1的溶液中只存在NaOH溶质,则由H2O电离出来的c水(OH—)=
(3)实验室用Zn和稀硫酸反应制取H2,反应时溶液中水的电离平衡
(4)25℃时,0.1mol•L﹣1的下列4种溶液,水电离出的c水(H+)由大到小的关系是
①盐酸 ②H2SO4 ③NaOH ④Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】10种短周期主族元素a-j的原子半径、最高正价、最低负价随着原子序数的递增变化如下图所示。

回答下列问题:
(1)元素e在元素周期表中的位置是_______ 。
(2)元素d、e、f形成的简单离子半径由小到大的顺序是_______ (用离子符号表示)。
(3)下列事实能说明j的非金属性强于i的是_______(填标号)。
(4)由a、c、d三种元素组成的化合物一定含有的化学键类型为_______ 。
(5)甲是元素b的氢化物,含有18个电子。用甲、氧气和f的最高价氧化物对应水化物的溶液设计成燃料电池,负极的电极反应式为_______ 。
(6)乙是元素i的低价气态氧化物,丙是由d、f、j按原子个数比1∶1∶1组成的化合物。工业上常用丙和NaOH的混合溶液吸收乙,该反应的离子方程式为_______ 。

回答下列问题:
(1)元素e在元素周期表中的位置是
(2)元素d、e、f形成的简单离子半径由小到大的顺序是
(3)下列事实能说明j的非金属性强于i的是_______(填标号)。
| A.单质与氢气化合的难易程度:i难于j |
| B.简单阴离子的还原性:i强于j |
| C.简单氢化物的沸点:i高于j |
| D.含氧酸的酸性:j强于i |
(5)甲是元素b的氢化物,含有18个电子。用甲、氧气和f的最高价氧化物对应水化物的溶液设计成燃料电池,负极的电极反应式为
(6)乙是元素i的低价气态氧化物,丙是由d、f、j按原子个数比1∶1∶1组成的化合物。工业上常用丙和NaOH的混合溶液吸收乙,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)g元素的离子结构示意图为___________ ;元素y的一种质子数与中子数相同的核素符号为___________ 。
(2)元素z与x元素形成一种离子zx ,检验某溶液中含该离子的方法是
,检验某溶液中含该离子的方法是___________ 。
(3)e和f两元素相比较,金属性较强是___________ (填元素符号),可以证明该结论的实验是___________ 。
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.比较这两种元素的气态氢化物的稳定性
C.将相同大小的这两种元素单质分别放入冷水中,观察反应现象
D.比较物质的量相同的这两种元素的单质与酸反应时失电子的数目
(4)z、d、e、f元素分别形成的简单离子中离子半径由大到小的顺序是___________ (填离子符号)。
(5)e2g4是离子化合物,各原子均满足8电子稳定结构,则e2g4的电子式为___________ ,z2x4的结构式为___________ ,fh3溶液和e2g溶液混合反应的离子方程式为___________ 。

(1)g元素的离子结构示意图为
(2)元素z与x元素形成一种离子zx
 ,检验某溶液中含该离子的方法是
,检验某溶液中含该离子的方法是(3)e和f两元素相比较,金属性较强是
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.比较这两种元素的气态氢化物的稳定性
C.将相同大小的这两种元素单质分别放入冷水中,观察反应现象
D.比较物质的量相同的这两种元素的单质与酸反应时失电子的数目
(4)z、d、e、f元素分别形成的简单离子中离子半径由大到小的顺序是
(5)e2g4是离子化合物,各原子均满足8电子稳定结构,则e2g4的电子式为
您最近一年使用:0次
【推荐3】现有a,b、c、d、e五种前四周期的元素,它们的原子序数依次增大,请根据下列相关信息,回答问题:
(1)元素a的名称是_______ ,c在元素周期表中的位置是_______ ,a2c的空间构型为_______ 。
(2)d元素基态原子中最高能层符号是_______ ,核外电子的空间运动状态有_______ 种。
(3)e元素处于周期表的_______ 区,价层电子的轨道表达式为_______ 。
(4)元素a,b、d的电负性由大到小的顺序是_______ (用元素符号表示,下同);元素c,d、e的第一电离能由大到小的顺序是_______ 。
(5)元素b、c、d的最高价氧化物的水化物酸性由强到弱的顺序是_______ (用化学式表示)。
| a | 基态原子的核外电子数等于电子层数 |
| b | 基态原子的核外s电子是p电子的2倍 |
| c | 最高正价与最低负价的代数和为4 |
| d | 基态原子的价层电子排布式为:(n+1)sn(n+1)pn+3 |
| e | 基态原子中未成对电子数是本周期中最多的元素 |
(2)d元素基态原子中最高能层符号是
(3)e元素处于周期表的
(4)元素a,b、d的电负性由大到小的顺序是
(5)元素b、c、d的最高价氧化物的水化物酸性由强到弱的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用相应的化学用语回答下列问题:
(1)③的单质的电子式为_______ ,结构式为_______ 。
(2)④、⑥、⑧的原子半径由小到大的顺序为_______ (用元素符号作答)。
(3)金属性最强的是_______ ,非金属性最强的是_______ ,(用元素符号答)②、③、⑨的最高价氧化物的水化物的酸性由弱到强的顺序是_______ (用化学式答)。
(4)写出⑦元素的最高价氧化物对应水化物分别与元素⑥的最高价氧化物对应水化物的水溶液反应的离子方程式_______ 。
(5)①和④形成的气态氢化物与①和⑧形成的气态氢化物相比较,_______ 的稳定性强;_______ 的沸点高(填化学式),理由是_______ 。
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)④、⑥、⑧的原子半径由小到大的顺序为
(3)金属性最强的是
(4)写出⑦元素的最高价氧化物对应水化物分别与元素⑥的最高价氧化物对应水化物的水溶液反应的离子方程式
(5)①和④形成的气态氢化物与①和⑧形成的气态氢化物相比较,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)z在元素周期表中的位置是_______ 。
(2)写出化合物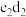 的电子式:
的电子式:_______ ,将少量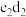 投入水中,剧烈反应,写出反应的化学方程式:
投入水中,剧烈反应,写出反应的化学方程式:_______ 。
(3)g与h的简单氢化物的稳定性由强到弱的顺序为_______ (用化学式表示)。
(4)d、e、f、g这四种元素分别形成的简单离子,离子半径由小到大的顺序是_______ (用离子符号表示)。
(5)e和f两元素相比较,金属性较强的是_______ (填元素符号),请设计一个实验验证该结论(简要描述实验步骤和现象):_______ 。

(1)z在元素周期表中的位置是
(2)写出化合物
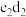 的电子式:
的电子式: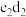 投入水中,剧烈反应,写出反应的化学方程式:
投入水中,剧烈反应,写出反应的化学方程式:(3)g与h的简单氢化物的稳定性由强到弱的顺序为
(4)d、e、f、g这四种元素分别形成的简单离子,离子半径由小到大的顺序是
(5)e和f两元素相比较,金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,a~k分别代表10种元素,请回答:
(1)元素a~k中,其简单氢化物最稳定的是_____ (填元素符号)。
(2)b的简单氢化物的结构式_____ 。
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是_____ (填离子符号)。
(4)写出两种由c原子和e原子构成的化合物的电子式_____ 。
(5)元素h、i的最高价氧化物对应水化物中酸性较强的是_____ (填化学式)。
(6)写出84号元素在元素周期表中的位置_____ 。
(7)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是_____ 。
(8)下列说法能证明金属性k强于f的是_____ (填序号)。
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
| a | ||||||||
| b | c | d | ||||||
| e | f | g | h | i | ||||
| k | …… | |||||||
(2)b的简单氢化物的结构式
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是
(4)写出两种由c原子和e原子构成的化合物的电子式
(5)元素h、i的最高价氧化物对应水化物中酸性较强的是
(6)写出84号元素在元素周期表中的位置
(7)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是
(8)下列说法能证明金属性k强于f的是
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知有A、B、C、D、E五种微粒:
①A微粒核内有12个中子,核外M电子层上有1个电子;
②B微粒得到2个电子后,其电子层结构与Ne相同;
③C微粒带有2个单位的正电荷,核电荷数为12;
④D微粒核外有18个电子,当失去2个电子时呈电中性;
⑤E微粒不带电,其质量数为1。
(1)请写出各微粒的符号:A___________ 、B___________ 、C___________ 、D___________ 、E___________ ;
(2)上述五种微粒中,半径最大的是___________ ;
(3)A、B和E三种元素所形成的化合物的晶体中含有的化学键有___________ ,该化合物的电子式___________ 。
①A微粒核内有12个中子,核外M电子层上有1个电子;
②B微粒得到2个电子后,其电子层结构与Ne相同;
③C微粒带有2个单位的正电荷,核电荷数为12;
④D微粒核外有18个电子,当失去2个电子时呈电中性;
⑤E微粒不带电,其质量数为1。
(1)请写出各微粒的符号:A
(2)上述五种微粒中,半径最大的是
(3)A、B和E三种元素所形成的化合物的晶体中含有的化学键有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下面是八种短周期元素的相关信息(已知Be的原子半径为0.089nm)
F原子中无中子,G最高正价与负价绝对值相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色。
(1)B元素在元素周期表中的位置___________ ;B形成的简单离子的结构示意图___________
(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是___________ (填化学式)。
(3)用电子式表示C,H形成化合物的过程___________
(4)H,E形成原子个数比为1:1的化合物中所含化学键类型为___________ 。
(5)F与C和F与E均能形成18个电子的化合物,这两种化合物发生反应可生成C,其反应的化学方程式为:___________ ;
(6)A,B,C,E所形成的简单离子半径由大到小的顺序为(离子符号表示)___________
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,﹣2 | ﹣1 | ﹣2 |
(1)B元素在元素周期表中的位置
(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是
(3)用电子式表示C,H形成化合物的过程
(4)H,E形成原子个数比为1:1的化合物中所含化学键类型为
(5)F与C和F与E均能形成18个电子的化合物,这两种化合物发生反应可生成C,其反应的化学方程式为:
(6)A,B,C,E所形成的简单离子半径由大到小的顺序为(离子符号表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,针对表中的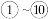 元素,用元素符号或化学式填空回答以下问题:
元素,用元素符号或化学式填空回答以下问题:
(1)元素①、②的简单氢化物中的稳定性最强的是_______  用化学式表示
用化学式表示 ;
;
(2)元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ ,元素③的最高价氧化物对应水化物中含有的化学键类型为_______ ;
(3)在③④⑤⑦四种元素中,简单离子半径最小的是_______ ;
(4) 的电子式为
的电子式为_______ ; 的电子式为
的电子式为_______ ;
(5)在⑦与⑩的单质中,氧化性较强的是_______ ,用化学反应方程式证明:_______ 。
 元素,用元素符号或化学式填空回答以下问题:
元素,用元素符号或化学式填空回答以下问题: |  |  | 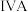 | 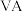 | 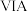 | 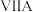 |  | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 用化学式表示
用化学式表示 ;
;(2)元素的最高价氧化物对应的水化物中酸性最强的是
(3)在③④⑤⑦四种元素中,简单离子半径最小的是
(4)
 的电子式为
的电子式为 的电子式为
的电子式为(5)在⑦与⑩的单质中,氧化性较强的是
您最近一年使用:0次



