工业上生产环氧乙烷的反应为:2 CH2=CH2 (g) + O2 (g) = 2 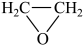 (g) ∆H = -106 kJ • mol−1,其反应机理如下:
(g) ∆H = -106 kJ • mol−1,其反应机理如下:
①Ag + O2=AgO2慢
②CH2=CH2+ AgO2 = + AgO 快
+ AgO 快
③CH2= CH2 + 6AgO =2CO2 + 2H2O + 6Ag 快
下列有关该反应的说法正确的是
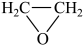 (g) ∆H = -106 kJ • mol−1,其反应机理如下:
(g) ∆H = -106 kJ • mol−1,其反应机理如下:①Ag + O2=AgO2慢
②CH2=CH2+ AgO2 =
 + AgO 快
+ AgO 快③CH2= CH2 + 6AgO =2CO2 + 2H2O + 6Ag 快
下列有关该反应的说法正确的是
| A.反应的活化能等于 106 kJ·mol−1 |
| B.工业上生产环氧乙烷的反应是一个焓减熵增的反应,所以能自发进行 |
| C.增大乙烯浓度能显著提高环氧乙烷的生成速率 |
| D.理论上 0.7 mol 乙烯参与反应最多可得到 0.6 mol 环氧乙烷 |
更新时间:2020-10-31 15:46:26
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列涉及化学学科观点的有关说法正确的是

| A.微粒观:二氧化硫是由硫原子和氧原子构成的 |
| B.转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和 |
| C.守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g |
| D.结构观:金刚石和石墨由于结构中碳原子的排列方式不同,物理性质存在着较大的差异 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】MnO2催化某反应的一种催化机理如图所示。下列叙述不正确的是
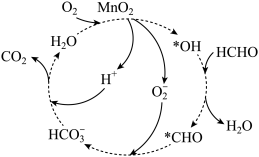

| A.催化过程中,所发生的反应均为氧化还原反应 |
B.该反应的化学方程式可表示为:HCHO+O2 CO2+H2O CO2+H2O |
C. 为中间产物之一,该微粒与KO2中所含阴离子种类相同 为中间产物之一,该微粒与KO2中所含阴离子种类相同 |
| D.CO2的结构式为O=C=O |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】一定条件下的密闭容器中发生反应: ,若其他条件不变,下列措施会使该反应速率减小的是
,若其他条件不变,下列措施会使该反应速率减小的是
 ,若其他条件不变,下列措施会使该反应速率减小的是
,若其他条件不变,下列措施会使该反应速率减小的是| A.升高温度 | B.减小压强 | C.增大 浓度 浓度 | D.加入催化剂 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关化学反应速率说法中正确的是
| A.实验室用H2O2分解制O2,加热后反应速率无明显变化 |
| B.在金属钠与足量水反应中,增加水的量能加快反应速率 |
| C.在恒容容器中发生2SO2+O2 ⇌2SO3反应,充入一定量He能加快反应速率 |
| D.实验室用碳酸钙和盐酸反应制取CO2,用粉末状碳酸钙比块状碳酸钙反应要快 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列推论正确的是( )
| A.S(g)+O2(g)=SO2(g)△H1,S(s)+O2(g)=SO2(g)△H2;则△H1>△H2 |
| B.C(石墨,s)=C(金刚石,s)△H=+1.9kJ/mol,则金刚石比石墨稳定 |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4kJ/mol,则中和热为57.4kJ/mol |
| D.CaCO3(s)=CaO(s)+CO2(g)△H>0,△S>0,则该反应任何温度下都能自发进行 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法中正确的是
| A.凡是放热反应都是自发的,吸热反应都是非自发的 |
| B.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的∆S<0 |
| C.使用催化剂可降低反应的∆H和反应的活化能,从而提高化学反应速率 |
| D.升高温度,可使单位体积内活化分子数增多,反应速率加快 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】乙烯是重要的有机化工原料,广泛用于合成乙醇、乙醛、乙酸等;乙烯直接氧化制乙酸的反应为CH2=CH2(g)+O2(g) CH3COOH(g)ΔΗ。实验室可用加热乙醇和浓硫酸混合物至170℃时反应制取乙烯。下列有关乙烯直接氧化制乙酸反应的说法正确的是
CH3COOH(g)ΔΗ。实验室可用加热乙醇和浓硫酸混合物至170℃时反应制取乙烯。下列有关乙烯直接氧化制乙酸反应的说法正确的是
 CH3COOH(g)ΔΗ。实验室可用加热乙醇和浓硫酸混合物至170℃时反应制取乙烯。下列有关乙烯直接氧化制乙酸反应的说法正确的是
CH3COOH(g)ΔΗ。实验室可用加热乙醇和浓硫酸混合物至170℃时反应制取乙烯。下列有关乙烯直接氧化制乙酸反应的说法正确的是| A.反应中投入1molO2和1molCH2=CH2,反应结束转移电子的数目约等于4×6.02×1023 |
| B.反应的ΔΗ=E(C−C)+4E(C−H)−E(C=O)−E(C−O)−E(O−H)(E表示键能) |
| C.一定温度下,反应可以自发进行,该反应的ΔH<0 |
| D.反应使用高效选择性催化剂,可以提高CH2=CH2的平衡转化率 |
您最近半年使用:0次

 的硫酸溶液反应,一定温度下,为了加快反应的速率,又不影响产生H2的总量,可向反应物中加入适量的
的硫酸溶液反应,一定温度下,为了加快反应的速率,又不影响产生H2的总量,可向反应物中加入适量的

