铁黄是一种重要的颜料,化学式为Fe2O3·xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如下:
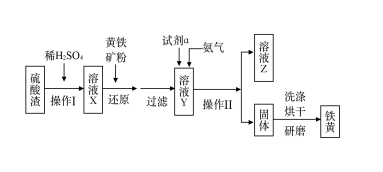
(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是______________ 、________________ 。
(2)试剂a最好选用__________________ (供选择使用的有:铝粉、空气、浓HNO3);
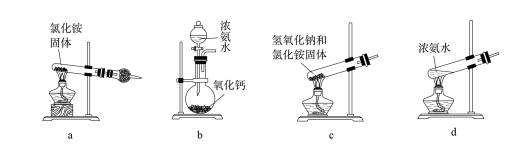
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是_____ (填序号)。
(4)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。
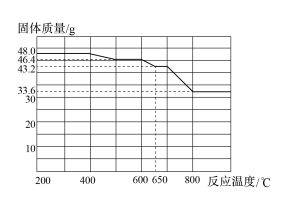
根据图像推断670℃时Fe2O3还原产物的化学式为_________ ,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论)_____________________________
仪器自选。可供选择的试剂:稀硫酸、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。

(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是
(2)试剂a最好选用
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是

(4)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。

根据图像推断670℃时Fe2O3还原产物的化学式为
仪器自选。可供选择的试剂:稀硫酸、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。
更新时间:2020-10-31 16:23:14
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O),其实验方案如下:

请回答下列问题:
(1)操作I的名称______ 。
(2)写出滤液A到生成滤液C的离子方程式为_____ 。
(3)小组成员经过检测,发现制得的绿矾不纯。经分析原因:要想由沉淀I最终制得纯度较高的绿矾,改进方法为____ 。
(4)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2可以使B溶解,则该反应的化学方程式为___ 。
(5)有同学提出可将方案中最初溶解合金的盐酸改为烧碱溶液,重新设计方案,也能最终制得三种物质,老师认为后者方案相对于前者方案更合理,其理由是____ 。

请回答下列问题:
(1)操作I的名称
(2)写出滤液A到生成滤液C的离子方程式为
(3)小组成员经过检测,发现制得的绿矾不纯。经分析原因:要想由沉淀I最终制得纯度较高的绿矾,改进方法为
(4)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2可以使B溶解,则该反应的化学方程式为
(5)有同学提出可将方案中最初溶解合金的盐酸改为烧碱溶液,重新设计方案,也能最终制得三种物质,老师认为后者方案相对于前者方案更合理,其理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】实验室用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备硫酸亚铁晶体,设计流程如下:
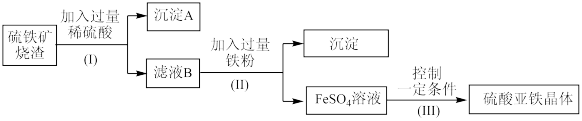
(1)步骤(I)中分离溶液和沉淀的操作是_______ ,该操作中用到的玻璃仪器有玻璃棒、烧杯和_______ 。
(2)沉淀A的主要成分是_______ 。
(3)滤液B中的阳离子有H+、Fe2+和_______ 。
(4)写出步骤(Ⅱ)中Fe3+和Fe反应生成Fe2+的离子方程式:_______ 。

(1)步骤(I)中分离溶液和沉淀的操作是
(2)沉淀A的主要成分是
(3)滤液B中的阳离子有H+、Fe2+和
(4)写出步骤(Ⅱ)中Fe3+和Fe反应生成Fe2+的离子方程式:
您最近一年使用:0次
【推荐1】CdS又称镉黄,可用作黄色颜料,也用于制备荧光粉等。以镉铁矿(主要成分为CdO2、Fe2O3、FeO及少量的Al2O3和SiO2)为原料制备CdS的工艺流程如图:

回答下列问题。
(1)“还原镉”时,产生能使澄清石灰水变浑浊的气体,发生反应的离子方程式为___________
(2)加入H2O2溶液的目的是___________ 。
(3)通入H2S也可以“沉镉”,发生反应的离子方程式为___________ 。
(4)CdS不溶于稀盐酸,可溶于浓盐酸,并生成H2[CdCl4],反应的化学方程式为___________

回答下列问题。
(1)“还原镉”时,产生能使澄清石灰水变浑浊的气体,发生反应的离子方程式为
(2)加入H2O2溶液的目的是
(3)通入H2S也可以“沉镉”,发生反应的离子方程式为
(4)CdS不溶于稀盐酸,可溶于浓盐酸,并生成H2[CdCl4],反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】酸亚铁作为补血剂,可促进动物的生长发育,增强抗病能力。以钛白副产绿矾(成分为 )为原料制备绿矾(
)为原料制备绿矾( )的工艺流程如下:
)的工艺流程如下:
(1)写出两条可提高“酸浸”效率的措施:___________ 。
(2)“酸浸”过程,矿渣中的 与稀
与稀 反应的离子方程式为
反应的离子方程式为___________ 。
(3)检验“酸浸”后的溶液中是否含 常用的试剂是
常用的试剂是___________ 。
(4)“还原”时溶液中含铁物质发生反应的化学方程式为___________ 。
(5)“一系列操作”包括___________ 、洗涤、干燥。干燥时温度不宜过高,其原因是___________ 。
(6)绿矾晶体在空气中易被氧化。取xg样品,加水完全溶解,用酸化的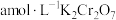 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液bmL。反应原理:
溶液bmL。反应原理: 。则绿矾晶体纯度的计算式为
。则绿矾晶体纯度的计算式为___________ ( 摩尔质量为
摩尔质量为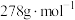 )
)
 )为原料制备绿矾(
)为原料制备绿矾( )的工艺流程如下:
)的工艺流程如下:
(1)写出两条可提高“酸浸”效率的措施:
(2)“酸浸”过程,矿渣中的
 与稀
与稀 反应的离子方程式为
反应的离子方程式为(3)检验“酸浸”后的溶液中是否含
 常用的试剂是
常用的试剂是(4)“还原”时溶液中含铁物质发生反应的化学方程式为
(5)“一系列操作”包括
(6)绿矾晶体在空气中易被氧化。取xg样品,加水完全溶解,用酸化的
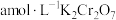 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液bmL。反应原理:
溶液bmL。反应原理: 。则绿矾晶体纯度的计算式为
。则绿矾晶体纯度的计算式为 摩尔质量为
摩尔质量为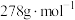 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯乙酮(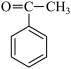 )广泛用于皂用香精中,可由苯和乙酸酐(
)广泛用于皂用香精中,可由苯和乙酸酐(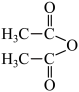 )在氯化铝的催化作用下制备。
)在氯化铝的催化作用下制备。
| 名称 | 熔点/℃ | 沸点/℃ | 密度/(g·mL-1) | 溶解性 |
| 苯 | 5.5 | 80.1 | 0.88 | 不溶于水,易溶于有机溶剂 |
| 苯乙酮 | 19.6 | 203 | 1.03 | 微溶于水,易溶于有机溶剂 |
| 乙酸酐 | -73 | 139 | 1.08 | 遇水反应,易溶于有机溶剂 |
| 乙酸 | 16.6 | 118 | 1.05 | 易溶于水,易溶于有机溶剂 |
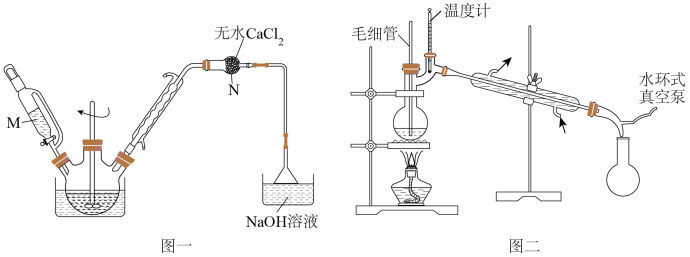
步骤Ⅱ冷却后将反应物倒入100g冰水中,有白色胶状沉淀Al(OH)3生成,采用合适的方法处理,水层用苯萃取,合并苯层溶液,再依次用30mL5%NaOH溶液和30mL水洗涤,分离出的苯层。
步骤Ⅲ:苯层用无水硫酸镁干燥,蒸馏回收苯,再收集产品苯乙酮。
(1)仪器M的名称为
(2)步骤Ⅰ三颈烧瓶中发生反应的化学方程式为
(3)根据上述实验药品的用量,三颈烧瓶的最适宜规格为_____(填标号)。
| A.100mL | B.250mL | C.500mL | D.1000mL |
(5)本实验为收集产品用了减压蒸馏装置,如图二所示,其中毛细管的作用是
A.202℃ B.220℃ C.175℃
(6)实验中收集到24.0mL苯乙酮,则苯乙酮的产率为
(7)已知:
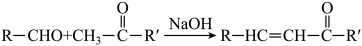 。苯乙酮(
。苯乙酮(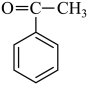 )和苯甲醛(
)和苯甲醛(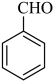 )在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
)在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】高纯硫酸锰为合成镍钴锰三元正极材料的原料,工业上可由软锰矿浆(主要成分是MnO2)吸收含硫废渣产生的废气制备,其工艺流程如图所示。

已知:①浸出液的pH <2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。
②生成氢氧化物沉淀的pH如表所示:
请回答下列问题:
(1)“高温焙烧”前需将矿石研成粉末,其目的是_______ 。
(2)“氧化”中添加适量的MnO2的作用是_______ (用离子方程式表示);写出“沉锰”的离子方程式是_______ 。
(3)下列各组试剂中,能准确测定尾气中SO2含量的是_______ 。(填序号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液 c.碘水、淀粉溶液 d.氨水、酚酞试液
(4)滤渣的主要成分有_______ 。
(5)室温下,除去MnSO4溶液中的Fe3+、Al3+,需调节溶液pH范围为_______ 。
(6)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是_______ (用字母填空)。
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.干燥

已知:①浸出液的pH <2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。
②生成氢氧化物沉淀的pH如表所示:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
| 开始沉淀时的pH | 3.4 | 6.3 | 1.5 | 7.1 |
| 沉淀完全时的pH | 4.7 | 8.3 | 3.0 | 9.8 |
(1)“高温焙烧”前需将矿石研成粉末,其目的是
(2)“氧化”中添加适量的MnO2的作用是
(3)下列各组试剂中,能准确测定尾气中SO2含量的是
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液 c.碘水、淀粉溶液 d.氨水、酚酞试液
(4)滤渣的主要成分有
(5)室温下,除去MnSO4溶液中的Fe3+、Al3+,需调节溶液pH范围为
(6)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.干燥
您最近一年使用:0次
【推荐2】硼及其化合物在工业、医药、农业等部门有许多用途。某工厂以铁硼精矿(主要成分为B2O3·2MgO,还有SiO2、CaO、FeO等杂质)制取制硼酸、金属镁的工艺流程图为:
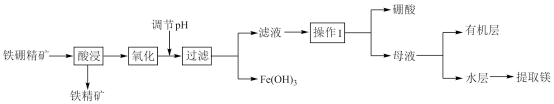
已知:硼酸在不同温度下的溶解度:
回答下列问题:
(1)使用盐酸酸浸,过程中主要反应的化学方程式为_________ ,为提高浸出速率,可采取的措施有_________ (写出两条)。
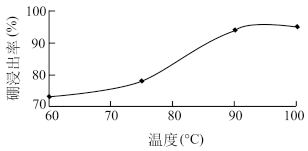
(2)酸浸时,温度与硼浸出率的关系如图所示,则合适的酸浸温度为_________ 。
(3)浸出液“氧化”的是将溶液中的Fe2+用_______ 试剂氧化为Fe3+,反应的离子方程式为_________ 。
(4)从滤液中获得H3BO3晶体的“操作I”具体操作是_________ 。
(5)向滤液中加入有机萃取剂萃取分液,此时硼酸处于_________ 层中(填“有机”或“无机”)。实验室模拟萃取操作使用的玻璃仪器除烧杯外,另一主要玻璃仪器是_________ 。
(6)某工厂用 m1 kg的铁硼精矿制备硼酸,得到纯度为99.8%的硼酸m2 kg,则铁硼精矿中硼的质量分数是__________ (列式表达)。

已知:硼酸在不同温度下的溶解度:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度(g/100g水) | 3 | 3 | 5 | 7 | 9 | 11 | 15 | 18 | 23 | 29 |
(1)使用盐酸酸浸,过程中主要反应的化学方程式为
(2)酸浸时,温度与硼浸出率的关系如图所示,则合适的酸浸温度为

(3)浸出液“氧化”的是将溶液中的Fe2+用
(4)从滤液中获得H3BO3晶体的“操作I”具体操作是
(5)向滤液中加入有机萃取剂萃取分液,此时硼酸处于
(6)某工厂用 m1 kg的铁硼精矿制备硼酸,得到纯度为99.8%的硼酸m2 kg,则铁硼精矿中硼的质量分数是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】黄铁矿石是制取硫酸的主要原料,主要成分为FeS2和少量FeS(假设其它杂质中不含铁、硫元素,且高温下不发生化学变化)。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为4FeS2+11O2=2Fe2O3+8SO2,4FeS+7O2=2Fe2O3+4SO2
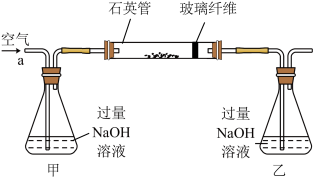
(1)鼓人空气的作用是___________ ,锥形瓶乙中NaOH溶液的作用是___________ 。
【实验一】测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:
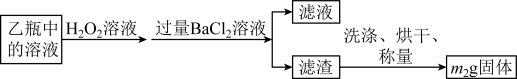
(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是___________ (用化学方程式表示)。
(3)洗涤滤渣的方法是______________________ 。
(4)该黄铁矿石中硫元素的质量分数为___________ (列出表达式即可)。
【实验二】测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣;②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤;③将滤液稀释至250mL;④取25.00mL稀释液,用0.1000mol·L-1的酸性KMnO4溶液滴定,三次滴定实验,平均消耗酸性KMnO4溶液25.00mL。
(5)操作②中用铁粉作还原剂,测定铁的含量___________ (填“偏高”或“偏低”或“不变”),操作④中滴定时酸性KMnO4溶液盛装在___________ 填“酸式滴定管”或“碱式滴定管”),③中稀释液中Fe2+的物质的量浓度c(Fe2+)=___________ 。

(1)鼓人空气的作用是
【实验一】测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:

(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是
(3)洗涤滤渣的方法是
(4)该黄铁矿石中硫元素的质量分数为
【实验二】测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣;②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤;③将滤液稀释至250mL;④取25.00mL稀释液,用0.1000mol·L-1的酸性KMnO4溶液滴定,三次滴定实验,平均消耗酸性KMnO4溶液25.00mL。
(5)操作②中用铁粉作还原剂,测定铁的含量
您最近一年使用:0次




