A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的简单气态氢化物的水溶液呈碱性,C、E同主族,形成的化合物 是形成酸雨的主要物质之一。请回答下列问题:
是形成酸雨的主要物质之一。请回答下列问题:
(1)F在元素周期表中的位置为_________ 。
(2)D2E溶液在空气中长期放置会发生反应,生成物之一为H。H与 的结构和化学性质相似,其溶液显黄色。写出
的结构和化学性质相似,其溶液显黄色。写出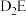 溶液在空气中长期放置生成H的化学方程式:
溶液在空气中长期放置生成H的化学方程式:___________ 。H溶液与稀硫酸反应产生的现象为_______________ 。
(3)化学家发现一种化学式为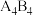 的离子化合物,一定条件下
的离子化合物,一定条件下 熔融
熔融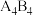 电离生成两种离子各
电离生成两种离子各 ,则该物质熔融时的电离方程式为
,则该物质熔融时的电离方程式为______________ 。
(4)向 某浓度由A、B、C、D中的三种元素形成的一元强碱溶液中通入
某浓度由A、B、C、D中的三种元素形成的一元强碱溶液中通入 气体后得溶液M,因
气体后得溶液M,因 通入量的不同,溶液M的组成也不同。若向溶液M中逐滴加入
通入量的不同,溶液M的组成也不同。若向溶液M中逐滴加入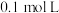 盐酸,产生的气体体积
盐酸,产生的气体体积 与加入盐酸的体积[V(盐酸)]的关系有如图所示两种情况(不计
与加入盐酸的体积[V(盐酸)]的关系有如图所示两种情况(不计 的溶解)。
的溶解)。
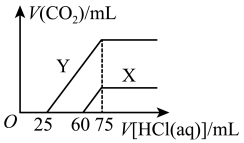
①原一元强碱溶液的物质的量浓度为________  。
。
②由曲线X、Y可知,两次实验通入的 体积之比为
体积之比为__________ 。
 是形成酸雨的主要物质之一。请回答下列问题:
是形成酸雨的主要物质之一。请回答下列问题:(1)F在元素周期表中的位置为
(2)D2E溶液在空气中长期放置会发生反应,生成物之一为H。H与
 的结构和化学性质相似,其溶液显黄色。写出
的结构和化学性质相似,其溶液显黄色。写出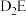 溶液在空气中长期放置生成H的化学方程式:
溶液在空气中长期放置生成H的化学方程式:(3)化学家发现一种化学式为
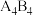 的离子化合物,一定条件下
的离子化合物,一定条件下 熔融
熔融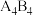 电离生成两种离子各
电离生成两种离子各 ,则该物质熔融时的电离方程式为
,则该物质熔融时的电离方程式为(4)向
 某浓度由A、B、C、D中的三种元素形成的一元强碱溶液中通入
某浓度由A、B、C、D中的三种元素形成的一元强碱溶液中通入 气体后得溶液M,因
气体后得溶液M,因 通入量的不同,溶液M的组成也不同。若向溶液M中逐滴加入
通入量的不同,溶液M的组成也不同。若向溶液M中逐滴加入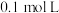 盐酸,产生的气体体积
盐酸,产生的气体体积 与加入盐酸的体积[V(盐酸)]的关系有如图所示两种情况(不计
与加入盐酸的体积[V(盐酸)]的关系有如图所示两种情况(不计 的溶解)。
的溶解)。
①原一元强碱溶液的物质的量浓度为
 。
。②由曲线X、Y可知,两次实验通入的
 体积之比为
体积之比为
更新时间:2020-10-10 14:50:57
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】乙二酸(H2C2O4)俗名草酸,是一种有还原性的有机二元弱酸,在化学上有广泛应用。为测定某乙二酸样品的纯度,实验步骤如下:
①准确称量5.000g乙二酸样品,配成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,加入少量硫酸酸化,用0.1000mol·L-1KMnO4溶液滴定至草酸恰好全部氧化成二氧化碳,共消耗KMnO4溶液20.00mL(杂质不与KMnO4溶液反应)。
回答下列问题:
(1)写出草酸的电离方程式_______ 。
(2)KMnO4标准液应装入_______ (填“酸式”或“碱式”)滴定管,理由是_______ 。
(3)KMnO4溶液滴定草酸过程中发生反应的离子方程为_______ ,滴定终点的现象为_______ 。
(4)计算此样品的纯度为_______ 。
(5)下列操作会导致测定结果偏高的是_______ (填字母)。
a.未用KMnO4标准溶液润洗滴定管
b.滴定前锥形瓶内有少量水
c.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
d.观察读数时,滴定前仰视,滴定后俯视
①准确称量5.000g乙二酸样品,配成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,加入少量硫酸酸化,用0.1000mol·L-1KMnO4溶液滴定至草酸恰好全部氧化成二氧化碳,共消耗KMnO4溶液20.00mL(杂质不与KMnO4溶液反应)。
回答下列问题:
(1)写出草酸的电离方程式
(2)KMnO4标准液应装入
(3)KMnO4溶液滴定草酸过程中发生反应的离子方程为
(4)计算此样品的纯度为
(5)下列操作会导致测定结果偏高的是
a.未用KMnO4标准溶液润洗滴定管
b.滴定前锥形瓶内有少量水
c.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
d.观察读数时,滴定前仰视,滴定后俯视
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】分类法是进行化学研究的重要方法。不同的标准可以把物质及化学反应分为不同的类别。现有以下物质:①固体氢氧化钠②熔化的铁块③CaCO3④Fe(OH)3胶体⑤NaHSO4溶液⑥干冰⑦盐酸⑧蔗糖
(1)以上物质中能导电的是_______ (填序号,下同),属于电解质是_______ 。
(2)④⑤的微观本质区别是_______ 。
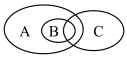
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,采用的分类方法名称是_______ ,其中表示离子反应的是_______ (填字母)。
(4)有同学认为所有强酸、强碱之间的中和反应均可表示为OH-+H+=H2O,请举个例子反驳上述观点(用离子方程式表示)_______ 。
(5)将过量的⑥放入①的溶液中充分反应,然后将反应后的溶液分成两等份,分别加入足量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:①_______ 。②_______ 。
(1)以上物质中能导电的是
(2)④⑤的微观本质区别是
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,采用的分类方法名称是

(4)有同学认为所有强酸、强碱之间的中和反应均可表示为OH-+H+=H2O,请举个例子反驳上述观点(用离子方程式表示)
(5)将过量的⑥放入①的溶液中充分反应,然后将反应后的溶液分成两等份,分别加入足量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:①
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。
(1)室温下,测得0.1 mol/L H2C2O4溶液的pH=1.3,写出草酸的电离方程式_______ 。
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如图所示:
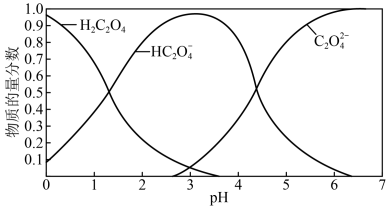
①向草酸溶液中滴加KOH溶液至pH=2.5,该过程中发生的主要反应的离子方程式是_______ 。
②草酸的二级电离平衡常数Ka2的数量级是______ (填选项)。
A. 10-2 B. 10-3 C.10-4 D.10-5
③0.1 mol/LKHC2O4溶液中,下列粒子浓度关系正确的是_______ (填选项)。
A.c(K+)+c(H+)=c( )+c(
)+c( )+c(OH-)
)+c(OH-)
B.c(K+)>c( )>c(
)>c( )>c(H2C2O4)
)>c(H2C2O4)
C. c(K+)= c( )+c(
)+c( )+c(H2C2O4)
)+c(H2C2O4)
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2++ H2C2O4+ xH2O FeC2O4∙xH2O +2H+
FeC2O4∙xH2O +2H+
①制备时需添加氨水以提高FeC2O4∙xH2O的产率,从化学产衡移动原理角度解释原因:_______ 。
②测定草酸亚铁晶体(FeC2O4∙xH2O)的x值,实验如下:称取1.8000g草酸亚铁晶体溶于一定浓度的硫酸中,用 KMnO4酸性溶液滴定。到达滴定终点时,消耗0.3000 mol/L的KMnO4酸性溶液20.00 mL。已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+。计算可得 FeC2O4∙xH2O中x=_______ (已知:M(FeC2O4)= 144 g/mol)。
(1)室温下,测得0.1 mol/L H2C2O4溶液的pH=1.3,写出草酸的电离方程式
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如图所示:

①向草酸溶液中滴加KOH溶液至pH=2.5,该过程中发生的主要反应的离子方程式是
②草酸的二级电离平衡常数Ka2的数量级是
A. 10-2 B. 10-3 C.10-4 D.10-5
③0.1 mol/LKHC2O4溶液中,下列粒子浓度关系正确的是
A.c(K+)+c(H+)=c(
 )+c(
)+c( )+c(OH-)
)+c(OH-)B.c(K+)>c(
 )>c(
)>c( )>c(H2C2O4)
)>c(H2C2O4)C. c(K+)= c(
 )+c(
)+c( )+c(H2C2O4)
)+c(H2C2O4) (3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2++ H2C2O4+ xH2O
 FeC2O4∙xH2O +2H+
FeC2O4∙xH2O +2H+①制备时需添加氨水以提高FeC2O4∙xH2O的产率,从化学产衡移动原理角度解释原因:
②测定草酸亚铁晶体(FeC2O4∙xH2O)的x值,实验如下:称取1.8000g草酸亚铁晶体溶于一定浓度的硫酸中,用 KMnO4酸性溶液滴定。到达滴定终点时,消耗0.3000 mol/L的KMnO4酸性溶液20.00 mL。已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+。计算可得 FeC2O4∙xH2O中x=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】过碳酸钠( ,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用
,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用 和
和 采用“醇析法”制取过碳酸钠晶体的工艺流程如下:
采用“醇析法”制取过碳酸钠晶体的工艺流程如下: 极易溶于水,难溶于乙醇。
极易溶于水,难溶于乙醇。
回答下列问题:
(1)“控温 反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式
反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式___________ 。
(2)“操作a”的名称是___________ ,完成此操作需要的玻璃仪器有烧杯、玻璃棒和___________ ;“洗涤”所用试剂为___________ 。
(3)查阅资料知过碳酸钠在水溶液中氧化性更强,原因是 与
与 反应转化为氧化性更强的
反应转化为氧化性更强的 。写出过碳酸钠溶液中产生
。写出过碳酸钠溶液中产生 的离子方程式
的离子方程式___________ 。
(4)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:称量 样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为
样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为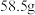 。
。
①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式___________ ;
②该样品中过碳酸钠的质量分数为___________ (保留小数点后一位)。
 ,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用
,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用 和
和 采用“醇析法”制取过碳酸钠晶体的工艺流程如下:
采用“醇析法”制取过碳酸钠晶体的工艺流程如下: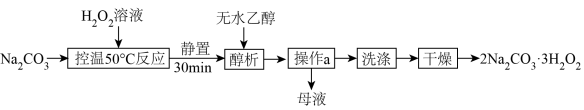
 极易溶于水,难溶于乙醇。
极易溶于水,难溶于乙醇。回答下列问题:
(1)“控温
 反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式
反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式(2)“操作a”的名称是
(3)查阅资料知过碳酸钠在水溶液中氧化性更强,原因是
 与
与 反应转化为氧化性更强的
反应转化为氧化性更强的 。写出过碳酸钠溶液中产生
。写出过碳酸钠溶液中产生 的离子方程式
的离子方程式(4)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:称量
 样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为
样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为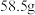 。
。①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式
②该样品中过碳酸钠的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为金属单质,C是一种强碱。请按要求填空:
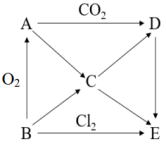
(1)写出下列物质的化学式:A_______ ,E_______ 。
(2)写出物质D的任意两种用途_______ 。
(3)写出B→C的化学方程式,并用双线桥分析,在双线桥上标出电子转移的方向和数目:_______ 。

(1)写出下列物质的化学式:A
(2)写出物质D的任意两种用途
(3)写出B→C的化学方程式,并用双线桥分析,在双线桥上标出电子转移的方向和数目:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为测定氢氧化钠和碳酸钠固体混合物样品中碳酸钠的质量分数,甲、乙两位同学分别设计了如下实验方案:
Ⅰ.甲同学的方案是:将m g样品溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称得固体为n g。
(1)混合物中碳酸钠的质量分数为_____ (用m、n表示),甲同学洗涤沉淀的具体操作是_____ 。
(2)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是①________ ;②BaCO3的摩尔质量比CaCO3的大,与等质量的Na2CO3反应,Ba2+产生沉淀的质量大,称量误差小。
Ⅱ.乙同学的方案的实验装置如图所示:
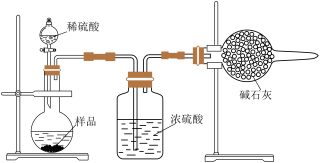
(1)盛有浓硫酸的装置的作用是______ 。
(2)乙同学的方案的装置中存在一定的缺陷,请你提出改进的方法:______ (简单叙述做法,不必画图)。
Ⅰ.甲同学的方案是:将m g样品溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称得固体为n g。
(1)混合物中碳酸钠的质量分数为
(2)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是①
Ⅱ.乙同学的方案的实验装置如图所示:

(1)盛有浓硫酸的装置的作用是
(2)乙同学的方案的装置中存在一定的缺陷,请你提出改进的方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某小组报探究 和
和 性质:
性质:
【实验一】 和
和 的溶解性和水溶液的酸碱性
的溶解性和水溶液的酸碱性
根据上述实验现象,回答下列问题:
(1)常温下, 的溶解度
的溶解度___________ (填“大于”“小于”或“等于”) 的溶解度。
的溶解度。
(2)下列推断正确的是___________(填字母)。
(3) 溶液和少量盐酸反应生成
溶液和少量盐酸反应生成 ,离子方程式为
,离子方程式为______ 。
【实验二】 和
和 的热稳定性
的热稳定性
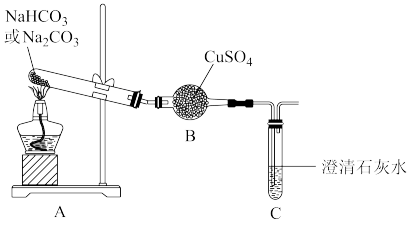
观察到实验现象如下表所示:
根据上述实验现象,回答下列问题:
(4)加热 时,装置C中产生气泡的原因是
时,装置C中产生气泡的原因是___________ 。
(5)实验结论是___________ 。
(6)加热 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
【实验三】探究 溶液、
溶液、 溶液分别与溶液反应。
溶液分别与溶液反应。
步骤1:在2ml 溶液、2ml
溶液、2ml 溶液分别滴加溶液,都产生白色沉淀,后者有少量气泡。
溶液分别滴加溶液,都产生白色沉淀,后者有少量气泡。
步骤2:加热热饱和 溶液,产生大量气泡。
溶液,产生大量气泡。
(7)加热 溶液产生气泡是
溶液产生气泡是___________ (填化学式);写出 溶液和
溶液和 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
 和
和 性质:
性质:【实验一】
 和
和 的溶解性和水溶液的酸碱性
的溶解性和水溶液的酸碱性| 步骤 | 实验操作 | 观察到的实验现象 | |
 |  | ||
| ① | 在2支试管里分别加入1g 和1g 和1g ,各加入10mL水,振荡 ,各加入10mL水,振荡 | 全部溶解,得到透明溶液 | 部分溶解,试管底部有少证固体 |
| ② | 将步骤①的试管中溶液分别分成两份,其中1份溶液中各滴加2滴酚酞溶液 | 溶液变红色 | 溶液变浅红色 |
| ③ | 在步骤②的另两份溶液中各滴加2滴10%盐酸,振荡 | 没有气泡产生 | 产生少量气泡 |
(1)常温下,
 的溶解度
的溶解度 的溶解度。
的溶解度。(2)下列推断正确的是___________(填字母)。
| A.碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性 |
| B.碳酸钠溶液、碳酸氢钠溶液都呈碱性 |
| C.碳酸钠溶液、碳酸氢钠溶液都呈酸性 |
| D.碳酸钠溶液呈碱性,碳酸氢钠溶液呈中性 |
 溶液和少量盐酸反应生成
溶液和少量盐酸反应生成 ,离子方程式为
,离子方程式为【实验二】
 和
和 的热稳定性
的热稳定性
观察到实验现象如下表所示:
| 物质 | 装置B中现象 | 装置C中现象 |
 | 无明显变化 | 开始断断续续产生气泡,一会儿后,,没有气泡,溶液保持澄清 |
 | 白色粉末变蓝色 | 开始断断续续产生气泡,一会儿后,产生连续气泡,溶液变浑浊 |
(4)加热
 时,装置C中产生气泡的原因是
时,装置C中产生气泡的原因是(5)实验结论是
(6)加热
 发生反应的化学方程式为
发生反应的化学方程式为【实验三】探究
 溶液、
溶液、 溶液分别与溶液反应。
溶液分别与溶液反应。步骤1:在2ml
 溶液、2ml
溶液、2ml 溶液分别滴加溶液,都产生白色沉淀,后者有少量气泡。
溶液分别滴加溶液,都产生白色沉淀,后者有少量气泡。步骤2:加热热饱和
 溶液,产生大量气泡。
溶液,产生大量气泡。(7)加热
 溶液产生气泡是
溶液产生气泡是 溶液和
溶液和 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】品牌膨松剂中发挥作用的物质为碳酸氢钠。某化学兴趣小组利用下列有关装置,加热该膨松剂样品,通过放出气体的量来检验其品质。
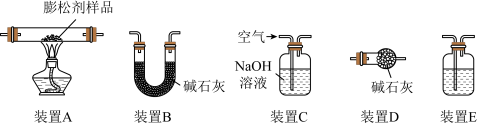
(1)装置D仪器的名称是_________ 。
(2)装置E中所盛试剂为____________ ,其作用是______________ 。
(3)装置的连接顺序为_____________ (填装置序号)。
(4)实验过程中,装置A中发生反应的化学方程式为________________ 。
(5)实验过程中必须向装置内通入空气,装置C的作用是除去空气中的________ (填化学式)。加热前,通入一段时间空气的具体操作为________________________ 。
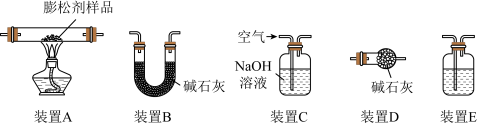
(1)装置D仪器的名称是
(2)装置E中所盛试剂为
(3)装置的连接顺序为
(4)实验过程中,装置A中发生反应的化学方程式为
(5)实验过程中必须向装置内通入空气,装置C的作用是除去空气中的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】我国制碱工业先驱侯德榜发明了侯氏制碱法。其模拟流程如图:
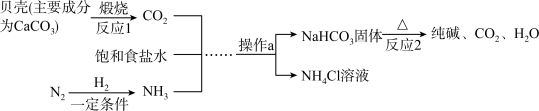
回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:________ 。
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:_________ 。
(3)进行操作a时所需的玻璃仪器有玻璃棒、________ 和________ 。
(4)NaHCO3固体受热分解的化学方程式为_______ 。
(5)现有ag质量分数为w的NH4Cl溶液(不考虑 与水发生的反应):
与水发生的反应):
①该溶液中所含溶质的总质量为________ (用含a、w的代数式表示,写出计算式即可)g。
②________ gNH3中所含的氮元素的总质量与该溶液中所含的氮元素的总质量相等。

回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:
(3)进行操作a时所需的玻璃仪器有玻璃棒、
(4)NaHCO3固体受热分解的化学方程式为
(5)现有ag质量分数为w的NH4Cl溶液(不考虑
 与水发生的反应):
与水发生的反应):①该溶液中所含溶质的总质量为
②
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A元素的一种原子没有中子;B元素的原子得1个电子后形成的离子与氩原子电子数相同;C元素的原子第三层电子数比第二层少2个;D元素的原子与A原子构成的分子A2D有10个电子。则A的元素符号为_____ ;B的离子结构示意图为_________________ ;C的原子结构示意图为_____________ ;D的元素名称为______________ 。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有元素X、Y、Z,已知X元素为-2价离子和Y元素为+1价离子的核外电子排布均与氖相同,Z元素最高价氧化物分子组成为Z2O3,4.5gZ元素的形成的单质与盐酸反应,在标准状况下生成5.6L氢气;Z原子核中质子数比中子数少一个。
(1)Z3+离子的结构示意图为___________ Y元素位于周期表中的第_____ 周期,第_____ 族。
(2)X和Y形成的化合物有__________ 、_________ (填化学式)其中高温下最稳定的化合物的电子式为____________ 。
(1)Z3+离子的结构示意图为
(2)X和Y形成的化合物有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F为原子序数依次增大的短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B的单质在D的单质中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A的单质在F的单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)元素A的名称为__________ 。
(2)A、D、E组成的化合物中,D的质量分数为40%,该化合物俗名为_____ 。其水溶液与F的单质反应的化学方程式为______ 。
(3)由这些元素组成的物质,其组成和结构信息如下表:
a的化学式为______ ;b的化学式为_______ ;c的电子式为________ 。
(1)元素A的名称为
(2)A、D、E组成的化合物中,D的质量分数为40%,该化合物俗名为
(3)由这些元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 由A和D组成的化合物,且原子个数之比为1:1 |
b | 由A、C、F三种元素组成的离子化合物 |
c | 化学组成为BDF2,且所有原子均满足最外层8电子结构 |
您最近一年使用:0次



