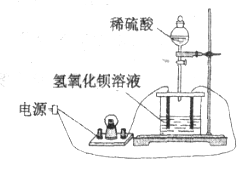
工业制硫酸的流程如图所示:
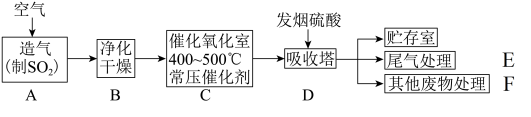
(1)早期以硫铁矿为原料造气,方程式为4FeS2+11O2 2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有
2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有___ mol电子发生了转移。
(2)如今大量改用固体硫为原料,同时生产过程中送入过量的空气,该改进从“减少污染物的排放”和___ 两个方面体现“绿色化学”。
(3)硫酸厂尾气处理的流程如图:
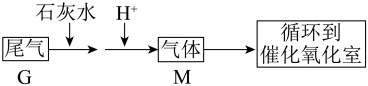
G的主要成分和M一样,如此处理的目的是___ ,将尾气G通入足量澄清石灰水,主要反应的离子方程式为___ 。
(4)如果C装置中生成0.1molSO3气体,可放出9.83kJ的热量。则该反应的热化学方程式为___ 。
(5)其他废弃物F中可能含有砷元素(As3+),处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式___ 。

(1)早期以硫铁矿为原料造气,方程式为4FeS2+11O2
 2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有
2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有(2)如今大量改用固体硫为原料,同时生产过程中送入过量的空气,该改进从“减少污染物的排放”和
(3)硫酸厂尾气处理的流程如图:

G的主要成分和M一样,如此处理的目的是
(4)如果C装置中生成0.1molSO3气体,可放出9.83kJ的热量。则该反应的热化学方程式为
(5)其他废弃物F中可能含有砷元素(As3+),处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式
更新时间:2020-11-12 19:01:27
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】稀土金属元素钪在国防、航天、核能等领域具有重要应用。从某工业废料“赤泥”(含有Fe2O3、Fe3O4、Al2O3、SiO2、Sc2O3、TiO2等)中回收Sc2O3的工艺流程如下:

已知:该条件下,Ksp[Fe(OH)3]=1.0×10−38,Ksp[Al(OH)3]=1.0×10−33,Kw=1.0×10−14。
请回答下列问题:
(1)稀土元素Y为第五周期Sc的同族元素,基态Y原子的d能级和s能级电子个数比为___________ 。
(2)“滤渣”的成分为TiO2和________ (填化学式,下同)。
(3)“氢氧化物沉淀”的成分为________ ;为使杂质离子沉淀完全,“调pH”范围应调节为_______ ~6之间。
(4)“氧化”时反应离子方程式为___________ 。
(5)“沉钪”时,将K2CO3固体加入草酸(H2C2O4)溶液[配料比n(K2CO3):n(H2C2O4)=2:3],制得KHC2O4和K2C2O4混合溶液。K2CO3需分批缓慢加入的原因是_______ ;发生反应的离子方程式为______ 。
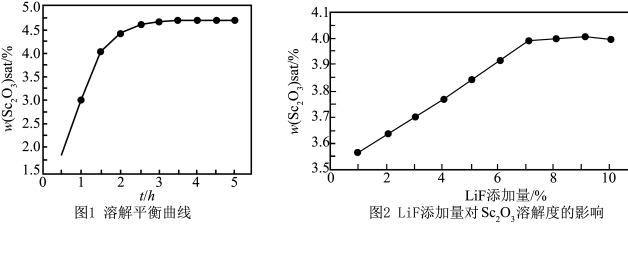
(6)Al-Sc合金是新一代航天结构材料,制备该合金的熔盐电解法涉及原料Sc2O3在熔盐体系中的溶解问题。950℃下部分条件对Sc2O3的溶解影响如图1、图2所示,则应采取的最佳溶解时间和LiF添加量分别为___________ 。

已知:该条件下,Ksp[Fe(OH)3]=1.0×10−38,Ksp[Al(OH)3]=1.0×10−33,Kw=1.0×10−14。
请回答下列问题:
(1)稀土元素Y为第五周期Sc的同族元素,基态Y原子的d能级和s能级电子个数比为
(2)“滤渣”的成分为TiO2和
(3)“氢氧化物沉淀”的成分为
(4)“氧化”时反应离子方程式为
(5)“沉钪”时,将K2CO3固体加入草酸(H2C2O4)溶液[配料比n(K2CO3):n(H2C2O4)=2:3],制得KHC2O4和K2C2O4混合溶液。K2CO3需分批缓慢加入的原因是
(6)Al-Sc合金是新一代航天结构材料,制备该合金的熔盐电解法涉及原料Sc2O3在熔盐体系中的溶解问题。950℃下部分条件对Sc2O3的溶解影响如图1、图2所示,则应采取的最佳溶解时间和LiF添加量分别为

您最近一年使用:0次
【推荐2】Ⅰ.Y、Y、Z三种物质有如图所示转化关系,其中X与稀盐酸不反应:

(1)写出上述①③④步反应的离子方程式:
①________ ;③________ ;
④________ 。
Ⅱ.有下列反应:①
② 根据两个反应回答:
根据两个反应回答:
(2)KMnO4、H2SO4、Cl2氧化性由强到弱顺序为________ 。
(3)反应①中氧化产物和还原产物的质量之比为________ 。
(4)反应②中浓盐酸表现出的性质是________(填字母)。
Ⅲ.已知化学方程式: 。
。
(5)请用双线桥法标出电子转移的方向和数目:________ 。

(1)写出上述①③④步反应的离子方程式:
①
④
Ⅱ.有下列反应:①

②
 根据两个反应回答:
根据两个反应回答:(2)KMnO4、H2SO4、Cl2氧化性由强到弱顺序为
(3)反应①中氧化产物和还原产物的质量之比为
(4)反应②中浓盐酸表现出的性质是________(填字母)。
| A.还原性 | B.酸性 | C.氧化性 |
Ⅲ.已知化学方程式:
 。
。(5)请用双线桥法标出电子转移的方向和数目:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子,原子核外有_______ 种不同能量的电子,写出其最外层电子的轨道表示式_______ ;碘元素在元素周期表中的位置是_______ ;液溴的保存通常采取的方法是_______ 。
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
(3) 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是_______ 。
(4)已知: 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:_______
(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_______
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是_______ (填字母)。
a.海盐提纯:

b.海水提镁:
c.海带提碘: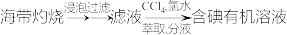

d.海水提溴:
(1)与氯元素同族的短周期元素的原子,原子核外有
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
A. 、 、 、 、 的氧化性 的氧化性 | B. 、 、 、 、 的熔点 的熔点 |
| C.HCl、HBr、HI的热稳定性 | D.HCl、HBr、HI的酸性 |
 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是(4)已知:
 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是
a.海盐提纯:


b.海水提镁:

c.海带提碘:
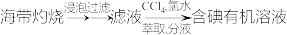

d.海水提溴:

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】(1)如图是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,已知E1=+134kJ·mol-1、E2=+368kJ·mol-1, 若在反应体系中加入催化剂,反应速率增大,E1的变化是________ (填“增大”“减小”或“不变”,下同),ΔH的变化是________ 。请写出NO2和CO反应的热化学方程式:________ 。

(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:
a: 2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ·mol-1
b: NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ·mol-1
c: H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
①对于a反应来说,________ (填“高温”“低温”或“无影响”)更有利于该反应的自发。
②写出CO2与NH3合成尿素和液态水的热化学反应方程式:________ 。

(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:
a: 2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ·mol-1
b: NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ·mol-1
c: H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
①对于a反应来说,
②写出CO2与NH3合成尿素和液态水的热化学反应方程式:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】(1)NaHCO3和Na2CO3可用于面食制作和油污清洗。
①常温下0.1mol·L-1 NaHCO3溶液呈_____ 性(填“酸”、“碱”或“中”),溶液中c(Na+)___ c (HCO3-)(填“>”、“<”或“=”);
②用Na2CO3溶液清洗油污时,加热可以增强去污能力,是由于升温_______ (填“促进”或“抑制”)Na2CO3水解,使溶液pH增大。
(2)C(s)与H2O(g)反应生成1molCO(g)和1molH2(g)吸收131.5kJ热量。该反应的热化学方程式为___ (填字母代号)。
A. C+H2O=CO+H2 △H= + 131.5kJ·mol-1
B. C(s)+H2O(g) =CO(g)+ H2(g) △H= + 131.5kJ
C. C(s)+H2O(g) =CO(g)+ H2(g) △H= + 131.5kJ·mol-1
(3)一定温度和压强下,可逆反应CO(g)+H2O(g) CO2(g)+H2(g)在密闭容器中达到平衡,请回答下列问题:
CO2(g)+H2(g)在密闭容器中达到平衡,请回答下列问题:
①若增大H2O(g)的浓度,则CO的转化率_______ (填“增大”或“减小”);
②若降低温度,平衡向正反应方向移动,则正反应为_____ 反应(填“放热”或“吸热”);
③若加入催化剂,则平衡______ (填字母代号)。
A.不移动 B.向正反应方向移动 C.向逆反应方向移动
(4)钢铁是目前用量最大、用途最广的金属材料,但钢铁容易生锈。
①某同学取一颗光亮的铁钉按图装置实验,数天后,试管内的现象是_______ (填字母代号);

A.铁钉不生锈,液面上升 B. 铁钉生锈,液面上升 C. 铁钉生锈,液面下升
②铁表面镀锌可以增强铁的耐腐蚀性。铁片镀锌装置的原理示意图如图所示,铁片作____ 极(填“阳”或“阴”),锌片上的电极反应式是______________________________________ 。

①常温下0.1mol·L-1 NaHCO3溶液呈
②用Na2CO3溶液清洗油污时,加热可以增强去污能力,是由于升温
(2)C(s)与H2O(g)反应生成1molCO(g)和1molH2(g)吸收131.5kJ热量。该反应的热化学方程式为
A. C+H2O=CO+H2 △H= + 131.5kJ·mol-1
B. C(s)+H2O(g) =CO(g)+ H2(g) △H= + 131.5kJ
C. C(s)+H2O(g) =CO(g)+ H2(g) △H= + 131.5kJ·mol-1
(3)一定温度和压强下,可逆反应CO(g)+H2O(g)
 CO2(g)+H2(g)在密闭容器中达到平衡,请回答下列问题:
CO2(g)+H2(g)在密闭容器中达到平衡,请回答下列问题:①若增大H2O(g)的浓度,则CO的转化率
②若降低温度,平衡向正反应方向移动,则正反应为
③若加入催化剂,则平衡
A.不移动 B.向正反应方向移动 C.向逆反应方向移动
(4)钢铁是目前用量最大、用途最广的金属材料,但钢铁容易生锈。
①某同学取一颗光亮的铁钉按图装置实验,数天后,试管内的现象是

A.铁钉不生锈,液面上升 B. 铁钉生锈,液面上升 C. 铁钉生锈,液面下升
②铁表面镀锌可以增强铁的耐腐蚀性。铁片镀锌装置的原理示意图如图所示,铁片作

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】高铁酸钾(K2FeO4)是一种新型绿色、高效的水处理剂,对病毒的去除率可达99.95%。某兴趣小组设计如下实验制备K2FeO4并探究其性质。
已知:①K2FeO4为紫色固体,微溶于KOH溶液;
② 具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。

(1)制备K2FeO4(夹持装置略)
①如图所示,A为氯气发生装置,装置A中盛放KMnO4的仪器名称是_______ 。
②装置C中的KOH溶液需过量,目的是_______ 。
③C中得到紫色固体和溶液,则C中Cl2与Fe(OH)3发生反应生成K2FeO4的离子方程式为_______ ,此外Cl2还与过量的KOH反应。
(2)探究K2FeO4的性质
甲同学取装置C中紫色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2.该现象不能证明“酸性条件下 氧化性强于Cl2”,其理由是:
氧化性强于Cl2”,其理由是:_______ 。
(3)测定K2FeO4的产率
若在制备装置C中加入Fe(OH)3的质量为10.7g,充分反应后经过滤、洗涤、干燥得K2FeO4固体10.3g,则K2FeO4的产率为_______ (保留3位有效数值)。
已知:①K2FeO4为紫色固体,微溶于KOH溶液;
②
 具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
①如图所示,A为氯气发生装置,装置A中盛放KMnO4的仪器名称是
②装置C中的KOH溶液需过量,目的是
③C中得到紫色固体和溶液,则C中Cl2与Fe(OH)3发生反应生成K2FeO4的离子方程式为
(2)探究K2FeO4的性质
甲同学取装置C中紫色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2.该现象不能证明“酸性条件下
 氧化性强于Cl2”,其理由是:
氧化性强于Cl2”,其理由是:(3)测定K2FeO4的产率
若在制备装置C中加入Fe(OH)3的质量为10.7g,充分反应后经过滤、洗涤、干燥得K2FeO4固体10.3g,则K2FeO4的产率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】四氯化锡可用作媒染剂等。某学习小组设计了如图所示的装置制备无水四氯化锡。反应原理是Sn(s)+2Cl2(g) SnCl4(l) ΔH=-511kJ·mol-1。已知:SnCl4熔点为-33°C,沸点为114°C,易水解。
SnCl4(l) ΔH=-511kJ·mol-1。已知:SnCl4熔点为-33°C,沸点为114°C,易水解。

(1)装置F的名称为_______ ,该装置的进水口为_______ (填“a”或“b”)。
(2)装置A中发生反应的离子方程式为_______ 。
(3)装置B中所用试剂X的名称是_______ 。
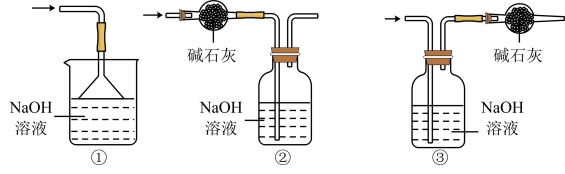
(4)上述实验设计中,还需尾气处理装置,可选用的装置是_______ (填序号)。
(5)实验结束后打开开关K通入氮气的目的是_______ 。
(6)SnCl4能溶解一定量的氯气,若制取300g溶有Cl2的SnCl4(其中Cl2的质量分数为13.0%,假设不含除Cl2外的其他杂质),则本实验中至少所需氯气的体积(标准状况下)是_______ L(保留2位小数)。
 SnCl4(l) ΔH=-511kJ·mol-1。已知:SnCl4熔点为-33°C,沸点为114°C,易水解。
SnCl4(l) ΔH=-511kJ·mol-1。已知:SnCl4熔点为-33°C,沸点为114°C,易水解。
(1)装置F的名称为
(2)装置A中发生反应的离子方程式为
(3)装置B中所用试剂X的名称是
(4)上述实验设计中,还需尾气处理装置,可选用的装置是

(5)实验结束后打开开关K通入氮气的目的是
(6)SnCl4能溶解一定量的氯气,若制取300g溶有Cl2的SnCl4(其中Cl2的质量分数为13.0%,假设不含除Cl2外的其他杂质),则本实验中至少所需氯气的体积(标准状况下)是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】从化合价的角度认识氯的化合物。
(1)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备 的反应原理如下:
的反应原理如下:

①该反应中,氧化剂是___________ ,氧化产物是___________ , 在反应中体现了
在反应中体现了___________ (填性质),依据氧化还原反应规律判断,氧化性强弱为
___________  (填>、<或
(填>、<或 )。
)。
② 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去,下列试剂中,可将
除去,下列试剂中,可将 转化为
转化为 的是
的是___________ (填字母序号)。
a. b.
b. c.
c. d.
d.
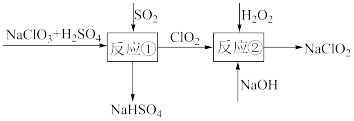
(2)亚氯酸钠 (NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:
请将流程中发生的两个反应的离子方程式补充完整(框中填系数,横线上填物质):
反应①_______
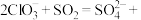 □___________
□___________
反应②________

(1)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备
 的反应原理如下:
的反应原理如下:
①该反应中,氧化剂是
 在反应中体现了
在反应中体现了
 (填>、<或
(填>、<或 )。
)。②
 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去,下列试剂中,可将
除去,下列试剂中,可将 转化为
转化为 的是
的是a.
 b.
b. c.
c. d.
d.
(2)亚氯酸钠 (NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:

请将流程中发生的两个反应的离子方程式补充完整(框中填系数,横线上填物质):
反应①
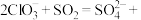 □___________
□___________反应②

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】“建设生态文明是中华民族永续发展的千年大计”。控制和治理NOx、SO2是解决光化学烟雾、减少酸雨、提高空气质量的有效途径,对构建生态文明有着极为重要的意义。
I.用下图装置可以制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。

(1)氨气的发生装置选择________ (填装置的字母符号),则其化学反应方程式为_________ 。
(2)装置D中观察到的现象为___________ 。
(3)用H装置做氨气喷泉实验时,氨气的进气口为___________ (填“M”或“N”),请写出引发喷泉的简单操作___________ 。
II.工业上制取硝酸铵的流程如图所示,请回答下列问题:
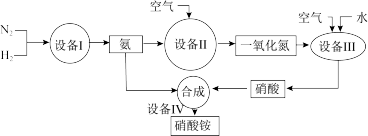
(4)设备II中,每有1molNO生成转移电子数目为___________ 。
(5)设备IV中的尾气主要为NO。NH3催化还原氮氧化物(SCR技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理下图所示:

SCR催化化反器中NH3还原NO的程式为___________ 。
I.用下图装置可以制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。

(1)氨气的发生装置选择
(2)装置D中观察到的现象为
(3)用H装置做氨气喷泉实验时,氨气的进气口为
II.工业上制取硝酸铵的流程如图所示,请回答下列问题:

(4)设备II中,每有1molNO生成转移电子数目为
(5)设备IV中的尾气主要为NO。NH3催化还原氮氧化物(SCR技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理下图所示:

SCR催化化反器中NH3还原NO的程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】高效灭菌消毒剂 气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性
气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性 溶液贮存,再经酸活化处理后使用。以氯酸盐
溶液贮存,再经酸活化处理后使用。以氯酸盐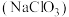 、过氧化氢和碳酸盐为主要原料制备稳定性
、过氧化氢和碳酸盐为主要原料制备稳定性 溶液的流程如下:
溶液的流程如下:

(1)反应器中发生的主要反应为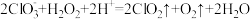 。
。
①该反应中 是
是___________ (填“氧化剂”、“还原剂”或“氧化剂和还原剂”)。
②制备时向反应器中通入空气的作用是___________ 。
(2)反应器中的反应温度控制在 左右为宜。
左右为宜。
①工业上采用的加热方式为___________ 。
②当温度超过 ,
, 的收率(
的收率(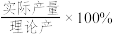 )随温度升高而减小,其原因可能是
)随温度升高而减小,其原因可能是___________ 。
(3)吸收瓶中发生反应 ,获得稳定性
,获得稳定性 溶液。当有
溶液。当有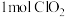 参加反应,转移的电子数为
参加反应,转移的电子数为___________  。
。
(4)以亚氯酸盐( )为原料进行酸化是生产
)为原料进行酸化是生产 最简单的方法,其反应原理为
最简单的方法,其反应原理为 ,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是
,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是___________ 。
 气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性
气态时不稳定,受热或光照易分解,浓度过高时甚至会发生爆炸。工业上通常先制成稳定性 溶液贮存,再经酸活化处理后使用。以氯酸盐
溶液贮存,再经酸活化处理后使用。以氯酸盐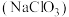 、过氧化氢和碳酸盐为主要原料制备稳定性
、过氧化氢和碳酸盐为主要原料制备稳定性 溶液的流程如下:
溶液的流程如下:
(1)反应器中发生的主要反应为
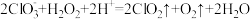 。
。①该反应中
 是
是②制备时向反应器中通入空气的作用是
(2)反应器中的反应温度控制在
 左右为宜。
左右为宜。①工业上采用的加热方式为
②当温度超过
 ,
, 的收率(
的收率(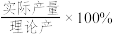 )随温度升高而减小,其原因可能是
)随温度升高而减小,其原因可能是(3)吸收瓶中发生反应
 ,获得稳定性
,获得稳定性 溶液。当有
溶液。当有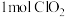 参加反应,转移的电子数为
参加反应,转移的电子数为 。
。(4)以亚氯酸盐(
 )为原料进行酸化是生产
)为原料进行酸化是生产 最简单的方法,其反应原理为
最简单的方法,其反应原理为 ,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是
,但该方法在实际生产中未得到广泛应用。与题干中的氯酸盐法相比,亚氯酸盐酸化法可能存在的缺点是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】为了将混有CaCl2、MgCl2、Na2SO4和难溶性杂质的粗盐进行提纯,某同学设计了如图实验方案:

请回答下列问题:
(1)操作①为___ 。
(2)操作②~④加入的试剂依次是___ 、___ 、___ 。
(3)写出过滤操作中所使用的玻璃仪器除了烧杯外,还需要___ 、___ 。
(4)简述判断SO 已除尽的方法
已除尽的方法___ 。
(5)工业上用电解精制的饱和食盐水的方法制取氯气,方程式为___ ,理论上每产生标准状况下5.6LCl2,转移电子的物质的量为___ 。

请回答下列问题:
(1)操作①为
(2)操作②~④加入的试剂依次是
(3)写出过滤操作中所使用的玻璃仪器除了烧杯外,还需要
(4)简述判断SO
 已除尽的方法
已除尽的方法(5)工业上用电解精制的饱和食盐水的方法制取氯气,方程式为
您最近一年使用:0次

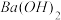 溶液中逐滴加入稀硫酸,不断搅拌至过量。
溶液中逐滴加入稀硫酸,不断搅拌至过量。