高铁酸钠是一种高效多功能水处理剂,制备高铁酸钠有多种方法。
(1)用Na2O2与FeSO4干法制备Na2FeO4的反应包含的热化学方程式有:
4FeSO4(s)+4Na2O2(s)=2Fe2O3(s)+4Na2SO4(s)+O2(g) ΔH=a kJ·mol-1
2Fe2O3(s)+2Na2O2(s)=4NaFeO2(s)+O2(g) ΔH=b kJ·mol-1
2NaFeO2(s)+3Na2O2(s)=2Na2FeO4(s)+2Na2O(s) ΔH=c kJ·mol-1
反应2FeSO4(s)+6Na2O2(s)=2Na2FeO4(s)+2Na2O(s)+2Na2SO4(s)+O2(g) ΔH=___________ kJ·mol-1(用含a、b、c的代数式表示)。
(2)Na2FeO4在强碱性条件稳定,易被H2还原。以铁合金、Ni为电极,电解NaOH溶液制取Na2FeO4的装置如图所示。
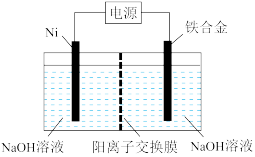
①电解时所发生总反应的化学方程式为___________ 。
②电解槽使用阳离子交换膜的作用:___________ 和允许导电的Na+通过。
③如果用铅蓄电池作为该电解池的电源,则铁合金应与铅蓄电池的___________ (填“Pb”或“PbO2”)相连。阳离子交换膜每通过1 mol Na+,铅蓄电池的正极将增重___________ g。
④将Na2FeO4投入水中,会有红褐色沉淀生成,同时溶液中气体放出,该气体的化学式为___________ 。
(1)用Na2O2与FeSO4干法制备Na2FeO4的反应包含的热化学方程式有:
4FeSO4(s)+4Na2O2(s)=2Fe2O3(s)+4Na2SO4(s)+O2(g) ΔH=a kJ·mol-1
2Fe2O3(s)+2Na2O2(s)=4NaFeO2(s)+O2(g) ΔH=b kJ·mol-1
2NaFeO2(s)+3Na2O2(s)=2Na2FeO4(s)+2Na2O(s) ΔH=c kJ·mol-1
反应2FeSO4(s)+6Na2O2(s)=2Na2FeO4(s)+2Na2O(s)+2Na2SO4(s)+O2(g) ΔH=
(2)Na2FeO4在强碱性条件稳定,易被H2还原。以铁合金、Ni为电极,电解NaOH溶液制取Na2FeO4的装置如图所示。

①电解时所发生总反应的化学方程式为
②电解槽使用阳离子交换膜的作用:
③如果用铅蓄电池作为该电解池的电源,则铁合金应与铅蓄电池的
④将Na2FeO4投入水中,会有红褐色沉淀生成,同时溶液中气体放出,该气体的化学式为
更新时间:2020-12-10 10:35:22
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】绿色能源是未来能源发展的重要方向,氢能是重要的绿色能源,利用生物乙醇来制取氢气的部分反应过程如图所示。

(1)已知:反应①:CH3CH2OH(g)+3H2O(g)=2CO2(g)+6H2(g) ΔH1=+173.5kJ·mol-1
反应②:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1
则反应Ⅰ的热化学方程式为____ 。
(2)反应Ⅱ在不同进气比[n(CO)∶n(H2O)]、不同温度下,测得相应的CO平衡转化率见表(各点对应的其他反应条件都相同)。
①a点平衡混合物中H2的体积分数为____ ,a、c两点对应的反应温度Ta____ Tc(填“<”“=”或“>”),d点对应的平衡常数K=____ 。
②有利于提高CO平衡转化率的是____ (填标号)。
A.增大压强 B.降低温度 C.增大进气比[n(CO)∶n(H2O)] D.分离出CO2
(3)反应Ⅱ在工业上称为一氧化碳的催化变换反应,若用[K]表示催化剂,则反应历程可用下式表示:
第一步:[K]+H2O(g)=[K]O+H2
第二步:[K]O+CO=[K]+CO2
第二步比第一步反应慢,则第二步反应的活化能比第一步反应____ 。
(4)研究表明,CO催化变换反应的速率方程为 =k(
=k(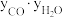 -
-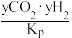 )式中,yCO、
)式中,yCO、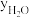 、
、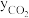 、
、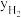 分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp
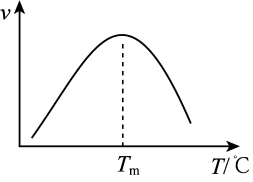
分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp___ (填“增大”“减小”)。根据速率方程分析,T>Tm时 逐渐减小的原因是
逐渐减小的原因是____ 。

(1)已知:反应①:CH3CH2OH(g)+3H2O(g)=2CO2(g)+6H2(g) ΔH1=+173.5kJ·mol-1
反应②:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1
则反应Ⅰ的热化学方程式为
(2)反应Ⅱ在不同进气比[n(CO)∶n(H2O)]、不同温度下,测得相应的CO平衡转化率见表(各点对应的其他反应条件都相同)。
| 平衡点 | a | b | c | d |
| n(CO)∶n(H2O) | 0.5 | 0.5 | 1 | 1 |
| CO平衡转化率/% | 50 | 66.7 | 50 | 60 |
②有利于提高CO平衡转化率的是
A.增大压强 B.降低温度 C.增大进气比[n(CO)∶n(H2O)] D.分离出CO2
(3)反应Ⅱ在工业上称为一氧化碳的催化变换反应,若用[K]表示催化剂,则反应历程可用下式表示:
第一步:[K]+H2O(g)=[K]O+H2
第二步:[K]O+CO=[K]+CO2
第二步比第一步反应慢,则第二步反应的活化能比第一步反应
(4)研究表明,CO催化变换反应的速率方程为
 =k(
=k(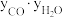 -
-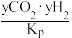 )式中,yCO、
)式中,yCO、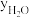 、
、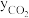 、
、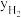 分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp
分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp 逐渐减小的原因是
逐渐减小的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】对 和
和 的高效利用能够有效缓解全球变暖。
的高效利用能够有效缓解全球变暖。
(1)已知标准大气压下, 、CO、
、CO、 的燃烧热分别为890.0kJ/mol、283.0kJ/mol、285.8kJ/mol,请计算反应
的燃烧热分别为890.0kJ/mol、283.0kJ/mol、285.8kJ/mol,请计算反应 的△H=
的△H=___________ kJ/mol。
(2)在两个体积均为2L的恒容密闭容器中,在相同温度下进行反应:
 (假设不发生其他反应),起始时按表中相应的量加入物质。
(假设不发生其他反应),起始时按表中相应的量加入物质。 的平衡转化率如表所示。
的平衡转化率如表所示。
①该温度下,反应的平衡常数K=___________ 。
②下列条件能说明反应达到平衡状态的是___________ (填标号)。
A.
B.容器内混合气体的总压强不再变化
C.容器内混合气体的密度保持不变
D.容器内各物质的浓度满足
③达到平衡时,Y内 的平衡转化率
的平衡转化率___________ 50%(填“>”,“<”或“=”)。判断理由是:___________ 。
(3) 还可以通过催化加氢合成乙醇:
还可以通过催化加氢合成乙醇: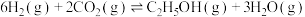 △H<0,设m为起始时的投料比,即
△H<0,设m为起始时的投料比,即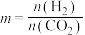 。通过实验得到下列图像:
。通过实验得到下列图像:___________ 。
②图2表示在m=3时,平衡状态各物质的物质的量分数与温度的关系,则a曲线表示的是___________ 的物质的量分数。恒压下,温度为 时
时 的平衡转化率为
的平衡转化率为___________ (保留3位有效数字)。
 和
和 的高效利用能够有效缓解全球变暖。
的高效利用能够有效缓解全球变暖。(1)已知标准大气压下,
 、CO、
、CO、 的燃烧热分别为890.0kJ/mol、283.0kJ/mol、285.8kJ/mol,请计算反应
的燃烧热分别为890.0kJ/mol、283.0kJ/mol、285.8kJ/mol,请计算反应 的△H=
的△H=(2)在两个体积均为2L的恒容密闭容器中,在相同温度下进行反应:
 (假设不发生其他反应),起始时按表中相应的量加入物质。
(假设不发生其他反应),起始时按表中相应的量加入物质。 的平衡转化率如表所示。
的平衡转化率如表所示。| 容器 | 起始物质的量/mol |  的平衡转化率 的平衡转化率 | |||
 |  | CO |  | ||
| X | 1 | 1 | 0 | 0 | 50% |
| Y | 2 | 2 | 0 | 0 | — |
②下列条件能说明反应达到平衡状态的是
A.

B.容器内混合气体的总压强不再变化
C.容器内混合气体的密度保持不变
D.容器内各物质的浓度满足

③达到平衡时,Y内
 的平衡转化率
的平衡转化率(3)
 还可以通过催化加氢合成乙醇:
还可以通过催化加氢合成乙醇: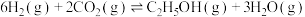 △H<0,设m为起始时的投料比,即
△H<0,设m为起始时的投料比,即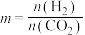 。通过实验得到下列图像:
。通过实验得到下列图像: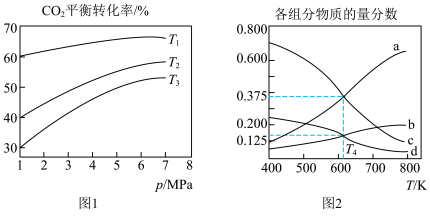
②图2表示在m=3时,平衡状态各物质的物质的量分数与温度的关系,则a曲线表示的是
 时
时 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】完成下列问题。
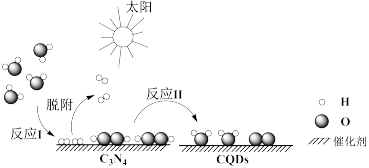
(1)中国化学家研究出一种新型复合光催化剂(C3N4/CQDs),能利用太阳光高效分解水,原理如下图所示。
已知化学键键能如下表:
①反应I化学方程式为___________ 。
②写出反应II的热化学方程式___________ 。
③设总反应反应热为∆H,反应I反应热为∆H1,则∆H___________ ∆H1填“>”“<”或“=”)。
(2)已知H3PO2(次磷酸)酸性比H3PO4弱,H3PO2与过量的NaOH反应生成NaH2PO2。
①写出次磷酸的电离方程式___________ 。
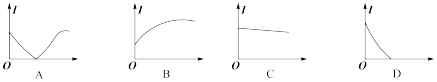
②向H3PO2溶液中逐滴加入等浓度的NaOH溶液至过量,其导电性变化图象为___________ ;向稀NaOH溶液中逐滴滴加浓H3PO2溶液至恰好中和,其导电性变化图象为___________ 。
③常温下磷酸和氢氧化钠溶液反应获得含磷各物种的分布分数与pH的关系如图所示。

由图分析:H3PO4的Ka1=___________ 。
(1)中国化学家研究出一种新型复合光催化剂(C3N4/CQDs),能利用太阳光高效分解水,原理如下图所示。

已知化学键键能如下表:
| 共价键 | O-H | O-O | O=O |
| 键能/(kJ∙mol-1) | 464 | 146 | 498 |
①反应I化学方程式为
②写出反应II的热化学方程式
③设总反应反应热为∆H,反应I反应热为∆H1,则∆H
(2)已知H3PO2(次磷酸)酸性比H3PO4弱,H3PO2与过量的NaOH反应生成NaH2PO2。
①写出次磷酸的电离方程式
②向H3PO2溶液中逐滴加入等浓度的NaOH溶液至过量,其导电性变化图象为

③常温下磷酸和氢氧化钠溶液反应获得含磷各物种的分布分数与pH的关系如图所示。

由图分析:H3PO4的Ka1=
您最近一年使用:0次
【推荐1】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
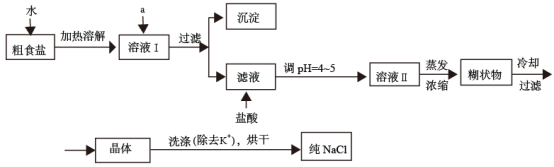
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液 、
BaCl2溶液、Ba(NO3)2溶液 、75%乙醇 、四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为_________ (只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为________________ 。
(2)用提纯的NaCl配制500mL4.00 mol·L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有______________ (填仪器名称)。
(3)用pH试纸测定滤液pH的操作是:___________________ 。
(4)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2______ (填“>”、“=”或“<”)2L,原因是_________________________ 。 装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为___________________ 。
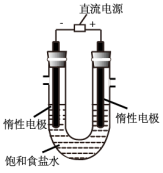
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液 、
BaCl2溶液、Ba(NO3)2溶液 、75%乙醇 、四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
(2)用提纯的NaCl配制500mL4.00 mol·L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有
(3)用pH试纸测定滤液pH的操作是:
(4)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2

您最近一年使用:0次
【推荐2】铅的单质、氧化物、盐在现代工业中有着重要用途。
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,盛有PbO2的圆底烧瓶中滴加浓盐酸,产生黄绿色气体,其反应的化学方程式为__ 。
(2)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如图:
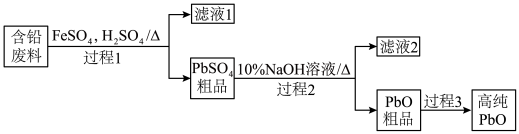
过程1中分离提纯的方法是__ ,滤液2中的溶质主要是_ (填物质的名称)。过程1中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__ 。
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
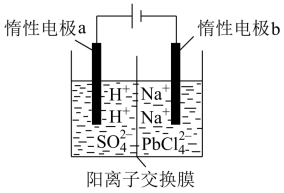
①写出电解时阴极的电极反应式__ 。
②电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向__ 极室(填“阴”或者“阳”)加入__ (填化学式)。
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,盛有PbO2的圆底烧瓶中滴加浓盐酸,产生黄绿色气体,其反应的化学方程式为
(2)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如图:

过程1中分离提纯的方法是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近一年使用:0次
【推荐3】工业上由黄铜矿(主要成分为CuFeS2)冶炼铜的主要流程如图:

请回答下列问题:
(1)气体A中的大气污染物可选用下列试剂中的___ 吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)由泡铜冶炼粗铜的化学方程式为____ 。
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___ 。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.从阳极泥中可回收Ag、Pt、Au等金属

请回答下列问题:
(1)气体A中的大气污染物可选用下列试剂中的
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)由泡铜冶炼粗铜的化学方程式为
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.从阳极泥中可回收Ag、Pt、Au等金属
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】如图为相互串联的甲乙两电解池.

试回答:
(1)甲池若为用电解原理精炼铜的装置,A是________ 极,材料是________ ,电极反应为_______ ,B是________ 极,材料是________ ,主要电极反应为__________ ,电解质溶液为________ .
(2)乙池中若滴入少量酚酞试液,电解一段时间后Fe极附近呈________ 色.
(3)若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为________ .若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为________

试回答:
(1)甲池若为用电解原理精炼铜的装置,A是
(2)乙池中若滴入少量酚酞试液,电解一段时间后Fe极附近呈
(3)若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为
您最近一年使用:0次
【推荐2】“雾霾”成为人们越来越关心的环境问题.雾霾中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质.请回答下列问题:
(1)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨.

①a表示____ 离子交换膜(填“阴”或“阳”).A﹣E分别代表生产中的原料或产品.其中C为硫酸,则A表示______ .E表示_______ .
②阳极的电极反应式为___________________________________ .
(2)Na2SO3溶液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
①Na2SO3溶液显______ 性,理由(请用离子方程式表示)_______________________
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(3)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g) 2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示.
2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示.
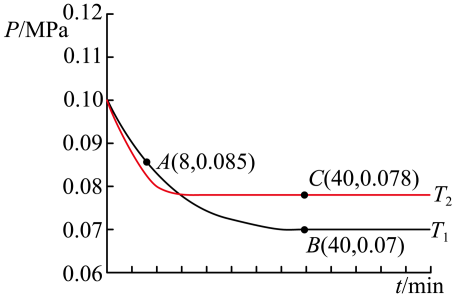
①图中A点时,SO2的转化率为________ .
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,C点的正反应速率vc(正)与A点的逆反应速率vA (逆)的大小关系为vc(正)_____ vA (逆)(填“>”、“<”或“=”)
③图中B点的压强平衡常数kp=__________ (用平衡分压代替平衡浓度计算.分压=总压×物质的量分数).
(1)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨.

①a表示
②阳极的电极反应式为
(2)Na2SO3溶液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
| n(SO3²﹣):n(HSO3﹣) | 99:1 | 1:1 | 1:99 |
| pH | 8.2 | 7.2 | 6.2 |
①Na2SO3溶液显
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(3)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g)
 2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示.
2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示.
①图中A点时,SO2的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,C点的正反应速率vc(正)与A点的逆反应速率vA (逆)的大小关系为vc(正)
③图中B点的压强平衡常数kp=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
某科研小组用电浮选凝聚法处理污水,设计装置如下图所示:
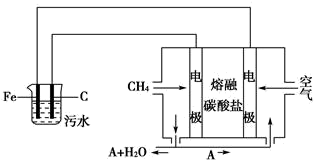
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的___________ 。
a.H2SO4 b.BaSO4c.Na2SO4d.NaoH e.CH3CH2OH
(2)电解池阳极的电极反应分别是①__________ ;②_________ 。
(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是:_____________ 。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应式为:CH4+4CO32—8e- 5CO2+2H2O。
①正极的电极反应是__________________________ 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是_____________ 。
(5)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)___________________ L。
某科研小组用电浮选凝聚法处理污水,设计装置如下图所示:

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的
a.H2SO4 b.BaSO4c.Na2SO4d.NaoH e.CH3CH2OH
(2)电解池阳极的电极反应分别是①
(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是:
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应式为:CH4+4CO32—8e- 5CO2+2H2O。
①正极的电极反应是
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是
(5)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
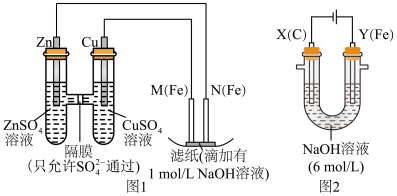
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是______ (填字母序号)。
A.铝 B.石墨 C.银 D.铂
(2)M 极发生反应的电极反应式为____________________________________________________ 。
此装置中发生的总反应化学方程式___________________________________________ 。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH________ (填“增大”“减小”或“不变”)。
(4)电解过程中, 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少________ g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为____________________________________________ 。

请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是
A.铝 B.石墨 C.银 D.铂
(2)M 极发生反应的电极反应式为
此装置中发生的总反应化学方程式
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH
(4)电解过程中, 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】某硫酸厂用以下几种方法处理SO2尾气。
(1)活性炭还原法
反应原理:恒温恒容2C(s)+2SO2(g) S2(g)+2CO2(g)。
S2(g)+2CO2(g)。
反应进行到不同时间测得各物质的浓度如图:
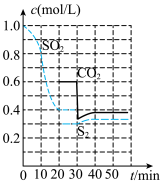
①第一次出现平衡的时间是第__ min;
②0~20min反应速率表示为v(SO2)=__ ;
③30min时,改变某一条件平衡移动,则改变的条件最有可能是__ ;40min时,平衡常数值为__ 。
(2)亚硫酸钠吸收法
常温下,Na2SO3溶液吸收SO2生成NaHSO3,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是__ (填序号)。
a.c(Na+)+c(H+)>c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
b.c(Na+)=c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
c.水电离出的c(OH-)=1×10-8mol·L-1
d.c(Na+)>c(SO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
(3)电化学处理法
如图所示,Pt(1)电极的反应式为__ ;碱性条件下,用Pt(2)电极排出的S2O 溶液吸收NO2,使其转化为N2,同时有SO
溶液吸收NO2,使其转化为N2,同时有SO 生成。若阳极转移电子6mol,则理论上处理NO2气体
生成。若阳极转移电子6mol,则理论上处理NO2气体__ g。

(1)活性炭还原法
反应原理:恒温恒容2C(s)+2SO2(g)
 S2(g)+2CO2(g)。
S2(g)+2CO2(g)。反应进行到不同时间测得各物质的浓度如图:

①第一次出现平衡的时间是第
②0~20min反应速率表示为v(SO2)=
③30min时,改变某一条件平衡移动,则改变的条件最有可能是
(2)亚硫酸钠吸收法
常温下,Na2SO3溶液吸收SO2生成NaHSO3,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是
a.c(Na+)+c(H+)>c(SO
 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)b.c(Na+)=c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)c.水电离出的c(OH-)=1×10-8mol·L-1
d.c(Na+)>c(SO
 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)(3)电化学处理法
如图所示,Pt(1)电极的反应式为
 溶液吸收NO2,使其转化为N2,同时有SO
溶液吸收NO2,使其转化为N2,同时有SO 生成。若阳极转移电子6mol,则理论上处理NO2气体
生成。若阳极转移电子6mol,则理论上处理NO2气体
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】知识的梳理和感悟是有效学习的方法之一、某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。

(1)图1中,电解一段时间后,气球b中的气体是___________ (填化学式),U形管___________ (填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的___________ 极;该发生器中反应的总离子方程式为___________ 。
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下面是以CH3OH燃料电池为电源电解法制取ClO2的装置图。
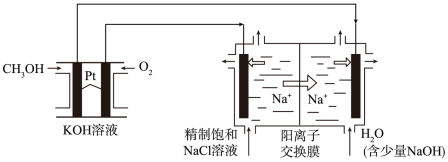
①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH___________ (填“增大”、“减小”或“不变”),负极反应式为___________ 。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.阳极产生ClO2的反应式为___________ 。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为___________ mol。

(1)图1中,电解一段时间后,气球b中的气体是
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下面是以CH3OH燃料电池为电源电解法制取ClO2的装置图。

①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.阳极产生ClO2的反应式为
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
您最近一年使用:0次



