已知K2HPO4溶液呈碱性,即HPO 结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:HPO
结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:HPO +H2O⇌PO
+H2O⇌PO +H3O+。下列操作能使该溶液中c(H3O+)增大的是
+H3O+。下列操作能使该溶液中c(H3O+)增大的是
 结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:HPO
结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:HPO +H2O⇌PO
+H2O⇌PO +H3O+。下列操作能使该溶液中c(H3O+)增大的是
+H3O+。下列操作能使该溶液中c(H3O+)增大的是| A.加水 | B.加热 | C.加消石灰 | D.加K2HPO4 |
20-21高二上·安徽宿州·阶段练习 查看更多[2]
安徽省泗县第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)3.3.2 影响盐类水解的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
更新时间:2020-12-23 10:54:56
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】在 溶液中存在电离平衡:
溶液中存在电离平衡: ,要使溶液中
,要使溶液中 浓度增大,且电离平衡逆向移动,可采取的措施是( )
浓度增大,且电离平衡逆向移动,可采取的措施是( )
 溶液中存在电离平衡:
溶液中存在电离平衡: ,要使溶液中
,要使溶液中 浓度增大,且电离平衡逆向移动,可采取的措施是( )
浓度增大,且电离平衡逆向移动,可采取的措施是( )| A.加水 | B.加热 | C.加 固体 固体 | D.加 固体 固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】某浓度的氨水中存在下列平衡:NH3·H2O
 +OH-,如想减小
+OH-,如想减小 的浓度,而增大OH-的浓度,采取措施有效的是( )
的浓度,而增大OH-的浓度,采取措施有效的是( )

 +OH-,如想减小
+OH-,如想减小 的浓度,而增大OH-的浓度,采取措施有效的是( )
的浓度,而增大OH-的浓度,采取措施有效的是( ) | A.通入HCl | B.加入NH4Cl固体 |
| C.加入少量FeCl3 | D.加入少量NaOH |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
| A.KAl(SO4)2溶液加热 | B.NH4NO3溶液中加入少量NaNO3固体 |
| C.氨水中加入少量NH4Cl固体 | D.Na2CO3溶液加热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】为使Na2S溶液中c(Na+)/c(S2-)的值减小,可加入的物质是
①盐酸 ②适量的NaOH溶液 ③适量的KOH溶液 ④适量的K2S固体
①盐酸 ②适量的NaOH溶液 ③适量的KOH溶液 ④适量的K2S固体
| A.①② | B.②③ | C.③④ | D.①④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】常温下,将等体积、等物质的量浓度的 与NaCl溶液混合,析出部分
与NaCl溶液混合,析出部分 晶体。下列指定溶液中微粒浓度大小比较正确的是
晶体。下列指定溶液中微粒浓度大小比较正确的是
 与NaCl溶液混合,析出部分
与NaCl溶液混合,析出部分 晶体。下列指定溶液中微粒浓度大小比较正确的是
晶体。下列指定溶液中微粒浓度大小比较正确的是A.原 溶液中: 溶液中: |
B.原 溶液中: 溶液中: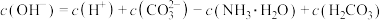 |
C.析出晶体后的溶液中: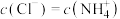 , ,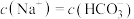 |
D.析出晶体后的溶液中: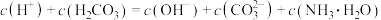 |
您最近一年使用:0次
单选题
|
较易
(0.85)
真题
名校
【推荐1】实验测得0.5 mol·L−1CH3COONa溶液、0.5 mol·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
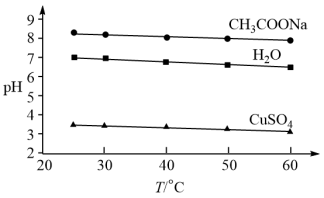

| A.随温度升高,纯水中c(H+)>c(OH−) |
| B.随温度升高,CH3COONa溶液的c(OH−)减小 |
| C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果 |
| D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在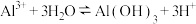 的平衡体系中,要抑制
的平衡体系中,要抑制 的水解,可采取的措施为
的水解,可采取的措施为
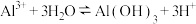 的平衡体系中,要抑制
的平衡体系中,要抑制 的水解,可采取的措施为
的水解,可采取的措施为| A.加热 | B.通入氯化氢气体 | C.加入适量的氢氧化钠溶液 | D.加入固体 |
您最近一年使用:0次


 +OH-,若要使平衡向逆方向移动,同时使c平(OH-)增大,应加入适量的
+OH-,若要使平衡向逆方向移动,同时使c平(OH-)增大,应加入适量的 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法正确的是(
。下列说法正确的是( ,平衡向正反应方向移动
,平衡向正反应方向移动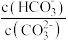 减小
减小

