氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,易溶于水,难溶于CCl4,某研究小组用如图1所示的实验装置制备氨基甲酸铵。反应原理:2NH3(g)+CO2(g) NH2COONH4(s);△H<0。
NH2COONH4(s);△H<0。
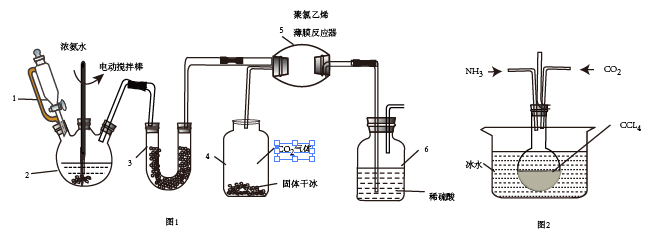
(1)仪器4的名称为__ ,仪器3中的固体是__ 。
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该__ (填“加快”、“减慢”或“不改变”)产生氨气的流速。
(3)另有一种制备氨基甲酸铵的反应器(CCl4充当惰性介质)如图2:
①图2装置采用冰水浴的原因为__ 。
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是__ (选填序号)
a.蒸馏 b.高压加热烘干 c.真空微热烘干
(4)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式为__ 。
 NH2COONH4(s);△H<0。
NH2COONH4(s);△H<0。
(1)仪器4的名称为
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该
(3)另有一种制备氨基甲酸铵的反应器(CCl4充当惰性介质)如图2:
①图2装置采用冰水浴的原因为
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是
a.蒸馏 b.高压加热烘干 c.真空微热烘干
(4)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式为
更新时间:2020-12-30 21:39:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
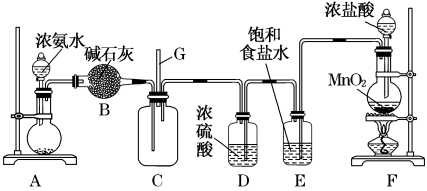
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用______(填序号)。
(2)装置B的作用是____ ;装置E的作用是____ 。
(3)通入装置C的两根导管左边较长、右边较短,目的是__________ 。
(4)装置F中发生反应的化学方程式是_______ 。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:_______ 。
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?___ 。

请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用______(填序号)。
| A.生石灰 | B.碱石灰 | C.五氧化二磷 | D.烧碱 |
(3)通入装置C的两根导管左边较长、右边较短,目的是
(4)装置F中发生反应的化学方程式是
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】下图为实验室制取氨气,二氧化硫及有关性质实验的组合装置。
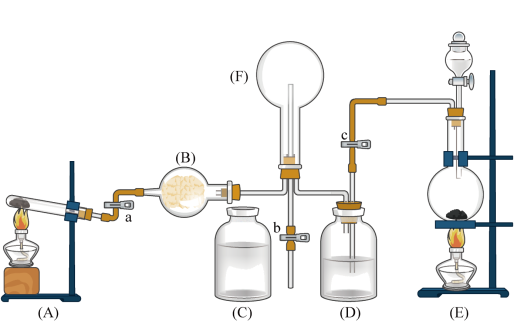
(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为___________ ;
(2)B仪器称为___________ ,在此实验中B应加入___________ (写名称);
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:___________ ;
②D的作用是干燥气体,D中盛的是___________ (写名称);
(4)A、E中产生的气体都是有污染性的,吸收A尾气的试剂是___________ ,吸收E尾气的离子方程式为___________ 。
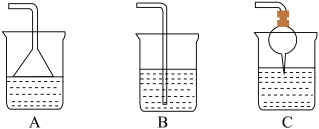
(5)生石灰与水反应生成 并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是___________ (填“a”“b”或“c”)。
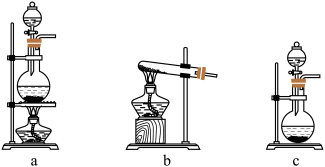
(6)为使生成的氨被硫酸吸收时不发生倒吸,可以选用下列装置中的___________ (填“A”“B”或“C”)。
(7)该小组又设计如图所示的实验装置(固定装置略),进行SO2性质的研究:
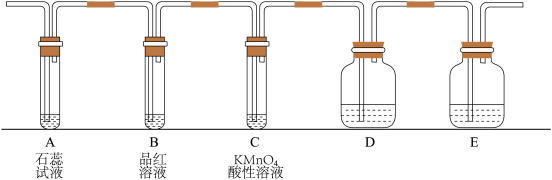
①当通入SO2时,A中紫色石蕊溶液变红,用化学方程式解释其原因是___________ 。
②可用来验证SO2具有漂白性的现象是:___________ 。
③从元素化合价的角度分析,SO2的性质:
a、当通入SO2一段时间后,可观察C中溶液褪色,说明SO2具有___________ 性。
b、如要验证SO2还具有另一方面的性质,D装置中的药品应为___________ 。
A.FeCl3溶液 B.氯水 C.氢硫酸 D.浓硝酸

(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为
(2)B仪器称为
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:
②D的作用是干燥气体,D中盛的是
(4)A、E中产生的气体都是有污染性的,吸收A尾气的试剂是
(5)生石灰与水反应生成
 并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
并放出热量。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
(6)为使生成的氨被硫酸吸收时不发生倒吸,可以选用下列装置中的

(7)该小组又设计如图所示的实验装置(固定装置略),进行SO2性质的研究:

①当通入SO2时,A中紫色石蕊溶液变红,用化学方程式解释其原因是
②可用来验证SO2具有漂白性的现象是:
③从元素化合价的角度分析,SO2的性质:
a、当通入SO2一段时间后,可观察C中溶液褪色,说明SO2具有
b、如要验证SO2还具有另一方面的性质,D装置中的药品应为
A.FeCl3溶液 B.氯水 C.氢硫酸 D.浓硝酸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学实验小组为了探究氨气的性质设计了如下实验方案。
实验一:探究氨气的溶解性
氨气具有强刺激性气味,会污染空气。实验小组经过多次尝试,最终将氨气的制备、收集、检验和喷泉实验于一体,设计出如图装置。
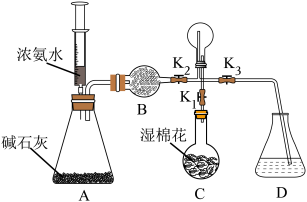
(1)写出气体发生装置仪器A中产生氨气的方程式___________ 。
(2)仪器B的名称___________ ,为了保证喷泉实验的良好效果,B中可以放入的试剂___________ 。
(3)实验时,打开K2,关闭K3,打开K1,将注射器中的浓氨水注入A中开始制备和收集氨气。已知仪器C中放入的是滴有酚酞溶液的湿棉花,则仪器C的作用___________ 。在不拆除装置的前提下,引发喷泉的操作是___________ 。
实验二:探究氨气的还原性
已知: Cu2O 呈红色固体,在酸性溶液中不稳定: Cu2O+ H2SO4=Cu+CuSO4+ H2O。
(4)装置G用于制备氨气,仪器的链接顺序为e,f接___________、___________、___________、___________ 、___________ 、___________接i,________ ,装置H的作用___________ 。实验开始前应先通一段时间的N2,其目的是___________ 。
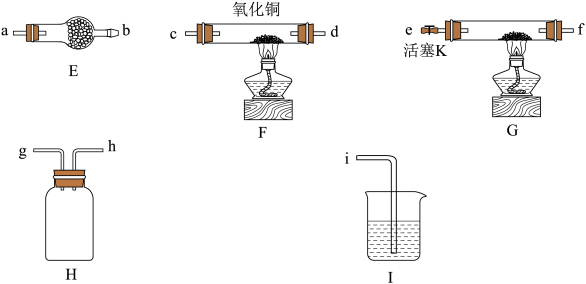
(5)反应结束后装置F中的氧化铜完全反应生成红色固体,为了探究红色固体的成分,进行了如下实验:取15.6g红色固体于烧杯中,加入足量稀硫酸充分搅拌、静置、过滤、洗涤、干燥、称重,得固体9.6g,则红色固体的成分及其物质的量为___________ 。
实验一:探究氨气的溶解性
氨气具有强刺激性气味,会污染空气。实验小组经过多次尝试,最终将氨气的制备、收集、检验和喷泉实验于一体,设计出如图装置。

(1)写出气体发生装置仪器A中产生氨气的方程式
(2)仪器B的名称
(3)实验时,打开K2,关闭K3,打开K1,将注射器中的浓氨水注入A中开始制备和收集氨气。已知仪器C中放入的是滴有酚酞溶液的湿棉花,则仪器C的作用
实验二:探究氨气的还原性
已知: Cu2O 呈红色固体,在酸性溶液中不稳定: Cu2O+ H2SO4=Cu+CuSO4+ H2O。
(4)装置G用于制备氨气,仪器的链接顺序为e,f接___________、___________、___________、___________ 、___________ 、___________接i,

(5)反应结束后装置F中的氧化铜完全反应生成红色固体,为了探究红色固体的成分,进行了如下实验:取15.6g红色固体于烧杯中,加入足量稀硫酸充分搅拌、静置、过滤、洗涤、干燥、称重,得固体9.6g,则红色固体的成分及其物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、CaO和SiO2等杂质)来制备,其工艺流程如下:

请回答下列问题:
(1)已知FeTiO3与盐酸反应后有TiOCl 生成, 写出该反应的离子方程式
生成, 写出该反应的离子方程式______ 。
(2)流程中的“氧化剂”最好选用什么试剂?为什么______ ?
(3)写出由FePO4制备LiFePO4的化学反应方程式______ 。
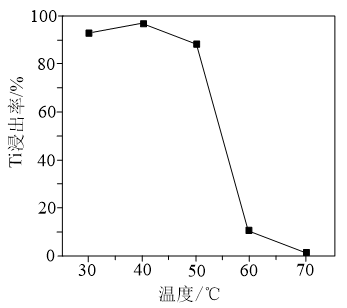
(4)用双氧水和氨水溶解TiO2固体时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti 元素浸出率下降,为什么______ ?
(5)过氧化钛酸锂Li2Ti5O15为一种配合物,请分析说明其中的过氧键(O- O)数目有多少_____ 个。
(6)“浸出”步骤中,温度对铁、钛的浸出效果如下图所示:
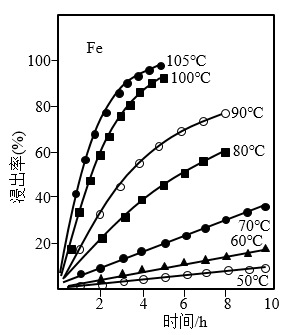

总结温度的影响规律:温度对铁和钛浸出效果的影响相似。请另写出两条规律_____ 。
(7) 25 °C 下,已知FePO4、Ca3(PO4)2与Mg3(PO4)2的标准溶度积常数K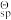 (简称为溶度积常数,简写为Ksp)分别为9.9 ×10-29、 2.0 ×10-33、 9.9 ×10-25, H3PO4的三级标准电离常数K
(简称为溶度积常数,简写为Ksp)分别为9.9 ×10-29、 2.0 ×10-33、 9.9 ×10-25, H3PO4的三级标准电离常数K (简称为电离常数,简写为Kai) 依次为7.1 ×10-3、 6.3 ×10-8、 4.2 ×10-13.若第二次过滤后所得滤液中Fe2+、Ca2+与Mg2+浓度分别为1.0、 0.02、 0.01 mol/L。试问,加入氧化剂和磷酸后(假设此时溶液中H+与H3PO4浓度均为1.0 mol/L),是否有Ca3(PO4)2与Mg3(PO4)2沉淀生成
(简称为电离常数,简写为Kai) 依次为7.1 ×10-3、 6.3 ×10-8、 4.2 ×10-13.若第二次过滤后所得滤液中Fe2+、Ca2+与Mg2+浓度分别为1.0、 0.02、 0.01 mol/L。试问,加入氧化剂和磷酸后(假设此时溶液中H+与H3PO4浓度均为1.0 mol/L),是否有Ca3(PO4)2与Mg3(PO4)2沉淀生成_____ ?
(8)若采用钛酸锂和磷酸亚铁锂作电极组成电池,充电时发生反应为:Li4Ti5O12 + LiFePO4 = Li4+xTi5O12 +Li 1-xFePO4 (0<x<1),请写出该电池放电时的阳极反应方程式_____ 。

请回答下列问题:
(1)已知FeTiO3与盐酸反应后有TiOCl
 生成, 写出该反应的离子方程式
生成, 写出该反应的离子方程式(2)流程中的“氧化剂”最好选用什么试剂?为什么
(3)写出由FePO4制备LiFePO4的化学反应方程式
(4)用双氧水和氨水溶解TiO2固体时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti 元素浸出率下降,为什么

(5)过氧化钛酸锂Li2Ti5O15为一种配合物,请分析说明其中的过氧键(O- O)数目有多少
(6)“浸出”步骤中,温度对铁、钛的浸出效果如下图所示:


总结温度的影响规律:温度对铁和钛浸出效果的影响相似。请另写出两条规律
(7) 25 °C 下,已知FePO4、Ca3(PO4)2与Mg3(PO4)2的标准溶度积常数K
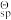 (简称为溶度积常数,简写为Ksp)分别为9.9 ×10-29、 2.0 ×10-33、 9.9 ×10-25, H3PO4的三级标准电离常数K
(简称为溶度积常数,简写为Ksp)分别为9.9 ×10-29、 2.0 ×10-33、 9.9 ×10-25, H3PO4的三级标准电离常数K (简称为电离常数,简写为Kai) 依次为7.1 ×10-3、 6.3 ×10-8、 4.2 ×10-13.若第二次过滤后所得滤液中Fe2+、Ca2+与Mg2+浓度分别为1.0、 0.02、 0.01 mol/L。试问,加入氧化剂和磷酸后(假设此时溶液中H+与H3PO4浓度均为1.0 mol/L),是否有Ca3(PO4)2与Mg3(PO4)2沉淀生成
(简称为电离常数,简写为Kai) 依次为7.1 ×10-3、 6.3 ×10-8、 4.2 ×10-13.若第二次过滤后所得滤液中Fe2+、Ca2+与Mg2+浓度分别为1.0、 0.02、 0.01 mol/L。试问,加入氧化剂和磷酸后(假设此时溶液中H+与H3PO4浓度均为1.0 mol/L),是否有Ca3(PO4)2与Mg3(PO4)2沉淀生成(8)若采用钛酸锂和磷酸亚铁锂作电极组成电池,充电时发生反应为:Li4Ti5O12 + LiFePO4 = Li4+xTi5O12 +Li 1-xFePO4 (0<x<1),请写出该电池放电时的阳极反应方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
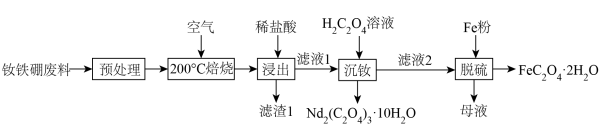
【推荐2】钕铁硼废料是一种具有较高经济价值的废弃物,主要成分为稀土元素钕(Nd)、Fe、B.一种采用分步沉淀从钕铁硼油泥中回收Nd2(C2O4)3·10H2O和FeC2O4·2H2O的工艺流程如图:
②H2CO4易与Fe3+形成多种配合物离子,易与Fe2+形成FeC2O4·2H2O沉淀。
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择___________ (填化学式)溶液。
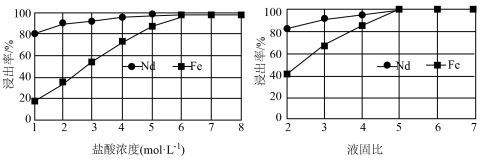
(2)“滤渣1”的主要成分是___________ (填名称)。“浸出”时,盐酸浓度和液固比对钕、铁的浸出率影响如图所示,则浸出过程的最佳条件是___________ 。___________ 。
(4)“沉铁”时,加入铁粉的作用是___________ 。
(5)FeC2O4·2H2O晶体结构片段如图所示。___________ ;碳原子采用___________ 杂化。现测定草酸亚铁晶体纯度。准确称取Wg样品于锥形瓶,加入适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液bmL。滴定反应: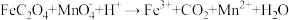 (未配平)。该样品纯度为
(未配平)。该样品纯度为___________ %。
②H2CO4易与Fe3+形成多种配合物离子,易与Fe2+形成FeC2O4·2H2O沉淀。
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择
(2)“滤渣1”的主要成分是
(4)“沉铁”时,加入铁粉的作用是
(5)FeC2O4·2H2O晶体结构片段如图所示。
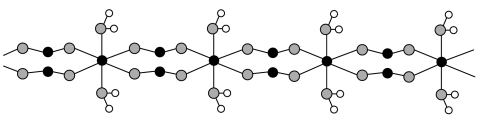
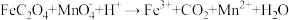 (未配平)。该样品纯度为
(未配平)。该样品纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】铵明矾晶体的化学式为 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。
(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有___________ 。
(2)步骤III中生成白色沉淀C反应的化学方程式为___________ 。
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是___________ 。
(4)设计实验验证固体A含有的金属元素:___________ 。
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值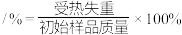 )
)
通过上述数据可判断,在温度区间___________ ℃,铵明矾基本上失去了结晶水。
 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。
 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有
(2)步骤III中生成白色沉淀C反应的化学方程式为
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是
(4)设计实验验证固体A含有的金属元素:
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值
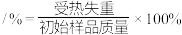 )
)| 温度区间/℃ | 18→190 | 190→430 | 430→505 | 505→900 |
| 失重计算值/% | 39.20 | 7.80 | 13.00 | 26.00 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铝氢化钠(NaAlH4)是有机合成中的一种重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝氢化钠的一种工艺流程如图:
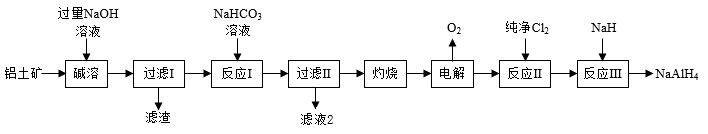
请根据所学知识回答下列问题:
(1)为了提高“碱溶”效率,在“碱溶”前对铝土矿进行的处理措施是_______ ;“过滤I”所得滤渣的主要成分为____________ 。
(2)反应I中主要反应的离子方程式为____________ 。
(3)反应III的化学方程式为________________ 。
(4)某学习小组对上面的工艺流程进行适当改变(如图所示。粗线框内为改变的流程),也达到了相同的目标。
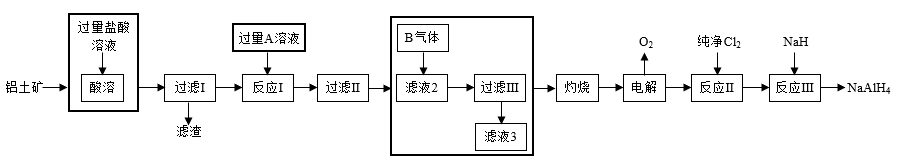
①A溶液可选用下列选项中的___________ (填标号)。
a NaOH溶液 b NH3·H2O溶液 c NaHCO3溶液 d Na2CO3溶液
②通常使用的B气体是________ ,通入过量B气体,滤液3中的主要溶质是____ (填化学式)。
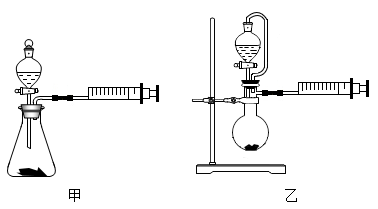
(5)铝氢化钠遇水发生剧烈反应生成偏铝酸钠和氢气,用此反应测定上述产品中铝氢化钠的纯度 (产品中杂质不与水反应),若用如图所示装置 (部分夹持仪器省略),则测出的最终结果准确度更高的是__________ (填“甲”或“乙”)。

请根据所学知识回答下列问题:
(1)为了提高“碱溶”效率,在“碱溶”前对铝土矿进行的处理措施是
(2)反应I中主要反应的离子方程式为
(3)反应III的化学方程式为
(4)某学习小组对上面的工艺流程进行适当改变(如图所示。粗线框内为改变的流程),也达到了相同的目标。

①A溶液可选用下列选项中的
a NaOH溶液 b NH3·H2O溶液 c NaHCO3溶液 d Na2CO3溶液
②通常使用的B气体是
(5)铝氢化钠遇水发生剧烈反应生成偏铝酸钠和氢气,用此反应测定上述产品中铝氢化钠的纯度 (产品中杂质不与水反应),若用如图所示装置 (部分夹持仪器省略),则测出的最终结果准确度更高的是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
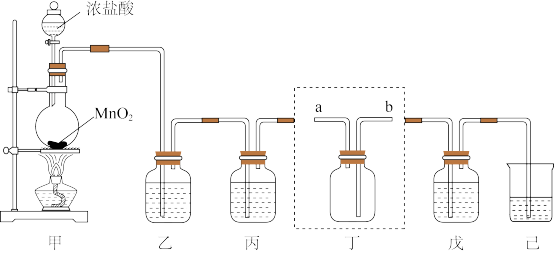
(1)盛装浓盐酸的仪器的名称为_______ ,装置甲中发生反应的化学方程式为_______ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为_______ (填标号);装置乙和丙盛装的试剂分别是_______ 、_______ 。(填名称)
(3)将氯气通入装置己中制备漂白液,则装置己中发生反应的离子方程式为_______ ,有同学认为装置己还有一个作用,该作用为_______ ,发挥该作用时_______ (填“能”或“不能”)用澄清石灰水代替。
(4)装置戊中盛装石灰乳用来制备漂白粉,漂白粉的有效成分为_______ (填化学式),漂白粉长时间暴露在空气中容易发生变质的原因为_______ (结合化学方程式说明)。

(1)盛装浓盐酸的仪器的名称为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备漂白液,则装置己中发生反应的离子方程式为
(4)装置戊中盛装石灰乳用来制备漂白粉,漂白粉的有效成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】无水 常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水
常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水 ,可选用的装置如图所示:
,可选用的装置如图所示:
i.熔融Sn与 反应生成
反应生成 (无色液体)时放出大量的热,
(无色液体)时放出大量的热, 熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成
熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成 ),且
),且 易溶于
易溶于 。
。
ii.Sn熔点为232℃;无水 熔点为246℃、沸点为652℃,具有强还原性。
熔点为246℃、沸点为652℃,具有强还原性。
回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)从平衡移动的角度解释 难溶于饱和食盐水的原因:
难溶于饱和食盐水的原因:___________ 。
(3)为了获得较纯的产品,当装置D处具支试管中___________ 时,再点燃装置D处酒精灯。反应制得的产品中可能会含有杂质 ,为加快反应速率并防止产品中混有
,为加快反应速率并防止产品中混有 ,除了通入过量
,除了通入过量 外,还应控制反应的最佳温度范围为
外,还应控制反应的最佳温度范围为___________ 。装置E的收集器中收集到的液体略显黄色,原因是___________ 。
(4)装置F的作用是___________ ;若缺少装置F,则装置E的收集器中发生反应的化学方程式为___________ 。
(5)碘氧化法滴定分析产品中 的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用
的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用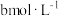 碘标准溶液滴定,发生反应:
碘标准溶液滴定,发生反应: 。滴定终点消耗碘标准溶液
。滴定终点消耗碘标准溶液 ,则产品中
,则产品中 的质量分数为
的质量分数为___________ (用含a、b、V的代数式表示)。
 常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水
常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水 ,可选用的装置如图所示:
,可选用的装置如图所示: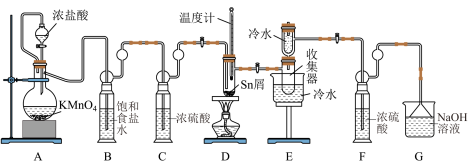
i.熔融Sn与
 反应生成
反应生成 (无色液体)时放出大量的热,
(无色液体)时放出大量的热, 熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成
熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成 ),且
),且 易溶于
易溶于 。
。ii.Sn熔点为232℃;无水
 熔点为246℃、沸点为652℃,具有强还原性。
熔点为246℃、沸点为652℃,具有强还原性。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)从平衡移动的角度解释
 难溶于饱和食盐水的原因:
难溶于饱和食盐水的原因:(3)为了获得较纯的产品,当装置D处具支试管中
 ,为加快反应速率并防止产品中混有
,为加快反应速率并防止产品中混有 ,除了通入过量
,除了通入过量 外,还应控制反应的最佳温度范围为
外,还应控制反应的最佳温度范围为(4)装置F的作用是
(5)碘氧化法滴定分析产品中
 的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用
的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用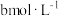 碘标准溶液滴定,发生反应:
碘标准溶液滴定,发生反应: 。滴定终点消耗碘标准溶液
。滴定终点消耗碘标准溶液 ,则产品中
,则产品中 的质量分数为
的质量分数为
您最近一年使用:0次



