设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温下,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
| B.常温下,2L0.1mol·L-1FeCl3溶液中,Fe3+的数目为0.2NA |
| C.常温下,1L pH=2的硫酸溶液中由水电离出的H+的数目为10-12NA |
| D.常温下,将0.1mol Cl2 溶于水,溶液中的HClO分子数为0.1 NA |
更新时间:2020-12-24 18:59:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
| A.1 mol Cu与足量S反应,转移的电子数为NA |
| B.1 mol Fe与稀硝酸反应转移电子数一定为3NA |
| C.22.4 L N2与足量的H2反应生成NH3的分子数为2NA |
| D.1 mol NH3与氧气恰好发生催化氧化反应,转移的电子数为7NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA表示阿伏加 德罗常数值,下列说法正确的是( )
| A.46gNO2和N2O4混合气体中含有原子数为3.5NA |
| B.50g质量分数为46%的乙醇水溶液中氧原子数为2NA |
| C.用惰性电极电解H2SO4溶液,若阳极产生5.6L气体,则电路中通过0.5NA电子 |
| D.常温下,1LpH=3的醋酸溶液稀释到10L时,溶液中H+的数目大于0.01NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下图为不同温度下水的电离平衡曲线,已知pOH=−lgc(OH−),下列说法正确的是
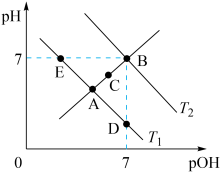

| A.T1和T2的关系是:T1>T2 |
| B.A点到D点:加入少量碱可实现 |
| C.Kw的关系是:B>C>A=D=E |
| D.T1时:pH=2的硫酸与pH=12的NaOH溶液等体积混合,溶液呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】有关化学反应原理的下列说法中正确的是
A. 溶液水解的离子方程式: 溶液水解的离子方程式: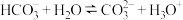 |
B.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
| C.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快 |
| D.常温下,向纯水中加入钠或氢氧化钠都能使水的电离平衡逆向移动,水离子积不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据实验操作和现象,所得到的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 相同温度下,用pH传感器测定SO2和CO2饱和溶液的pH,后者pH大 | 酸性: |
| B | 向5 mLFeCl3溶液中滴加10 mL等浓度的KI溶液,充分反应后,再滴加KSCN溶液,溶液最终变为血红色 | FeCl3溶液与KI溶液的反应为可逆反应 |
| C | 取两支试管,分别加入2 mL0.2 mol/L的酸性KMnO4溶液,然后分别向两支试管中加入2 mL0.6 mol/L和1.2 mol/L的H2C2O4溶液,后者完全褪色所需时间更短 | 其他条件相同时,增大反应物浓度反应速率增大 |
| D | 向K2Cr2O7溶液中滴加AgNO3溶液,有砖红色沉淀(Ag2CrO4)生成 | Ag2CrO4溶解度比Ag2Cr2O7小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中: 的溶液中: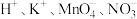 |
B. 溶液中: 溶液中: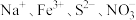 |
C.无色溶液中: |
D.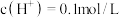 的溶液中: 的溶液中: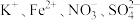 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据下列图示所得出的结论正确的是( )
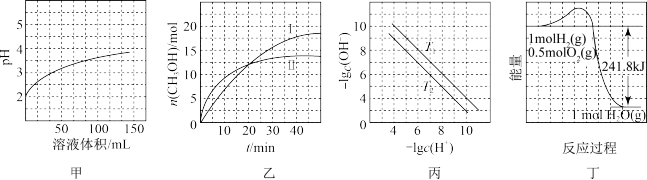

| A.图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸 |
B.图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g)  CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ |
| C.图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2 |
| D.图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是
A.某二元酸 在水中的电离方程式是: 在水中的电离方程式是: , , ;则NaHA溶液中: ;则NaHA溶液中: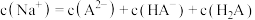 |
B.相同温度下将足量氯化银固体分别放入相同体积的①蒸馏水、② 盐酸、③ 盐酸、③ 氯化镁溶液、④ 氯化镁溶液、④ 硝酸银溶液中, 硝酸银溶液中, 为①>④=②>③ 为①>④=②>③ |
C.常温下,某溶液的 ,则该物质一定是酸或强酸弱碱盐 ,则该物质一定是酸或强酸弱碱盐 |
D.若 、 、 、 、 分别表示常温下 分别表示常温下 的电离平衡常数、 的电离平衡常数、 的水解平衡常数和水的离子积常数,则三者之间的关系为 的水解平衡常数和水的离子积常数,则三者之间的关系为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】关于常温下pH=12的氨水和氢氧化钠两溶液,下列说法正确的是
| A.氨水溶液的浓度大于氢氧化钠溶液 |
| B.NH3·H2O的电离方程式:NH3·H2O=NH4++OHˉ |
| C.c(NH3·H2O)+c(NH4+)=0.01mol·Lˉ1 |
| D.将两溶液稀释100倍,则稀释后溶液的pH值相同 |
您最近一年使用:0次

 )=0.5 mol,则Na+数目为NA
)=0.5 mol,则Na+数目为NA 、SO
、SO
 =1012的溶液中,NH
=1012的溶液中,NH 、Ca2+、Cl-、NO
、Ca2+、Cl-、NO



