羟胺(NH2OH)在水溶液中的电离方程式为NH2OH+H2O⇌NH3OH++OH-。温度不变条件下向该溶液中加入NaOH固体,下列说法不正确 的是
| A.平衡常数K减小 | B.n(OH-)增大 | C.平衡向左移动 | D. 增大 增大 |
20-21高二上·河北邯郸·期中 查看更多[6]
天津市河北区2021-2022学年高二上学期期末质量检测化学试题广东省清远市第一中学2021-2022学年高二上学期期中调研考试化学试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题湖北省应城市第一高级中学2020—2021学年高二12月月考化学试题(已下线)练习6 电离平衡与溶液的PH-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)河北省邯郸市联盟校2020-2021学年高二上学期期中考试化学试题
更新时间:2020-12-29 09:09:40
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列能证明乙酸是弱酸的事实是
A.乙酸能与纯碱溶液反应放出 | B.饱和乙酸钠溶液的pH>9 |
C.乙酸能电离出 | D.乙酸溶液能使紫色石蕊溶液变红 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA阿伏加德罗常数的值。下列叙述正确的是
| A.22 g D3O+中含有的中子数为10NA |
B.1 mol P4S3(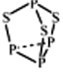 )分子中含有非极性键的数目为3NA )分子中含有非极性键的数目为3NA |
| C.1 L0.1 mol/L草酸(H2C2O4)溶液中含有H+的数目为0.2NA |
| D.11.2 L(标准状况)氧气与足量钠反应,转移的电子数一定为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某学习小组探究利用强碱准确滴定强酸和弱酸混合溶液中强酸的可能性,以 溶液滴定同浓度HCl和HA混合溶液为例(HA代表
溶液滴定同浓度HCl和HA混合溶液为例(HA代表 不同的任意弱酸)。HCl滴定百分比x、分布系数
不同的任意弱酸)。HCl滴定百分比x、分布系数 随pH变化关系如下图所示。
随pH变化关系如下图所示。 ,lg2=0.3]下列说法正确的是
,lg2=0.3]下列说法正确的是
 溶液滴定同浓度HCl和HA混合溶液为例(HA代表
溶液滴定同浓度HCl和HA混合溶液为例(HA代表 不同的任意弱酸)。HCl滴定百分比x、分布系数
不同的任意弱酸)。HCl滴定百分比x、分布系数 随pH变化关系如下图所示。
随pH变化关系如下图所示。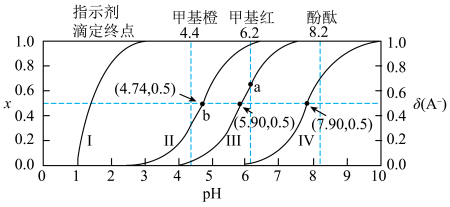
 ,lg2=0.3]下列说法正确的是
,lg2=0.3]下列说法正确的是| A.曲线对应酸的电离常数:Ⅱ<Ⅲ |
| B.a点的纵坐标约为0.67 |
C.b点处存在如下关系: |
D.甲基橙作指示剂, 大于 大于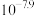 时,即可准确滴定混合溶液中的HCl 时,即可准确滴定混合溶液中的HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各项所述内容对应的图像不正确的是
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】水的电离平衡曲线如图所示。下列说法中,正确的是


| A.图中A、D、E三点处KW间的关系:E处>A处>D处 |
| B.温度不变时,往水中通入适量HCl气体,可以使水的电离从A点变化到D点 |
| C.温度不变时,在水中加入适量CH3COONa固体,可以使水的电离从A点变化到C点 |
| D.在B点处,0.5 mol·L-1的H2SO4溶液与1 mol·L-1的KOH溶液等体积混合,充分反应后,所得溶液的pH=7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于电解质溶液的叙述正确的是( )
| A.若常温下0.1mol/L的氨水pH为11, 则NH3·H2O电离常数约为10-6 |
| B.将pH=5的醋酸溶液稀释1000倍,溶液的pH=8 |
| C.某温度下纯水中c(OH-)=2×10—7mol/L,该温度下0.1mol/L的盐酸的pH=1 |
| D.用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaOH溶液的体积前者小于后者的10倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知25℃时,关于0.1mol/L醋酸溶液( ),下列说法正确的是
),下列说法正确的是
 ),下列说法正确的是
),下列说法正确的是A.升高温度,醋酸的电离程度增大, 增大 增大 |
B.向该溶液中通入HCl气体,平衡逆向移动, 减小 减小 |
| C.该温度下,该溶液中醋酸的电离程度大于0.01mol/L醋酸溶液中醋酸的电离程度 |
D.加水稀释后,溶液中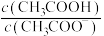 增大 增大 |
您最近一年使用:0次

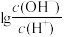 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 H++HA-
H++HA- )+c(NH3·H2O)=2c(A2-)
)+c(NH3·H2O)=2c(A2-)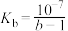

 溶液未达到电离平衡状态
溶液未达到电离平衡状态 相同
相同

