甲醇是可再生的清洁能源,可利用 与
与 合成甲醇,已知:①一定量
合成甲醇,已知:①一定量 和
和 反应生成
反应生成 和
和 ,当消耗
,当消耗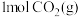 时,放出的能量是
时,放出的能量是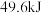 ;②
;②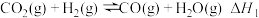 ;③
;③
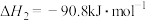 。下列说法正确的是
。下列说法正确的是
 与
与 合成甲醇,已知:①一定量
合成甲醇,已知:①一定量 和
和 反应生成
反应生成 和
和 ,当消耗
,当消耗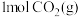 时,放出的能量是
时,放出的能量是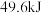 ;②
;②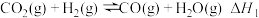 ;③
;③
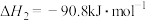 。下列说法正确的是
。下列说法正确的是A.①中反应的热化学方程式为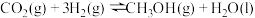  |
| B.在恒温恒容的密闭容器中发生反应②,气体压强不变时表明反应达到平衡 |
C.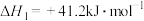 |
| D.反应③在高温下能自发进行 |
更新时间:2021-02-01 17:56:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】N2 (g)与H2 (g)在铁催化剂表面经历如下过程生成NH3(g): 下列说法正确的是
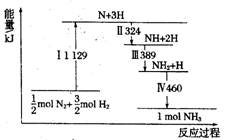

| A.I中破坏的均为极性键 | B.IV中NH2与H的总键能大于NH3中总键能 |
| C.II、III、IV均为放热过程 | D.N2 (g)+3H2 (g) NH3 (g) △H>0 NH3 (g) △H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知: 2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) △H=-226kJ/mol
O2(g) △H=-226kJ/mol

根据以上热化学方程式判断,下列说法正确的是
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) △H=-226kJ/mol
O2(g) △H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
| A.CO的燃烧热为283kJ |
| B.右图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)放出的热量小于452kJ |
| D.Na2O2(s)+CO(g)=Na2CO3(s) △H=-1018 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度恒容密闭容器,下列叙述不是可逆反应A(g)+3B(g) 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等;②单位时间内amolA生成,同时生成3amolB;③A,B,C的浓度不再变化;④混合气体的总压强不再变化;⑤混合气体的物质的量不再变化;⑥单位时间消耗amolA,同时生成2amolC;⑦A,B,C的分子数目比为1∶3∶2
 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是①C的生成速率与C的分解速率相等;②单位时间内amolA生成,同时生成3amolB;③A,B,C的浓度不再变化;④混合气体的总压强不再变化;⑤混合气体的物质的量不再变化;⑥单位时间消耗amolA,同时生成2amolC;⑦A,B,C的分子数目比为1∶3∶2
| A.②⑤⑥ | B.①③⑥ | C.②⑥⑦ | D.②⑤⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知: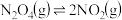 ,将装有
,将装有 (无色)和
(无色)和 混合气体的密闭烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论能说明该反应已经达到化学平衡状态的是:
混合气体的密闭烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论能说明该反应已经达到化学平衡状态的是:
①烧瓶内气体的质量不再变化 ②烧瓶内气体的颜色不再加深
③ ④烧瓶内气体的压强不再变化
④烧瓶内气体的压强不再变化
⑤混合气体密度保持不变 ⑥ 的浓度与
的浓度与 的浓度相等
的浓度相等
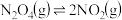 ,将装有
,将装有 (无色)和
(无色)和 混合气体的密闭烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论能说明该反应已经达到化学平衡状态的是:
混合气体的密闭烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论能说明该反应已经达到化学平衡状态的是:①烧瓶内气体的质量不再变化 ②烧瓶内气体的颜色不再加深
③
 ④烧瓶内气体的压强不再变化
④烧瓶内气体的压强不再变化⑤混合气体密度保持不变 ⑥
 的浓度与
的浓度与 的浓度相等
的浓度相等| A.②④ | B.①③⑥ | C.②③ | D.⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中错误的是
| A.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+ 2CO2(g)在低温下能自发进行,则该反应的△H<0 |
| B.NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的△H >0 |
| C.若△H<0,△S>0,化学反应在任何温度下都能自发进行 |
| D.加入合适的催化剂能降低反应活化能,从而改变反应的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,某密闭容器中加入足量的碳酸钙,发生反应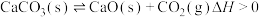 达到平衡,下列说法
达到平衡,下列说法不正确 的是
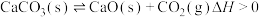 达到平衡,下列说法
达到平衡,下列说法A.将体积缩小为原来的一半,当体系再次达到平衡时, 的浓度不变 的浓度不变 |
| B.若温度升高,平衡正向移动,平衡常数增大 |
| C.该反应为吸热反应,高温能自发进行 |
| D.保持容器体积不变,充入He,平衡逆移 |
您最近一年使用:0次


 Fe3O4(s)+4H2(g),能表明反应达到平衡状态的叙述是
Fe3O4(s)+4H2(g),能表明反应达到平衡状态的叙述是
 。下列判断中正确的是
。下列判断中正确的是 ,则反应一定能自发向右进行
,则反应一定能自发向右进行 ,对于体积不变的容器,升高温度,气体平均相对分子质量不变
,对于体积不变的容器,升高温度,气体平均相对分子质量不变 ,往含mmol气体的平衡体系中充入nmolB,则达到平衡时气体总物质的量小于
,往含mmol气体的平衡体系中充入nmolB,则达到平衡时气体总物质的量小于


