铁及其化合物在生产、生活中有着广泛的应用。
(1)钢(一种铁碳合金)是用量最大、用途最广的合金。钢的硬度比纯铁_______ (填“大” 或“小”)。
(2)高铁酸钾(K2FeO4)是一种新型高效、无毒的多功能水处理剂,K2FeO4中Fe的化合价为_______ 。
(3)若一定量的普通铁粉和水蒸气在高温下反应生成44.8 LH2(标准状况),则转移电子的物质的量为_______ mol。
(4)FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的目的是_______ 。
(5)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,该反应的离子方程式为_______ ,检验反应后的溶液中是否还有三价铁离子的试剂是_______ 。
(6)聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,含少量碳及二氧化硅)为原料制备的流程如下:
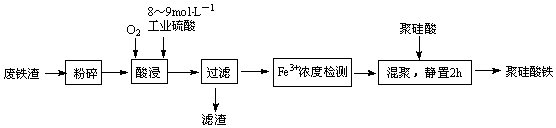
①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为_______ 。
②酸浸时,通入O2的目的是_______ 。
③“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7,标准溶液测定Fe2+的量(Cr2O 被还原为Cr3+),则SnCl2、Fe2+和Cr3+三者中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+三者中还原性最强的是_______ 。
(1)钢(一种铁碳合金)是用量最大、用途最广的合金。钢的硬度比纯铁
(2)高铁酸钾(K2FeO4)是一种新型高效、无毒的多功能水处理剂,K2FeO4中Fe的化合价为
(3)若一定量的普通铁粉和水蒸气在高温下反应生成44.8 LH2(标准状况),则转移电子的物质的量为
(4)FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的目的是
(5)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,该反应的离子方程式为
(6)聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,含少量碳及二氧化硅)为原料制备的流程如下:

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为
②酸浸时,通入O2的目的是
③“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7,标准溶液测定Fe2+的量(Cr2O
 被还原为Cr3+),则SnCl2、Fe2+和Cr3+三者中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+三者中还原性最强的是
更新时间:2021-02-08 16:05:00
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列物质的颜色及状态。
①Na2O___________ ;②Na2O2 ___________ ;③Na2CO3 ___________ ;④FeO___________ ;
⑤Fe2O3___________ ;⑥Fe3O4___________ ;⑦Fe(OH)2___________ ;⑧Fe(OH)3___________ ;
⑨Na___________ ;⑩铁粉___________ 。
①Na2O
⑤Fe2O3
⑨Na
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列关于铁元素及其化合物的知识:
(1)将 NaOH 溶液滴入 FeSO4溶液中,能观察到的现象是___ ,请写出产物颜色变化时发生的反应方程式___ 。
(2)实验室配制氯化铁溶液时,通常应将氯化铁固体溶解在加有少量___ 的水中; FeCl2溶液在空气中放置一段时间后,逐渐变成浅黄色,其原因是___ 。(用离子方程式表示)
(3)在常温下,铁与水并不起反应,但在高温下,铁与水蒸气可发生反应。该反应的化学方程式_________________ ,该反应中的还原剂是___ ,氧化剂是___ 。
(4)在 100mL18mol/L的浓硫酸中加入过量的铁片,加热使之充分反应,产生的气体在标准状况下的体积可能是___ 。
A.40.32L B.25.76L C.20.16L D.6.72L
(1)将 NaOH 溶液滴入 FeSO4溶液中,能观察到的现象是
(2)实验室配制氯化铁溶液时,通常应将氯化铁固体溶解在加有少量
(3)在常温下,铁与水并不起反应,但在高温下,铁与水蒸气可发生反应。该反应的化学方程式
(4)在 100mL18mol/L的浓硫酸中加入过量的铁片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B.25.76L C.20.16L D.6.72L
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】金属及其化合物在许多领域有着广泛的应用。
①绿矾 是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为
是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为___________ ;若将少量 固体加入
固体加入 溶液中,发生的反应为
溶液中,发生的反应为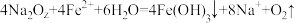 ,反应中被氧化的元素为
,反应中被氧化的元素为___________ (填元素符号)
(2)“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业味精”, 是两性氧化物,与强碱反应生成钒酸盐(阴离子为
是两性氧化物,与强碱反应生成钒酸盐(阴离子为 ),溶于强酸生成含钒氧离子(
),溶于强酸生成含钒氧离子( )的盐。请写出
)的盐。请写出 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
分别与烧碱溶液和稀硫酸反应生成的盐的化学式:___________ 、___________ 。
(3)科学研究表明,向 和
和 的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为
的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为 的特殊磁流体材料。
的特殊磁流体材料。
①在加热条件下,请写出生成难溶于水的 的化学方程式:
的化学方程式:___________ 。
②若 ,则
,则 中
中 和
和 的物质的量之比为
的物质的量之比为___________ 。
①绿矾
 是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为
是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH溶液可观察到的现象为 固体加入
固体加入 溶液中,发生的反应为
溶液中,发生的反应为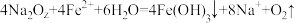 ,反应中被氧化的元素为
,反应中被氧化的元素为(2)“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业味精”,
 是两性氧化物,与强碱反应生成钒酸盐(阴离子为
是两性氧化物,与强碱反应生成钒酸盐(阴离子为 ),溶于强酸生成含钒氧离子(
),溶于强酸生成含钒氧离子( )的盐。请写出
)的盐。请写出 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
分别与烧碱溶液和稀硫酸反应生成的盐的化学式:(3)科学研究表明,向
 和
和 的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为
的混合溶液中加入适量KOH,在一定条件下可制得化学式通式为 的特殊磁流体材料。
的特殊磁流体材料。①在加热条件下,请写出生成难溶于水的
 的化学方程式:
的化学方程式:②若
 ,则
,则 中
中 和
和 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】某兴趣小组利用铁在氧气中燃烧的产物磁性氧化铁做如下实验:
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为___________ 。将磁性氧化铁完全溶于较浓的盐酸中,得到棕黄色的浓溶液,其反应的离子方程式为___________ 取少量所得溶液加入双氧水,其反应的离子方程式为___________ 。
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为___________ ;静置后向上层清液中加入NaOH溶液,并放置一段时间,观察到的实验现象为___________ 。
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为___________ 。写出高炉炼铁中一氧化碳还原氧化铁的化学方程式:___________ 。
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是____ (填字母代号)。
(2)向沸水中逐滴滴加lmol/LFeCl3溶液,至____ ,该分散系中粒子直径的范围是____ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:____ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:首先取少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是____ ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,____ (填实验操作,下同)、洗涤、干燥,称量沉淀质量为43.05g。则待测溶液中,FeCl3的物质的量浓度为____ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是____ (填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①____ ;②____ ;③____ ;④____ 。
B.请写出通入⑥的化学方程式:_____ 。
(1)所含铁元素既有氧化性又有还原性的物质是
| A.Fe | B.FeCl2 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①
B.请写出通入⑥的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学研究主要用的是实验方法,所以学习化学离不开实验。请回答:
(1)在试管里注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以观察到试管中产生白色絮状沉淀,发生反应的离子方程式是____________________ 。生成的沉淀迅速变成灰绿色,最后变成红褐色,发生反应的化学方程式为_______________________ 。
(2)实验室在保存含Fe2+的溶液时,经常向其中加入铁粉,其目的是___________ 。为了检验该溶液是否变质,应采用的实验操作及现象是__________________________ 。
(3)除去铁粉中混有的铝粉应选用的试剂为_____ ,发生反应的离子方程式为_____________ 。
(1)在试管里注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以观察到试管中产生白色絮状沉淀,发生反应的离子方程式是
(2)实验室在保存含Fe2+的溶液时,经常向其中加入铁粉,其目的是
(3)除去铁粉中混有的铝粉应选用的试剂为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)很多含氯物质都能做消毒剂。液氯可以用于饮用水消毒,但是消毒后的水中可能产生危害人体健康的有机氯化物。世界各国陆续开发新型自来水消毒剂,下列物质可以用于自来水消毒的有___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是___ (写出化学式)。高铁酸钠(Na2FeO4)也可以用于作自来水处理剂,高铁酸钠处理过的水中含有氢氧化铁胶体,则高铁酸钠作自来水处理剂的优点是___ 。
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:___ 。
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯= ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯=
 ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。

请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂______________________ ;
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板_________________________ 。
(2)吸收剂X的化学式为___________________ ;氧化剂Y的化学式为____________ 。
(3)碱性条件下反应①的离子方程式为____________________________________ 。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因________________ 。
(5)K2FeO4在水溶液中易发生反应:4FeO42+10H2O 4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用__________________ (填序号)。
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42-+CrO2-+2H2O CrO42-+Fe(OH)3↓+OH-
CrO42-+Fe(OH)3↓+OH-
②2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
③Cr2O72-+6Fe2++14H+ 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O
现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为____________ 。

请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板
(2)吸收剂X的化学式为
(3)碱性条件下反应①的离子方程式为
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因
(5)K2FeO4在水溶液中易发生反应:4FeO42+10H2O
 4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用| A.H2O |
| B.稀KOH溶液、异丙醇 |
| C.NH4Cl溶液、异丙醇 |
| D.Fe(NO3)3溶液、异丙醇 |
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42-+CrO2-+2H2O
 CrO42-+Fe(OH)3↓+OH-
CrO42-+Fe(OH)3↓+OH-②2CrO42-+2H+
 Cr2O72-+H2O
Cr2O72-+H2O③Cr2O72-+6Fe2++14H+
 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸盐(K2FeO4)在能源、环保等方面有着广泛的用途.湿法、干法制备高铁酸盐的原理如下表所示.
(1)写出干法制备K2FeO4的化学方程式为,_____________________________________ ,该
反应中氧化剂与还原剂的物质的量之比为_______________________________ 。
(2)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为_______________________________ ,它能净水的原因是_____________________________________ 。
(3)在实验室配制Fe(NO3)3溶液时,若用蒸馏水直接配制,所得溶液往往较浑浊,其原因是(用离子方程式表示)____________________________ ,因此,正确的配制操作是在溶液中加入少量的(填试剂名称)_____________ ,其目的是__________________________ 。
(4)Fe2O3是一种____________ 色的氧化物,写出它和盐酸反应的离子方程式___________ 。
(5)检验Fe3+的方法很多,写出其中的一种检验方法_______________________________ 。
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
反应中氧化剂与还原剂的物质的量之比为
(2)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为
(3)在实验室配制Fe(NO3)3溶液时,若用蒸馏水直接配制,所得溶液往往较浑浊,其原因是(用离子方程式表示)
(4)Fe2O3是一种
(5)检验Fe3+的方法很多,写出其中的一种检验方法
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】常用饱和氯化铁溶液腐蚀铜制印刷电路板,反应化学方程式__________ .
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答问题。
(1)补齐物质与其用途的连线_________ 。
(2)上述 的用途,利用了它的
的用途,利用了它的___________ (填“物理”或“化学”)性质。
(3) 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:___________ 。
| 用途 物质 |
| A.去除某些有机溶剂中的水分 ———— a.Na B.84消毒液的有效成分 b.Na2CO3 C.厨房中的食用䂸 c.Fe3O4 D.打印机墨粉中的磁性成分 d.NaClO E.自来水消毒剂 e.Fe2O3 F.治疗酸酸过多 f.Na2O2 G.用于处理废旧铜板 g.ClO2 H.红色油漆涂料 h.FeCl3 I.呼吸面罩供氧剂 i.NaHCO3 |
(2)上述
 的用途,利用了它的
的用途,利用了它的(3)
 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电池与工农业生产、日常生活有着密切的关联。请回答下列问题:
(1)燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。
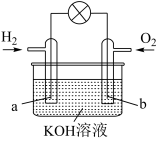
①负极是_______ (填“a”或“b”),该电极上发生_______ (填“氧化”或“还原”)反应。
②b极发生的电极反应式是_______ 。
③标准状况下,消耗11.2LH2时,转移的电子数为_______ 。
(2)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法正确的是_______(填字母)。

(3)铁及其化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:_______ 。
(1)燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①负极是
②b极发生的电极反应式是
③标准状况下,消耗11.2LH2时,转移的电子数为
(2)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法正确的是_______(填字母)。

| A.电子由铝制易拉罐经导线流向碳棒 |
| B.在碳棒上有气体生成,该气体可能为氢气 |
| C.铝质易拉罐逐渐被腐蚀,说明铝失去电子 |
| D.扬声器发声,说明该装置将电能转化为化学能 |
您最近半年使用:0次



