络氨铜是一种常用的农药中间体。为充分利用资源,变废为宝,在实验室中探究采用机床切削含铁的粗铜屑制备产品[Cu(NH3)4]SO4·H2O(能溶于水,难溶于乙醇),具体流程如图:回答下列问题:
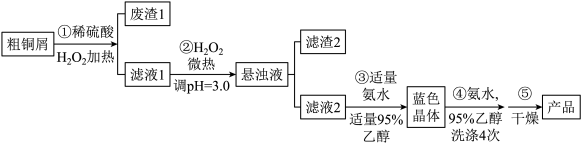
(1)步骤①中与产品有关的反应离子方程式是_______ 。
(2)步骤②中调节pH至3.0左右,主要目的是_______ 。检验悬浊液 中杂质离子沉淀完全的方法是_______ 。
(3)步骤③中加入95%的乙醇的作用是_______ 。
(4)步骤⑤正确的干燥方法是_______ (填标号)。
A.在烘箱中烘干 B.自然风干或晾干 C.在盛有浓硫酸的干燥器中干燥
(5)书写反应③中得到蓝色晶体的离子方程式_______ 。

(1)步骤①中与产品有关的反应离子方程式是
(2)步骤②中调节pH至3.0左右,主要目的是
(3)步骤③中加入95%的乙醇的作用是
(4)步骤⑤正确的干燥方法是
A.在烘箱中烘干 B.自然风干或晾干 C.在盛有浓硫酸的干燥器中干燥
(5)书写反应③中得到蓝色晶体的离子方程式
更新时间:2021-02-01 12:01:28
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
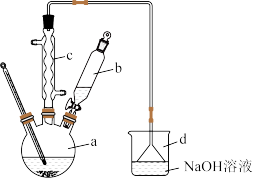
I.合成步骤:在a中加入15mL无水苯和少量铁屑。在b中小心加入5.0mL液溴。打开活塞,向a中滴入液溴,发生反应。请回答下列问题:
(1)实验室制取溴苯的化学方程式为_________________________ 。
(2)本实验应控制适宜的温度范围为 (填标号)。
(3)装置d的作用除了能防倒吸外,还有______________ 。
Ⅱ.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:
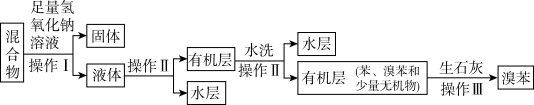
(4)操作Ⅱ所需主要玻璃仪器有_____________ 。
(5)设计实验检验水洗是否达到目的:_______________________ 。
(6)操作Ⅲ的名称为_________ 。若经过操作Ⅲ后得纯溴苯11.30g,则溴苯的产率是_________ (计算结果保留2位有效数字)。
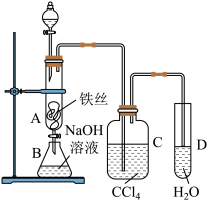
(7)也可以改为如下装置制备溴苯,装置C中盛放CCl4的作用是________ ;要证明苯和液溴发生的是取代,而不是加成反应,可向试管D中加入AgNO3溶液;另一种验证的方法是向试管D中加入_____ 。
苯 | 溴 | 溴苯 | |
密度g·cm-3 | 0.88 | 3.20 | 1.50 |
沸点/°C | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |

I.合成步骤:在a中加入15mL无水苯和少量铁屑。在b中小心加入5.0mL液溴。打开活塞,向a中滴入液溴,发生反应。请回答下列问题:
(1)实验室制取溴苯的化学方程式为
(2)本实验应控制适宜的温度范围为 (填标号)。
| A.>156°C | B.59°C- 80°C | C.<59°C | D.80°C- 156°C |
Ⅱ.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:

(4)操作Ⅱ所需主要玻璃仪器有
(5)设计实验检验水洗是否达到目的:
(6)操作Ⅲ的名称为
(7)也可以改为如下装置制备溴苯,装置C中盛放CCl4的作用是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学小组对当地化工厂排出的废水成分进行研究,经检测,废水呈酸性,且其中含有大量 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。

已知:NaCl、 在不同温度下的溶解度如下(g/100g水)。
在不同温度下的溶解度如下(g/100g水)。
回答下列问题:
(1)下列离子一定不能大量存在于该废水中的是___________(填标号)
(2)蓝色沉淀的成分是___________ (填化学式,下同);试剂c为___________ ,“操作2”需用到的玻璃仪器主要有烧杯、___________ 。
(3)向“溶液2”中加入盐酸,发生反应的离子方程式为___________ 。
(4)“溶液3”中溶质为NaCl、 ,操作3为___________(填编号)。
,操作3为___________(填编号)。
 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。
已知:NaCl、
 在不同温度下的溶解度如下(g/100g水)。
在不同温度下的溶解度如下(g/100g水)。| 温度物质 |  | NaCl |
| 10℃ | 80.5 | 35.7 |
| 100℃ | 175 | 39.1 |
(1)下列离子一定不能大量存在于该废水中的是___________(填标号)
A. | B. | C. | D. |
(3)向“溶液2”中加入盐酸,发生反应的离子方程式为
(4)“溶液3”中溶质为NaCl、
 ,操作3为___________(填编号)。
,操作3为___________(填编号)。| A.蒸发结晶 | B.蒸发浓缩、趁热过滤 | C.冷却结晶 | D.蒸发浓缩、冷却结晶 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】对废银合金触电材料进行分离回收既节约矿物资源,又可以减少环境污染。某废银合金触电材料含Ag、Cu、Sn等,现欲利用以下工艺流程回收其中的金属资源。

回答下列问题:
(1)“加热溶解”时Cu发生的离子方程式为___ 。
(2)“加热溶解”时温度常控制在50℃左右,温度不宜过高也不宜过低的原因为___ 。
(3)“酸溶解”过程中会产生少量遇空气变为红棕色的无色气体,则“酸溶解”过程主要的化学方程式为___ 。
(4)检验Sn(OH)4沉淀是否洗涤干净的方法是___ 。
(5)若想由CuCl2溶液得到无水CuCl2固体,则需进行的实验操作为___ 。

回答下列问题:
(1)“加热溶解”时Cu发生的离子方程式为
(2)“加热溶解”时温度常控制在50℃左右,温度不宜过高也不宜过低的原因为
(3)“酸溶解”过程中会产生少量遇空气变为红棕色的无色气体,则“酸溶解”过程主要的化学方程式为
(4)检验Sn(OH)4沉淀是否洗涤干净的方法是
(5)若想由CuCl2溶液得到无水CuCl2固体,则需进行的实验操作为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高纯无水 是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是
是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是 ,含少量
,含少量 杂质)为原料,以乙二醇为溶剂,采用氨络合法制备
杂质)为原料,以乙二醇为溶剂,采用氨络合法制备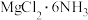 (白色块状固体或粉末,溶于水,易潮解),再转化为无水
(白色块状固体或粉末,溶于水,易潮解),再转化为无水 的新工艺,其流程图如图:
的新工艺,其流程图如图:
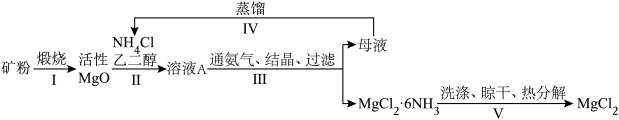
已知:①常压下, 的初始分解温度为399℃,
的初始分解温度为399℃, 的初始分解温度为896℃;
的初始分解温度为896℃;
②煅烧温度是影响MgO活性的关键因素;
③乙二醇的沸点197.3℃。
(1)步骤Ⅰ中工业上一般不选择800℃以上来完成这一步原因是_____ 。
(2)步骤Ⅱ中反应方程式为_____ 。
(3)步骤IV中蒸馏的目的是____ 。
(4)步骤V中的洗涤是为了除去晶体表面的杂质,最好选用下列哪种作为洗涤剂____ 。
A.氯化铵饱和溶液 B.乙二醇
C.冷水 D.氨气饱和的乙醇溶液
(5)实验过程需要测定 浓度,可通过EDTA滴定(与
浓度,可通过EDTA滴定(与 以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→
以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→___ →e(用操作步骤前的字母表示)。
a.移取25.00mL待测溶液于锥形瓶中,加入10mL水,摇匀
b.用0.1000mol/L的EDTA标准溶液滴定至终点,记录消耗标准液的体积
c.称取一定质量的样品,配制250mL待测溶液
d.滴加1-2滴指示剂
e.舍弃不可靠数据、取平均值等
 是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是
是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是 ,含少量
,含少量 杂质)为原料,以乙二醇为溶剂,采用氨络合法制备
杂质)为原料,以乙二醇为溶剂,采用氨络合法制备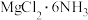 (白色块状固体或粉末,溶于水,易潮解),再转化为无水
(白色块状固体或粉末,溶于水,易潮解),再转化为无水 的新工艺,其流程图如图:
的新工艺,其流程图如图:
已知:①常压下,
 的初始分解温度为399℃,
的初始分解温度为399℃, 的初始分解温度为896℃;
的初始分解温度为896℃;②煅烧温度是影响MgO活性的关键因素;
③乙二醇的沸点197.3℃。
(1)步骤Ⅰ中工业上一般不选择800℃以上来完成这一步原因是
(2)步骤Ⅱ中反应方程式为
(3)步骤IV中蒸馏的目的是
(4)步骤V中的洗涤是为了除去晶体表面的杂质,最好选用下列哪种作为洗涤剂
A.氯化铵饱和溶液 B.乙二醇
C.冷水 D.氨气饱和的乙醇溶液
(5)实验过程需要测定
 浓度,可通过EDTA滴定(与
浓度,可通过EDTA滴定(与 以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→
以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→a.移取25.00mL待测溶液于锥形瓶中,加入10mL水,摇匀
b.用0.1000mol/L的EDTA标准溶液滴定至终点,记录消耗标准液的体积
c.称取一定质量的样品,配制250mL待测溶液
d.滴加1-2滴指示剂
e.舍弃不可靠数据、取平均值等
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硼酸(H3BO3)微溶于水,其水溶液显弱酸性,对人体的受伤组织有防腐作用。以硼镁矿(含Mg2B2O5 H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及碱式碳酸镁的工艺流程如图:
H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及碱式碳酸镁的工艺流程如图:

(1)“滤渣1”的主要成分有_______ 。
(2)在“过滤2”前,将溶液pH调节至3.5,目的是_______ 。
(3)H3BO3(一元弱酸)与足量的NaOH溶液反应,生成 NaB(OH)4。写出H3BO3的电离方程式:_______ 。
(4)用滴定法测定硼酸晶体的纯度。研究结果表明,用0.1mol·L-1NaOH溶液直接滴定硼酸溶液的如曲线①所示,向硼酸溶液中加入多元醇后再滴定如曲线②所示。

请分析,能否用强碱直接滴定硼酸溶液,_______ (填“能”或“不能”),理由是:_______ 。选择合适的方法进行滴定,取5g晶体,溶于水配成1L溶液,取出20mL进行滴定,指示剂为_______ 。平行实验三次,平均消耗0.1mol·L-1NaOH溶液14.10mL,则硼酸晶体的纯度为_______ 。
(5)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为_______ 。
 H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及碱式碳酸镁的工艺流程如图:
H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及碱式碳酸镁的工艺流程如图:
(1)“滤渣1”的主要成分有
(2)在“过滤2”前,将溶液pH调节至3.5,目的是
(3)H3BO3(一元弱酸)与足量的NaOH溶液反应,生成 NaB(OH)4。写出H3BO3的电离方程式:
(4)用滴定法测定硼酸晶体的纯度。研究结果表明,用0.1mol·L-1NaOH溶液直接滴定硼酸溶液的如曲线①所示,向硼酸溶液中加入多元醇后再滴定如曲线②所示。

请分析,能否用强碱直接滴定硼酸溶液,
(5)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】六氟锑酸锂 可用作锂离子电池的电解质锂盐,一种以锑白
可用作锂离子电池的电解质锂盐,一种以锑白 为原料,制备
为原料,制备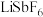 工艺流程如图所示:
工艺流程如图所示:
(1)请写出基态 原子价层电子排布式
原子价层电子排布式_________________ 。
(2)试剂 的化学式为
的化学式为_____________ ;根据流程和元素周期律推断 是
是_____________ 氧化物。
(3)“氧化”时,将溶液升至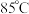 反应,温度不宜过高的原因是
反应,温度不宜过高的原因是_________________________ ;写出“氧化”步骤反应的离子方程式_____________________________ 。
(4)“酸溶”步骤一般使用聚四氟乙烯设备,不能使用金属或陶瓷设备,其原因是_____________ 。
(5)“操作Ⅴ"步骤为_________________ ;“过滤Ⅱ”所得的“母液”返回到_____________ 工序。
 可用作锂离子电池的电解质锂盐,一种以锑白
可用作锂离子电池的电解质锂盐,一种以锑白 为原料,制备
为原料,制备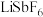 工艺流程如图所示:
工艺流程如图所示: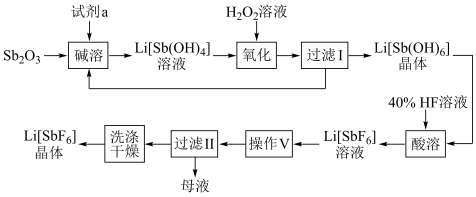
(1)请写出基态
 原子价层电子排布式
原子价层电子排布式(2)试剂
 的化学式为
的化学式为 是
是(3)“氧化”时,将溶液升至
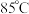 反应,温度不宜过高的原因是
反应,温度不宜过高的原因是(4)“酸溶”步骤一般使用聚四氟乙烯设备,不能使用金属或陶瓷设备,其原因是
(5)“操作Ⅴ"步骤为
您最近一年使用:0次



