几种主族元素在周期表中的位置如下
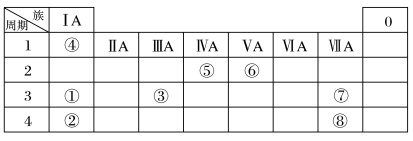
根据上表回答下列问题:
(1)⑥元素的氢化物的电子式是_______ 。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_______ ,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式),①与③最高价氧化物对应水化物反应的离子方程式为_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于 ⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(6)①和④形成的化合物是_______ (填“离子”或“共价”)化合物。

根据上表回答下列问题:
(1)⑥元素的氢化物的电子式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于 ⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(6)①和④形成的化合物是
20-21高一上·广东汕头·期末 查看更多[3]
广东省汕头市潮阳区2020-2021学年高一上学期期末考试化学试题(已下线)第1章 物质结构 元素周期律(基础过关卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)云南省昆明市四川师范大学昆明实验学校安宁校区2020-2021学年高二下学期入学化学试题
更新时间:2021-02-23 10:12:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】2019年诺贝尔化学奖颁给了三位为锂离子电池发展做出巨大贡献的科学家,锂离子电池广泛应用于手机、笔记本电脑等。
(1)锂元素在元素周期表中的位置:_________________ 。
(2)氧化锂(Li2O)是制备锂离子电池的重要原料,氧化锂的电子式为_____________ 。
(3)近日华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出了石墨烯电池,电池反应式为LIxC6+Li1-x C6+LiCoO2,其工作原理如图。
C6+LiCoO2,其工作原理如图。

①石墨烯的优点是提高电池的能量密度,石墨烯为层状结构,层与层之间存在的作用力是_______ 。
②锂离子电池不能用水溶液做离子导体的原因是___________ (用离子方程式表示)。
③锂离子电池放电时正极的电极反应式为________________ 。
④请指出使用锂离子电池的注意问题____________________ 。(回答一条即可)
(1)锂元素在元素周期表中的位置:
(2)氧化锂(Li2O)是制备锂离子电池的重要原料,氧化锂的电子式为
(3)近日华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出了石墨烯电池,电池反应式为LIxC6+Li1-x
 C6+LiCoO2,其工作原理如图。
C6+LiCoO2,其工作原理如图。
①石墨烯的优点是提高电池的能量密度,石墨烯为层状结构,层与层之间存在的作用力是
②锂离子电池不能用水溶液做离子导体的原因是
③锂离子电池放电时正极的电极反应式为
④请指出使用锂离子电池的注意问题
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)写出CO2的结构式___________ ;CCl4的电子式___________ 。
(2)写出NaHSO4在水中的电离方程式___________ 。
(3)写出CO2通入饱和Na2CO3溶液反应的离子方程式___________ 。
(4)用电子式表示K2O的形成过程___________ 。
(1)写出CO2的结构式
(2)写出NaHSO4在水中的电离方程式
(3)写出CO2通入饱和Na2CO3溶液反应的离子方程式
(4)用电子式表示K2O的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空:
(1)写出 的结构式
的结构式___________ 。
(2)写出 的电子式
的电子式___________ 。
(3)将过量的 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式___________ 。
(4)向 溶液中,缓慢滴加
溶液中,缓慢滴加 溶液至过量,现象是
溶液至过量,现象是___________ 。
(5)金属钠受热燃烧的化学方程式为___________
(6)将铜片投入 溶液中反应的离子方程式
溶液中反应的离子方程式___________ 。
(7)将一定量 投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:
投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:___________ 。
(8)向 溶液中滴入
溶液中滴入 溶液,可观察到的现象是
溶液,可观察到的现象是___________ 。
(1)写出
 的结构式
的结构式(2)写出
 的电子式
的电子式(3)将过量的
 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式(4)向
 溶液中,缓慢滴加
溶液中,缓慢滴加 溶液至过量,现象是
溶液至过量,现象是(5)金属钠受热燃烧的化学方程式为
(6)将铜片投入
 溶液中反应的离子方程式
溶液中反应的离子方程式(7)将一定量
 投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:
投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:(8)向
 溶液中滴入
溶液中滴入 溶液,可观察到的现象是
溶液,可观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)在最高价氧化物的水化物中,酸性最强的化合物的名称 是______ ,碱性最强的化合物的化学式 是_______ 。
(2)⑤⑦形成化合物的电子式___ 。②形成的最高价氧化物的结构式____ 。
(3)最高价氧化物是两性氧化物的元素 其元素符号是____ ;写出它的氢氧化物与 ⑧的最高价氧化物的水化物反应的离子方程式
⑧的最高价氧化物的水化物反应的离子方程式________ 。
(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是______ 。
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:____________ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的
(2)⑤⑦形成化合物的电子式
(3)最高价氧化物是两性氧化物的
 ⑧的最高价氧化物的水化物反应的离子方程式
⑧的最高价氧化物的水化物反应的离子方程式(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:

(1)在这10种元素中,非金属性最强的是______ (填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为__________ ,元素②与⑨形成的18e﹣化合物的电子式______ ;
(3)比较元素⑦⑧形成的气态氢化物的稳定性:__ >__ (用化学式表示);
(4)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式_____ ;
(5)元素④和③形成的化合物属于______ 化合物,用电子式表示其形成过程____ 。

(1)在这10种元素中,非金属性最强的是
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为
(3)比较元素⑦⑧形成的气态氢化物的稳定性:
(4)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式
(5)元素④和③形成的化合物属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期律是对元素性质的规律性总结,元素周期表是这种规律的呈现形式。利用元素周期律可以推测一些未知元素可能的性质。根据你所学的周期律,回答下列问题:
(1)元素周期表有几个周期,几个主族。正确选项是
(2)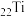 被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
(3)元素周期表中,第三电子层有一个未成对电子的元素有___________种(填序号)。
(1)元素周期表有几个周期,几个主族。正确选项是
| A.6,7 | B.7,7 | C.7,18 | D.7,14 |
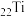 被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
被誉为21世纪明星金属,其最外层电子数为___________(填序号)。| A.1个 | B.2个 | C.3个 | D.5个 |
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表给出14~17号元素的一些性质,请回答:
(1)它们所形成的氢化物中稳定性最差的是________ ,还原性最差的是_____ 。
(2)四种元素的非金属性随着元素原子序数的递增而逐渐_____________________ ,试从原子结构的角度加以解释____________ 。
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由___________ 。
| 14Si | 15P | 16S | 17Cl | |
| 单质与H2反应的条件 | 高温 | 磷蒸气与H2能反应 | 加热 | 光照或点燃时发生爆炸 |
| 最高价氧化物的水化物 | H4SiO4弱酸 | H3PO4中强酸 | H2SO4强酸 | HClO4最强含氧酸 |
(1)它们所形成的氢化物中稳定性最差的是
(2)四种元素的非金属性随着元素原子序数的递增而逐渐
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】N、Mg及有关物质在生产、科研中有重要应用。回答下列问题:
(1)原子的质量数等于质子数与中子数之和。能用于研究古人类食物结构的 的质子数为
的质子数为______ 。中子数为______ ;N位于元素周期表第______ 周期第ⅤA族。
(2)与同主族的Be相比,Mg的原子半径比Be的______ (填“大”或“小”)。
(3)N的最高价氧化物对应的水化物的化学式为______ ,其酸性比同周期的C的最高价氧化物对应的水化物的酸性______ (填“强”或“弱”)。
(4)Mg与水反应时,很缓慢地放出气泡,并生成使酚酞溶液变红的物质,该物质的化学式为______ 。而Na与水的反应比Mg与水的反应更______ (填“剧烈”或“缓慢”),因此,Mg的金属性比Na的______ (填“强”或“弱”)。
(5)工业上合成 的原料为
的原料为 和
和 。
。 的结构式为
的结构式为______ ; 属于
属于______ (填“离子”或“共价”)化合物。
(1)原子的质量数等于质子数与中子数之和。能用于研究古人类食物结构的
 的质子数为
的质子数为(2)与同主族的Be相比,Mg的原子半径比Be的
(3)N的最高价氧化物对应的水化物的化学式为
(4)Mg与水反应时,很缓慢地放出气泡,并生成使酚酞溶液变红的物质,该物质的化学式为
(5)工业上合成
 的原料为
的原料为 和
和 。
。 的结构式为
的结构式为 属于
属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在科技发展中发挥着重要的作用。完成下列填空:
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指_______ ,58是指_______ 。
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为_______ 。
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是_______ ,SiH4的空间构型为_______ 。
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为_______ ,T的电子式为_______ 。
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是_______ (选填编号)
a.SiO + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.
c.SiH4 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑
d.Si+O2 SiO2;C+O2
SiO2;C+O2 CO2
CO2
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是
a.SiO
 + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.

c.SiH4
 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑d.Si+O2
 SiO2;C+O2
SiO2;C+O2 CO2
CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列编号代表元素周期表中的一部分元素,用化学式回答下列问题:
(1)①、③、⑤的最高价氧化物的水化物碱性由强到弱顺序为___________ (填化学式,下同)。
(2)②、③、④形成的简单阳离子半径由大到小的顺序是_______________ 。
(3)⑨和⑩的最高价氧化物对应的水化物化学式为_______ 和_________ 。①在氧气中点燃生成淡黄色的固体,该固体的电子式为_______________ ,①能够与水剧烈反应,请写出该反应的化学方程式_______________ ,将元素⑩的单质通入NaBr溶液中,反应的离子方程式为_______________ 。
(4)⑥、⑦、⑧三种元素形成的气态氢化物的稳定性排序是____________ (填化学式,下同),三种元素非金属性由强到弱的顺序为___________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑧ | |||||
| 三 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 四 | ② | ④ |
(1)①、③、⑤的最高价氧化物的水化物碱性由强到弱顺序为
(2)②、③、④形成的简单阳离子半径由大到小的顺序是
(3)⑨和⑩的最高价氧化物对应的水化物化学式为
(4)⑥、⑦、⑧三种元素形成的气态氢化物的稳定性排序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E是位于短周期的主族元素。已知:A、B、C、E在同一周期,在该周期元素中,A的原子半径最大,B的离子半径最小; A与B质子数之和是D质子数的3倍;C m- 、E (m-1)- 具有相同的电子层结构;热稳定性:H m D>H m C。依据上述信息用相应的化学用语回答下列问题:
(1)H m D m 的电子式为____________________
(2)C m- 、E (m-1)- 的还原性强弱顺序为:_________ ,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________ 。
(3)B单质与A的最高价氧化物对应水化物反应的化学方程式为:______________________ 。
(4)常温下,将CD m 通入H m C溶液中,有C析出,写出该过程的化学方程式__________________ 。
(5)在A、B、C、E单质中,符合下列转化关系的是___________ (填元素符号)。

(1)H m D m 的电子式为
(2)C m- 、E (m-1)- 的还原性强弱顺序为:
(3)B单质与A的最高价氧化物对应水化物反应的化学方程式为:
(4)常温下,将CD m 通入H m C溶液中,有C析出,写出该过程的化学方程式
(5)在A、B、C、E单质中,符合下列转化关系的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式 填空回答以下问题:
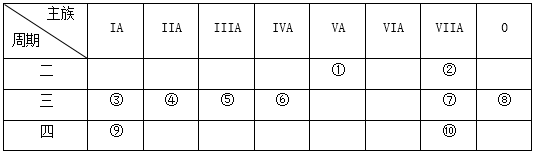
(1)在③~⑦中元素,原子半径最大的是_____________ ,其离子的结构示意图是__________________ 。
(2)表中的①~⑩中元素,非金属性最强的是_______ ,化学性质最稳定的是________ ,金属性最强的是__________ ,最高价氧化物的水化物的酸性最强的是(写该水化物的化学式)______________ 。
(3)⑦的氢化物的水溶液与①的氢化物的水溶液反应的离子方程式为___________________________ 。
(4)用一个化学反应说明⑦比⑩的单质化学性质活泼,写出反应的化学方程式:_____________________ 。

(1)在③~⑦中元素,原子半径最大的是
(2)表中的①~⑩中元素,非金属性最强的是
(3)⑦的氢化物的水溶液与①的氢化物的水溶液反应的离子方程式为
(4)用一个化学反应说明⑦比⑩的单质化学性质活泼,写出反应的化学方程式:
您最近一年使用:0次



