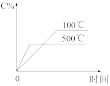
甲醇—水蒸气重整法所得氢气是电动汽车燃料电池的理想氢源。反应的热化学方程式如下:
反应Ⅰ

反应Ⅱ

 会损害燃料电池的交换膜。在压强、
会损害燃料电池的交换膜。在压强、 和
和 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下,
的起始浓度一定的条件下,催化反应相同时间,测得不同温度下, 的转化率、
的转化率、 的产率和
的产率和 的物质的量如图中实线所示(图中虚线表示相同条件下达平衡状态时的变化)。已知:
的物质的量如图中实线所示(图中虚线表示相同条件下达平衡状态时的变化)。已知: 的选择性
的选择性 。下列说法正确的是
。下列说法正确的是

反应Ⅰ


反应Ⅱ


 会损害燃料电池的交换膜。在压强、
会损害燃料电池的交换膜。在压强、 和
和 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下,
的起始浓度一定的条件下,催化反应相同时间,测得不同温度下, 的转化率、
的转化率、 的产率和
的产率和 的物质的量如图中实线所示(图中虚线表示相同条件下达平衡状态时的变化)。已知:
的物质的量如图中实线所示(图中虚线表示相同条件下达平衡状态时的变化)。已知: 的选择性
的选择性 。下列说法正确的是
。下列说法正确的是
A.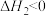 |
| B.210℃升温至270℃时,反应Ⅰ的活化能增大 |
| C.温度升高,反应Ⅰ的速率比反应Ⅱ增加的更多 |
| D.温度升高,n(CO)的实际值与平衡值相差越来越大,原因是催化剂对CO的选择性升高 |
20-21高三下·江苏扬州·开学考试 查看更多[2]
更新时间:2021-03-06 19:05:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验的操作和结论均正确的是
| 选项 | 实验操作 | 现象 | |
| A | Cu与足量浓硫酸反应,将反应混合物冷却后,再向反应器中加入冷水 | 溶液变蓝 | 验证生成 |
| B | 用惰性电极电解 和盐酸的混合溶液,电解一段时间后,在阳极附近滴加KI-淀粉溶液 和盐酸的混合溶液,电解一段时间后,在阳极附近滴加KI-淀粉溶液 | 阳极附近溶液变蓝 |  的还原性强于 的还原性强于 |
| C | 向 溶液中通入 溶液中通入 | 出现黑色沉淀 | 酸性: |
| D | 用玻璃棒蘸取 与水反应后的溶液,点在pH试纸中部 与水反应后的溶液,点在pH试纸中部 | pH试纸变蓝后褪色 |  与水反应生成 与水反应生成 的活化能小于 的活化能小于 分解的活化能 分解的活化能 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】甲烷与氧气直接选择性转化为甲醇是当今催化领域的“梦想反应”,科学家用 负载双组份催化剂(纳米金和
负载双组份催化剂(纳米金和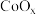 纳米簇)在室温和光照下完成了上述反应,选择性高达95%。机理如图A所示,下列说法不正确的是
纳米簇)在室温和光照下完成了上述反应,选择性高达95%。机理如图A所示,下列说法不正确的是
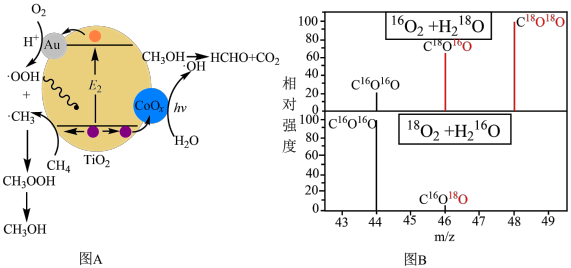
A.Au表面反应为: |
| B.图A中含碳微粒只存在2种杂化方式 |
C.有无催化剂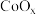 纳米簇对合成甲醇的产量无影响 纳米簇对合成甲醇的产量无影响 |
D.图B是通过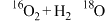 和 和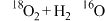 同位素示踪分析氧化甲烷过程中的产品质谱测试图,由图可知体系中产品 同位素示踪分析氧化甲烷过程中的产品质谱测试图,由图可知体系中产品 中氧主要来源于 中氧主要来源于 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下列实验操作(或实验操作和现象)能得到的结论正确的是
选项 | 实验操作(或实验操作和现象) | 结论 |
A | 向两支盛有5mL不同浓度的 | 反应物浓度越大,反应速率越大 |
B |
|
|
C |
| 验证AgC1的溶解度大于 |
D |
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
| B | 向5mL0.005mol/LFeCl3溶液中加入5mL0.010mol/LKSCN溶液,溶液呈红色,再滴加几滴KCl溶液,溶液颜色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) N2O4(g),△H<0,平衡向生成NO2方向移动 N2O4(g),△H<0,平衡向生成NO2方向移动 |
| D | 在密闭容器中有反应:A(?)+xB(g) 3C(g),达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的2倍,测得c(A)为0.2mol/L 3C(g),达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的2倍,测得c(A)为0.2mol/L | A为气体,x<2 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
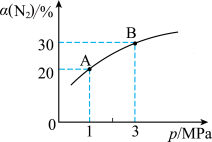
【推荐1】某温度下,发生反应
 ,
, 的平衡转化率(
的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
)与体系总压强(p)的关系如图所示。下列说法正确的是

 ,
, 的平衡转化率(
的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
)与体系总压强(p)的关系如图所示。下列说法正确的是
A.将1mol 和3mol 和3mol 置于1L密闭容器中发生反应,放出的热量小于92.4kJ 置于1L密闭容器中发生反应,放出的热量小于92.4kJ |
B.平衡状态由A到B时,平衡常数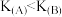 |
C.上述反应在达到平衡后,增大压强, 的产率减小 的产率减小 |
D.反应建立平衡后分离出部分 时,浓度商Q大于平衡常数K 时,浓度商Q大于平衡常数K |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
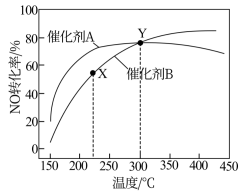
【推荐2】燃煤电厂锅炉尾气中含有的NO,以氨还原法除去,发生的反应如下:
反应Ⅰ:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) ΔH=-1627.7 kJ·mol-1
反应II:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-904.74 kJ·mol-1
在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列说法正确的是
反应Ⅰ:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) ΔH=-1627.7 kJ·mol-1
反应II:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-904.74 kJ·mol-1
在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列说法正确的是

| A.其他条件不变,升高温度,NO的平衡转化率一定降低 |
| B.催化剂B条件下,提高X点NO的转化率的方法可以是增大压强或延长反应时间 |
| C.在Y点所示条件下,使用催化剂A或催化剂B,反应均达平衡 |
| D.高效节能除去尾气中的NO,应选择催化剂B |
您最近半年使用:0次

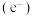 和空穴
和空穴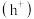 ,从而引发一系列反应的过程。一种光催化选择性氧化甲烷制备甲醇的机理如图所示,下列说法错误的是
,从而引发一系列反应的过程。一种光催化选择性氧化甲烷制备甲醇的机理如图所示,下列说法错误的是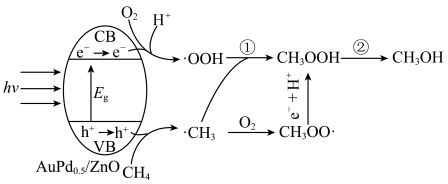
 的电子式为
的电子式为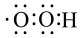
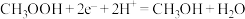
 可以加快该反应的速率,且不改变反应的焓变
可以加快该反应的速率,且不改变反应的焓变 溶液的试管中同时加入
溶液的试管中同时加入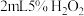 溶液,观察实验现象
溶液,观察实验现象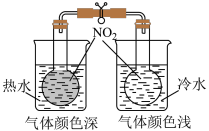
 为放热反应
为放热反应


 的水解程度比
的水解程度比 强
强 Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是