咔咯(corrole)及其配合物作为人工合成的大环配体之一,咔咯的合成及其与金属离子的配位化学备受关注。利用咔咯作为反应配体,可实现过渡金属离子的非常规氧化态,制备功能材料,探索新型催化剂,等等。下图(a)给出三(五氟苯基)咔咯分子(A)的示意图,简写为H3(tpfc)。它与金属离子结合时四个氮原子均参与配位。室温下,空气中,Cr(CO)6和A在甲苯中回流得到深红色晶体B(反应1),B显顺磁性,有效磁矩为1.72μB,其中金属离子的配位几何为四方锥;在惰性气氛保护下,B与三苯基膦(PPh3)和三苯基氧膦(OPPh3)按1:1:1在甲苯中反应得到绿色晶体C(反应2);在氩气保护下,CrCl2和A在吡啶(简写为py)中反应,得到深绿色晶体D(反应3),D中金属离子为八面体配位,配位原子均为氮原子。在一定的条件下,B、C和D之间可以发生转化(下图b),这一过程被认为有可能用于O2的活化或消除。
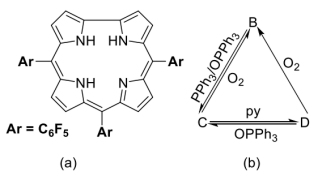
(1)A中的咔咯环是否有芳香性______ ?与之对应的π电子数是______ 。
(2)写出B、C、D的化学式(要求:配体用简写符号表示):
B______ 、C______ 、D______ 。
(3)写出B、C、D中金属离子的价电子组态(均用dn方式表示)。
B______ 、C______ 、D______ 。
(4)写出制备B、C、D的反应方程式(要求:配体用简写符号,系数为最简整数比)。
B______ 、C______ 、D______ 。
(5)利用电化学处理,B可以得电子转化为B-,也可以失去电子转化为B+。与预期的磁性相反,B+依然显示顺磁性。进一步光谱分析发现,与咔咯环配体相关的吸收峰位置发生了显著变化。推测金属离子的价电子组态______ (用dn方式表示),指出磁性与光谱变化的原因______ 。

(1)A中的咔咯环是否有芳香性
(2)写出B、C、D的化学式(要求:配体用简写符号表示):
B
(3)写出B、C、D中金属离子的价电子组态(均用dn方式表示)。
B
(4)写出制备B、C、D的反应方程式(要求:配体用简写符号,系数为最简整数比)。
B
(5)利用电化学处理,B可以得电子转化为B-,也可以失去电子转化为B+。与预期的磁性相反,B+依然显示顺磁性。进一步光谱分析发现,与咔咯环配体相关的吸收峰位置发生了显著变化。推测金属离子的价电子组态
更新时间:2021-03-24 21:31:31
|
相似题推荐
解答题-工业流程题
|
困难
(0.15)
解题方法
【推荐1】以 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:

已知:① ;
;
② ,
, 有两性,
有两性, ;
;
③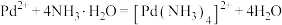 ,
,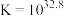 。
。
(1) 为二元强酸,写出“氧化”时发生的主要反应的离子方程式:
为二元强酸,写出“氧化”时发生的主要反应的离子方程式:___________ 。
(2)“氧化”时易产生一种有毒气体,该气体的化学式为___________ 。
(3)若“氧化”不充分,“沉钯”时所得 的产率降低,其原因是
的产率降低,其原因是___________ ;氧化液中Pd的浓度一定,为提高 的产率,“沉钯”时需控制的条件有反应的温度、
的产率,“沉钯”时需控制的条件有反应的温度、___________ 。
(4)CO可将 溶液还原得到金属Pd,写出反应的化学方程式:
溶液还原得到金属Pd,写出反应的化学方程式:___________ 。标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为 ,Pd的相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式:
,Pd的相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式:___________ 。若用 代替CO进行热还原,消耗
代替CO进行热还原,消耗 的质量比理论值略高,其原因是
的质量比理论值略高,其原因是___________ 。
 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:
已知:①
 ;
;②
 ,
, 有两性,
有两性, ;
;③
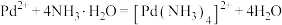 ,
,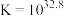 。
。(1)
 为二元强酸,写出“氧化”时发生的主要反应的离子方程式:
为二元强酸,写出“氧化”时发生的主要反应的离子方程式:(2)“氧化”时易产生一种有毒气体,该气体的化学式为
(3)若“氧化”不充分,“沉钯”时所得
 的产率降低,其原因是
的产率降低,其原因是 的产率,“沉钯”时需控制的条件有反应的温度、
的产率,“沉钯”时需控制的条件有反应的温度、(4)CO可将
 溶液还原得到金属Pd,写出反应的化学方程式:
溶液还原得到金属Pd,写出反应的化学方程式: ,Pd的相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式:
,Pd的相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式: 代替CO进行热还原,消耗
代替CO进行热还原,消耗 的质量比理论值略高,其原因是
的质量比理论值略高,其原因是
您最近一年使用:0次
解答题-无机推断题
|
困难
(0.15)
解题方法
【推荐2】已知A为一种盐,隔绝空气加热的条件下发生下述变化,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为常见的单质,I为常见的无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
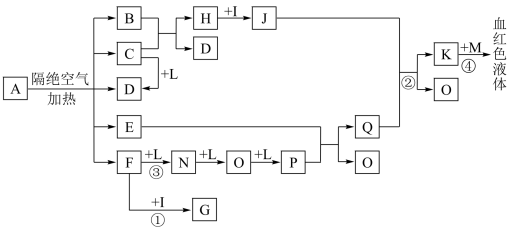
(1)写出G的电子式___________ ,M的化学式___________ 。
(2)写出反应②的离子反应方程式___________ 。
(3)写出反应③的化学反应方程式___________ ,反应①—④中属于非氧化还原反应的是___________ 。
(4)用石墨电极电解溶液K时,电解初始阶段电极反应方程式为:
阴极:___________
阳极:___________
(5)已知A在隔绝空气条件下分解产生的各产物的物质的量之比为
B:C:D:E:F=1:2:2:1:2,写出A分解的化学反应方程式___________ 。

(1)写出G的电子式
(2)写出反应②的离子反应方程式
(3)写出反应③的化学反应方程式
(4)用石墨电极电解溶液K时,电解初始阶段电极反应方程式为:
阴极:
阳极:
(5)已知A在隔绝空气条件下分解产生的各产物的物质的量之比为
B:C:D:E:F=1:2:2:1:2,写出A分解的化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
解题方法
【推荐3】工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,在空气中煅烧冰铜时,产生一种有刺激性气味的气体A,该气体排放到空气中,是导致酸雨的形成的主要原因。

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的________ (填序号)吸收。
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d.石灰乳
(2)已知铝在高温下能将某些金属从其氧化物中置换出来。将铝与泡铜发生反应从而得到粗铜。泡铜冶炼粗铜的化学方程式是___________________ 。每当有1mol铝参加反应,则转移电子个数为____________
(3)SO2气体与氢氧化钠反应时,得到的盐为Na2SO3或 NaHSO3。通过计算回答:将0.3 mol SO2通入100mL含0.4 molNaOH溶液中,充分反应后得到的盐物质的量分别是多少?(写出计算过程)___________________

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d.石灰乳
(2)已知铝在高温下能将某些金属从其氧化物中置换出来。将铝与泡铜发生反应从而得到粗铜。泡铜冶炼粗铜的化学方程式是
(3)SO2气体与氢氧化钠反应时,得到的盐为Na2SO3或 NaHSO3。通过计算回答:将0.3 mol SO2通入100mL含0.4 molNaOH溶液中,充分反应后得到的盐物质的量分别是多少?(写出计算过程)
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐1】超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。___________ ;核外未成对电子数是___________ 个。
(2)该超分子中存在的化学键类型有___________ 。
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因___________ 。
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是___________ 。
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。___________ 。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是M g·mol-1,阿伏伽德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为___________ pm。

(2)该超分子中存在的化学键类型有
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。

您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
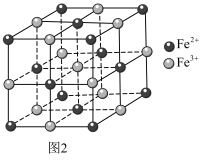
【推荐2】普鲁士蓝的化学式为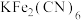 ,其结构如图1(可能位于中心的
,其结构如图1(可能位于中心的 未标出)或图2(
未标出)或图2( 、
、 未标出)所示。
未标出)所示。
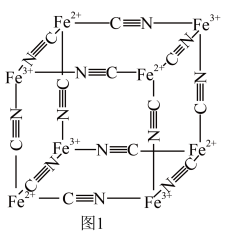
请回答:
(1)基态Fe价电子轨道表示式为_______ 。
(2)已知铁的电离能数据如下:
则,铁的第四电离能( )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:_______ 。
(3)关于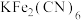 晶体下列说法不正确的是_______(填序号)。
晶体下列说法不正确的是_______(填序号)。
(4)可溶性氰化物(如KCN)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是_______ 。
(5)图2晶胞中 的个数为
的个数为_______ ,设普鲁士蓝的最简式的式量为Mr,晶体密度为 ,则相邻
,则相邻 之间的最短距离为
之间的最短距离为_______ nm。(列出计算式, 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
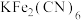 ,其结构如图1(可能位于中心的
,其结构如图1(可能位于中心的 未标出)或图2(
未标出)或图2( 、
、 未标出)所示。
未标出)所示。
请回答:
(1)基态Fe价电子轨道表示式为
(2)已知铁的电离能数据如下:
电离能/( ) ) |  |  |  |  | …… |
| Fe | 759 | 1561 | 2597 | 5290 | …… |
 )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:(3)关于
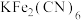 晶体下列说法不正确的是_______(填序号)。
晶体下列说法不正确的是_______(填序号)。| A.存在的化学键有σ键、π键、配位键、离子键等 |
B.Fe、N、C的电负性由大到小的顺序: |
C.晶体中 的键能>KCN中 的键能>KCN中 的键能 的键能 |
D.晶胞中 、 、 原子均参与形成配位键,其配位数之比为6:6 原子均参与形成配位键,其配位数之比为6:6 |
(5)图2晶胞中
 的个数为
的个数为 ,则相邻
,则相邻 之间的最短距离为
之间的最短距离为 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐3】1965年合成了催化剂A,实现了温和条件下的烯烃加氢。
(1)A是紫红色晶体,分子量925.23,抗磁性。它通过RhCl3·3H2O和过量三苯膦(PPh3)的乙醇溶液回流制得。画出A的立体结构_________ 。
(2)A可能的催化机理如下图所示(图中16e表示中心原子周围总共有16个电子):

画出D的结构式_______ 。
(3)确定图中所有配合物的中心原子的氧化态_________ 。
(4)确定A、C、D和E的中心离子的杂化轨道类型___________ 。
(5)用配合物的价键理论推测C和E显顺磁性还是抗磁性,说明理由__________ 。
(1)A是紫红色晶体,分子量925.23,抗磁性。它通过RhCl3·3H2O和过量三苯膦(PPh3)的乙醇溶液回流制得。画出A的立体结构
(2)A可能的催化机理如下图所示(图中16e表示中心原子周围总共有16个电子):

画出D的结构式
(3)确定图中所有配合物的中心原子的氧化态
(4)确定A、C、D和E的中心离子的杂化轨道类型
(5)用配合物的价键理论推测C和E显顺磁性还是抗磁性,说明理由
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
解题方法
【推荐1】一水硫酸四氨合铜晶体的部分性质如下:
①深蓝色,常温下在空气中易与水和 反应生成铜的碱式盐,变成绿色粉末;
反应生成铜的碱式盐,变成绿色粉末;
②受热易失氨;
③在乙醇水溶液中的溶解度随乙醇体积分数的变化如图所示:
某实验小组设计系列实验制备一水硫酸四氨合铜晶体、测定制备样品中氨的含量并探究四氨合铜离子的性质。

实验一、制备
步骤ⅰ:取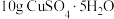 溶于
溶于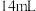 水中,加入
水中,加入 浓氨水。
浓氨水。
步骤ⅱ:沿烧杯壁慢慢加入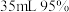 的乙醇,盖上表面皿,静置析出晶体后,过滤,洗涤,小心烘干、称重。
的乙醇,盖上表面皿,静置析出晶体后,过滤,洗涤,小心烘干、称重。
(1)制备一水硫酸四氨合铜晶体的总反应方程式为_______ 。
(2)步骤ⅱ加入乙醇后获得一水硫酸四氨合铜晶体,乙醇能降低该晶体溶解度的原因是_______ ;“过滤”应选择抽滤的操作方法,原因是_______ 。
(3)某同学认为步骤ⅱ也可以通过蒸发浓缩、冷却结晶获得所要晶体,你_______ (填“是”或“否”)同意他的观点,并说明理由:_______ 。
实验二、测定制备样品中氨的含量

步骤:按如图所示装置进行实验(药品及用量已标出;加热、夹持等装置已略去;硼酸极弱,仅作吸收剂,不影响盐酸标定氨的实验结果),维持沸腾一小时,取下锥形瓶,加入指示剂进行滴定操作,到达滴定终点时,消耗 溶液
溶液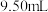 。
。
(4)装置图中仪器a的名称为_______ 。
(5)根据实验记录的结果,计算本次实验所得晶体含氨量为_______ (保留三位有效数字)。
实验三、探究四氨合铜离子的性质
步骤ⅳ:用所得晶体配成水溶液,取三份 试样,分别加入
试样,分别加入 的水、稀硫酸、氢氧化钠溶液,实验现象记录如下:
的水、稀硫酸、氢氧化钠溶液,实验现象记录如下:
(6)上述实验现象与配位离子的解离平衡有关,请用适当的化学用语表示该配位离子的解离平衡_______ ,预测加入氢氧化钠溶液后的现象:_______ 。
①深蓝色,常温下在空气中易与水和
 反应生成铜的碱式盐,变成绿色粉末;
反应生成铜的碱式盐,变成绿色粉末;②受热易失氨;
③在乙醇水溶液中的溶解度随乙醇体积分数的变化如图所示:
某实验小组设计系列实验制备一水硫酸四氨合铜晶体、测定制备样品中氨的含量并探究四氨合铜离子的性质。

实验一、制备
步骤ⅰ:取
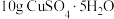 溶于
溶于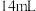 水中,加入
水中,加入 浓氨水。
浓氨水。步骤ⅱ:沿烧杯壁慢慢加入
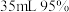 的乙醇,盖上表面皿,静置析出晶体后,过滤,洗涤,小心烘干、称重。
的乙醇,盖上表面皿,静置析出晶体后,过滤,洗涤,小心烘干、称重。(1)制备一水硫酸四氨合铜晶体的总反应方程式为
(2)步骤ⅱ加入乙醇后获得一水硫酸四氨合铜晶体,乙醇能降低该晶体溶解度的原因是
(3)某同学认为步骤ⅱ也可以通过蒸发浓缩、冷却结晶获得所要晶体,你
实验二、测定制备样品中氨的含量

步骤:按如图所示装置进行实验(药品及用量已标出;加热、夹持等装置已略去;硼酸极弱,仅作吸收剂,不影响盐酸标定氨的实验结果),维持沸腾一小时,取下锥形瓶,加入指示剂进行滴定操作,到达滴定终点时,消耗
 溶液
溶液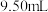 。
。(4)装置图中仪器a的名称为
(5)根据实验记录的结果,计算本次实验所得晶体含氨量为
实验三、探究四氨合铜离子的性质
步骤ⅳ:用所得晶体配成水溶液,取三份
 试样,分别加入
试样,分别加入 的水、稀硫酸、氢氧化钠溶液,实验现象记录如下:
的水、稀硫酸、氢氧化钠溶液,实验现象记录如下:| 加入试剂 | 水 | 稀硫酸 | 氢氧化钠 |
| 现象 | 几乎无变化 | 溶液颜色变成浅蓝色,与同浓度硫酸铜颜色相当 |
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
解题方法
【推荐2】某小组对Cu和 的反应进行相关实验探究。
的反应进行相关实验探究。
【实验探究】实验i:向装有0.5gCu的烧杯中加入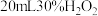 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:___________ 。
【继续探究】针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是___________ (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气先慢后快的原因是___________ 。(不考虑温度的影响)。
(3)对比实验i和iii,为探究氨水对Cu的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
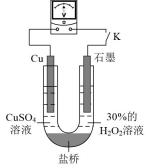
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①解释步骤c中电压增大的原因:___________ 。
②若向U型管左侧溶液中滴加硫酸后,电压不变,继续向U型管右侧溶液中滴加硫酸后,电压增大了z。则可以得出的结论是:___________ 。
(4)基于以上实验,影响Cu与 反应的因素有
反应的因素有___________ 。(任写一条)
(5)结合上述实验,下列说法正确的是___________ 。
A.电化学是研究物质氧化性、还原性的重要手段之一
B.实验ii中发生的反应中, 只体现氧化性
只体现氧化性
C.在还原反应(氧化反应)中,增大反应物浓度或降低生成物浓度,氧化剂(还原剂)的氧化性(还原性)增强
 的反应进行相关实验探究。
的反应进行相关实验探究。【实验探究】实验i:向装有0.5gCu的烧杯中加入
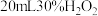 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。(1)写出该反应的化学方程式:
【继续探究】针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
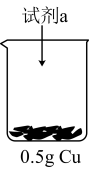 | ii | 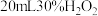 与 与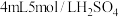 混合液 混合液 | Cu表面产生少量气泡,溶液逐渐变蓝,后产生较多气泡 |
| iii | 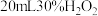 与 与 氨水混合液 氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对Cu的还原性或
 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①解释步骤c中电压增大的原因:
②若向U型管左侧溶液中滴加硫酸后,电压不变,继续向U型管右侧溶液中滴加硫酸后,电压增大了z。则可以得出的结论是:
(4)基于以上实验,影响Cu与
 反应的因素有
反应的因素有(5)结合上述实验,下列说法正确的是
A.电化学是研究物质氧化性、还原性的重要手段之一
B.实验ii中发生的反应中,
 只体现氧化性
只体现氧化性C.在还原反应(氧化反应)中,增大反应物浓度或降低生成物浓度,氧化剂(还原剂)的氧化性(还原性)增强
您最近一年使用:0次
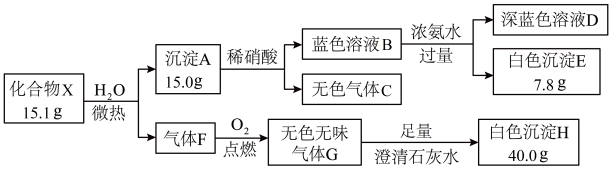
【推荐3】某化合物X由前四周期的四种元素组成,探究其组成的实验过程如图。
请回答:
(1)化合物X的化学式为______ 。气体F的电子式为______ 。
(2)深蓝色溶液D中所含的主要阳离子有(写离子符号)______ 。
(3)砖红色固体与稀硝酸反应的离子方程式为______ 。
(4)在深蓝色溶液D中滴加稀硫酸至pH为3~4,再加入过量KI固体,有白色沉淀(2种元素组成,个数比为1:1)生成,溶液由蓝色变为褐色。写出该反应过程的离子方程式:______ 。
(5)设计实验方案,鉴定蓝色溶液B中所含的阴离子成分______ 。
请回答:
(1)化合物X的化学式为
(2)深蓝色溶液D中所含的主要阳离子有(写离子符号)
(3)砖红色固体与稀硝酸反应的离子方程式为
(4)在深蓝色溶液D中滴加稀硫酸至pH为3~4,再加入过量KI固体,有白色沉淀(2种元素组成,个数比为1:1)生成,溶液由蓝色变为褐色。写出该反应过程的离子方程式:
(5)设计实验方案,鉴定蓝色溶液B中所含的阴离子成分
您最近一年使用:0次




