室温下,用 的盐酸分别滴定
的盐酸分别滴定 浓度均为
浓度均为 的
的 溶液、氨水以及醋酸铵溶液,滴定过程中溶液pH随加入盐酸体积的变化关系如图所示。下列说法正确的是( )
溶液、氨水以及醋酸铵溶液,滴定过程中溶液pH随加入盐酸体积的变化关系如图所示。下列说法正确的是( )

 的盐酸分别滴定
的盐酸分别滴定 浓度均为
浓度均为 的
的 溶液、氨水以及醋酸铵溶液,滴定过程中溶液pH随加入盐酸体积的变化关系如图所示。下列说法正确的是( )
溶液、氨水以及醋酸铵溶液,滴定过程中溶液pH随加入盐酸体积的变化关系如图所示。下列说法正确的是( )
| A.曲线X表示的是盐酸滴定氨水的曲线 |
| B.滴定三种溶液均能用酚酞作指示剂 |
C.室温下, 约为 约为 |
D.a,b两点均满足 |
更新时间:2021-04-01 16:17:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中不正确的是
A.反应 在常温下不能自发进行,则该反应的 在常温下不能自发进行,则该反应的 >0 >0 |
| B.用25mL碱式滴定管量取16.60mL碳酸钠溶液 |
| C.工业合成氨反应选择在400~500℃进行的重要原因是催化剂在该温度区间时的活性最大 |
| D.用托盘天平称量时,将NaOH固体放在左盘内的滤纸上称得质量为10.2g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列主要仪器与试剂能完成相应的实验的是
| 选项 | 主要仪器 | 试剂 | 实验目的 |
| A | 酸式滴定管、锥形瓶、铁架台(带铁夹) | 已知浓度的盐酸,待测NaOH溶液,酚酞 | 测定NaOH溶液的物质的量浓度 |
| B | 烧杯、漏斗、胶头滴管、铁架台 | 待提纯的AlCl3溶液、NaOH溶液、盐酸溶液 | 提纯混有MgCl2杂质的AlCl3溶液 |
| C | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、新制的氢氧化铜悬浊液 | 鉴别葡萄糖和蔗糖 |
| D | 烧杯、玻璃棒、胶头滴管 | FeCl3溶液、NaOH溶液 | 制Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】溶液中的离子平衡是以化学平衡理论为基础,以探讨离子反应原理的基础性理论。下列关于水溶液中的离子平衡问题叙述正确的是
A.等物质的量浓度的①NH4Cl、②CH3COONH4、③NH4Al(SO4)2三种溶液中,c( )的大小顺序为①>③>② )的大小顺序为①>③>② |
B.0.1mol·L-1NH4HCO3溶液中存在: |
C.HF溶液中滴加少量稀NaOH溶液, 的值减小 的值减小 |
| D.常温下,用0.1000mol·L-1的NaOH溶液滴定20.00mL0.1000mol·L-1的CH3COOH溶液,应该选择甲基橙作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
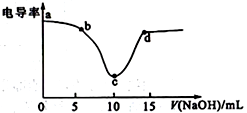
【推荐1】用0.1 mol·L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示。下列说法不正确的是

| A.b点pH值大于1 | B.盐酸浓度为 0.lmol·L-1 |
| C.c点:c(Na+)>c(A-)>c(H+)>c(OH-) | D.曲线Ⅰ为盐酸,曲线Ⅱ为醋酸溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25 ℃,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示。下列有关叙述正确的是( )

| A.pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点表示溶液中:2c(Na+)<c(CH3COO-)+c(CH3COOH) |
| C.pH=3.75溶液中:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.只根据图中数据,无法计算出25 ℃时醋酸的电离平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,将SO2通入蒸馏水中模拟酸雨形成过程,实验数据如图。下列说法不正确 的是


A.通入SO2后pH减小的原因:SO2+H2O H2SO3 H2SO3 H++HSO H++HSO |
| B.通入氧气后溶液pH下降是因为部分亚硫酸被氧化成硫酸 |
C.400s时溶液中存在:c(H+)=c(HSO )+2c(SO )+2c(SO )+c(OH-) )+c(OH-) |
| D.加入H2O2发生的反应为:H2O2+H2SO3=H2SO4+H2O;H2O2+SO2=H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温时,用 稀盐酸滴定
稀盐酸滴定 溶液,已知:
溶液,已知: 溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是
溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是

 稀盐酸滴定
稀盐酸滴定 溶液,已知:
溶液,已知: 溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是
溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是
| A.可选取酚酞作为滴定指示剂 |
| B.M点溶液的pH>7 |
| C.图中Q点水的电离程度最大 |
D.M点, |
您最近一年使用:0次

 加热到
加热到 ,不考虑水挥发,下列溶液的
,不考虑水挥发,下列溶液的 变大的是
变大的是 溶液
溶液 溶液
溶液 硫酸溶液
硫酸溶液 的
的