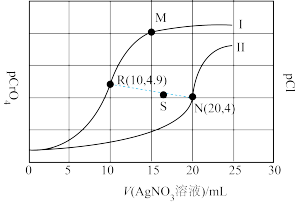
某温度下,分别向体积均为10 mL、浓度均为0.1 mol·L-1的KCl溶液和K2CrO4溶液中滴加0.1 mol·L-1的AgNO3溶液,滴加过程中pCl和pCrO4随加入AgNO3溶液的体积(V)的变化关系如图所示。已知:pCl=-lgc(Cl-),pCrO4=-lgc( )。下列说法不正确的是
)。下列说法不正确的是
 )。下列说法不正确的是
)。下列说法不正确的是
| A.曲线I表示pCl与V(AgNO3溶液)的变化关系 |
| B.若仅增大KCl的浓度,平衡点由R点沿虚线移向S点 |
C.M点溶液中:c( )>c(Ag+)>c(H+)>c(OH-) )>c(Ag+)>c(H+)>c(OH-) |
| D.该温度下,Ksp(Ag2CrO4)=4.0×10-12 |
2021·贵州黔东南·模拟预测 查看更多[6]
贵州省黔东南州2021届高三下学期3月高考模拟考试理综化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)第10练 沉淀溶解平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)安徽省舒城中学2021-2022学年高二下学期第一次月考化学试题(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
更新时间:2021-04-06 18:41:13
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】对某难溶电解质AnBm的饱和溶液中,下列说法正确的是
| A.加同温度的水,其溶度积减小、溶解度增大 |
| B.升高温度,它的溶解度和溶度积都增大 |
| C.饱和溶液中c(Am+)=c(Bn﹣) |
| D.加同温度的水,其溶度积、溶解度均不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】室温下,将 溶液与过量
溶液与过量 固体混合,溶液
固体混合,溶液 随时间变化如图所示。
随时间变化如图所示。
下列说法不正确的是
 溶液与过量
溶液与过量 固体混合,溶液
固体混合,溶液 随时间变化如图所示。
随时间变化如图所示。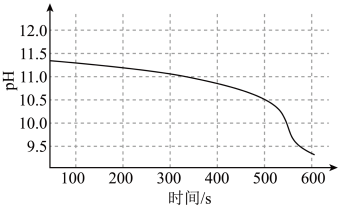
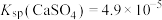
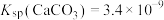
下列说法不正确的是
A.两者混合发生反应: |
B.随着反应的进行, 逆向移动,溶液 逆向移动,溶液 下降 下降 |
C.充分反应后上层清液中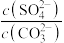 约为 约为 |
D.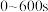 内上层清液中存在: 内上层清液中存在: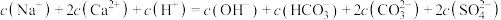 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】精炼铜工业中阳极泥的综合利用具有重要意义。从阳极泥中回收多种金属的流程如下。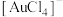 ;分金渣的主要成分为
;分金渣的主要成分为 ;
; 在反应中被氧化为
在反应中被氧化为 。
。
下列说法不正确 的是
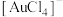 ;分金渣的主要成分为
;分金渣的主要成分为 ;
; 在反应中被氧化为
在反应中被氧化为 。
。下列说法
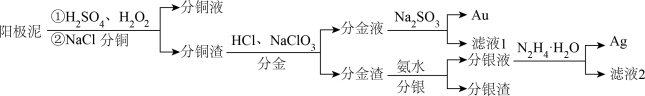
A.“分铜”时加入 的目的是降低银的浸出率 的目的是降低银的浸出率 |
B.得到分金液的反应为: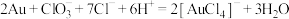 |
C.得到分银液的反应为: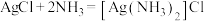 |
| D.“滤液2”中含有大量的氨,可直接循环利用 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】当氢氧化镁固体在水中达到溶解平衡 Mg(OH)2(s) Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
 Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的| A.NH3 ·H2O | B.NaOH | C.MgSO4 | D.NaHSO4 |
您最近一年使用:0次
【推荐1】根据下列实验操作和现象,所得结论或推论正确的是
| 实验操作和现象 | 实验结论或推论 | |
| A | 向FeCl3溶液中加入Cu片,振荡,溶液颜色变化 | Cu与FeCl3发生了置换反应 |
| B | 用pH试纸测得NaA、NaB溶液的pH分别为9、8 | 酸性:HB>HA |
| C | 用AgNO3标准溶液滴定待测液中c(Cl-),以K2CrO4为指示剂 | 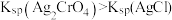 |
| D | 向Ba(NO3)2溶液中通入SO2气体,产生白色沉淀 | SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知,常温下 。向
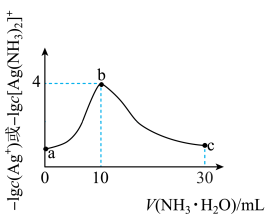
。向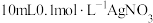 溶液中逐滴加入等浓度的氨水。反应过程中,
溶液中逐滴加入等浓度的氨水。反应过程中,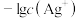 或
或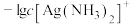 与加入氨水体积的关系如图所示。下列说法错误的是
与加入氨水体积的关系如图所示。下列说法错误的是
 。向
。向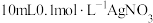 溶液中逐滴加入等浓度的氨水。反应过程中,
溶液中逐滴加入等浓度的氨水。反应过程中,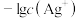 或
或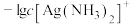 与加入氨水体积的关系如图所示。下列说法错误的是
与加入氨水体积的关系如图所示。下列说法错误的是
A.a点溶液中: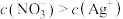 |
| B.从b到c的过程中,水的电离程度增大 |
| C.常温下,b点溶液的pH约为10 |
D.b点溶液中: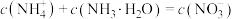 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知:25℃时,Ksp[Ni(OH)2]=2.0×10-15,Ksp[Fe(OH)3]=4.0×10-38。将含Fe2O3、Ag、Ni的某型废催化剂溶于盐酸,过滤,滤渣为Ag,所得溶液中c(Ni2+)=c(Fe3+)=0.4mol/L。向该溶液中滴加一定浓度的NaOH溶液(假设溶液体积不变)。下列说法中正确的是
| A.金属活动性:Ag>Ni |
| B.加入NaOH溶液时,先产生Ni(OH)2沉淀 |
C.当滴定到溶液pH=5时,溶液中lg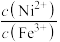 约为10 约为10 |
| D.当滴定到溶液呈中性时,Ni2+已沉淀完全 |
您最近一年使用:0次
【推荐1】秦俑彩绘中含有难溶的铅白( )和黄色的
)和黄色的 。常温下,
。常温下, 和
和 在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是
在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是

 )和黄色的
)和黄色的 。常温下,
。常温下, 和
和 在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是
在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是
A.完全沉淀废液中的 , , 的效果不如 的效果不如 |
B.z点,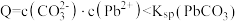 |
C.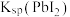 的数量级为 的数量级为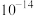 |
D. 转化为 转化为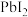 的反应趋势很大 的反应趋势很大 |
您最近一年使用:0次
【推荐2】25℃时,向2.5L蒸馏水中加入0.05molBaSO4固体粉末,再逐渐加入一定量的Na2CO3固体粉末,边加边搅拌(忽略溶液体积变化)。溶液中部分离子的浓度变化如图所示。下列说法正确的是
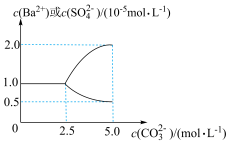

| A.25℃时,Ksp(BaCO3)<Ksp(BaSO4) |
| B.BaSO4在水中的Ksp大于其在BaCl2溶液中的Ksp |
| C.加入1.3molNa2CO3,即可使BaSO4全部转化为BaCO3 |
D.当BaSO4恰好全部转化为BaCO3时,c( )>c(Ba2+)>c( )>c(Ba2+)>c( )>c(OH-) )>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+、OH-未列出)
常温下,取一定量经Na2FeO4处理过海水为原料制备精制食盐水和MgCl2·7H2O,过程如下:
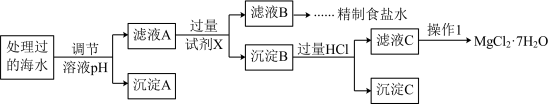
Ksp[Fe(OH)3]=1.0×10-38,Ksp[Mg(OH)2]=5.0×10-12(当溶液中某离子浓度低于1×10-5mol/L时,认为沉淀完全)。操作过程中溶液的体积变化忽略不计。下列说法正确的是
| 离子 | SO | Mg2+ | Fe3+ | Na+ | Cl- |
| 浓度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |

Ksp[Fe(OH)3]=1.0×10-38,Ksp[Mg(OH)2]=5.0×10-12(当溶液中某离子浓度低于1×10-5mol/L时,认为沉淀完全)。操作过程中溶液的体积变化忽略不计。下列说法正确的是
| A.表格中a>0.16 |
| B.沉淀A为Fe(OH)3,理论上应调节pH的范围是(5,11) |
| C.试剂X为NaOH溶液 |
| D.操作1是蒸发结晶 |
您最近一年使用:0次


 CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率

