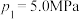在温度和容积不变的密闭容器中,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图所示,则下列叙述正确的是
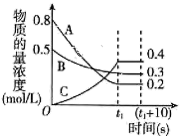

A.该反应的化学方程式为A+3B 2C 2C |
| B.在t1s时,v(A)正=0 |
| C.(t1+10)s时再充入0.4mol A和0.25mol B,反应物A的转化率增大 |
| D.若该反应在绝热容器中进行,也在t1时刻达到平衡 |
更新时间:2021-04-16 17:44:11
|
相似题推荐
【推荐1】一定温度下,在两个容积均为 的恒容密闭容器中加入一定量的反应物,发生反应
的恒容密闭容器中加入一定量的反应物,发生反应 ,相关数据见下表。
,相关数据见下表。
下列说法不正确 的是
 的恒容密闭容器中加入一定量的反应物,发生反应
的恒容密闭容器中加入一定量的反应物,发生反应 ,相关数据见下表。
,相关数据见下表。| 容器编号 | 温度/℃ | 起始物质的量/ | 平衡物质的量/ | |
 |  |  | ||
| Ⅰ |  | 0.4 | 0.4 | 0.2 |
| Ⅱ |  | 0.4 | 0.4 | 0.24 |
A. |
B.Ⅰ中反应达到平衡时, 的转化率为50% 的转化率为50% |
C.Ⅱ中反应平衡常数 |
D. 的容器中,若四种气体的物质的量均为 的容器中,若四种气体的物质的量均为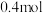 ,则 ,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】恒温下,对于可逆反应:2A(?) 2C(g)+B(s),在达到平衡状态后将容器容积缩小一半,待重新达到平衡状态后测得C的浓度与缩小容器容积前相同。则A的状态为
2C(g)+B(s),在达到平衡状态后将容器容积缩小一半,待重新达到平衡状态后测得C的浓度与缩小容器容积前相同。则A的状态为
 2C(g)+B(s),在达到平衡状态后将容器容积缩小一半,待重新达到平衡状态后测得C的浓度与缩小容器容积前相同。则A的状态为
2C(g)+B(s),在达到平衡状态后将容器容积缩小一半,待重新达到平衡状态后测得C的浓度与缩小容器容积前相同。则A的状态为| A.气态 | B.气态或液态 | C.液态或固态 | D.只能是固态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列表述与示意图不一致的是
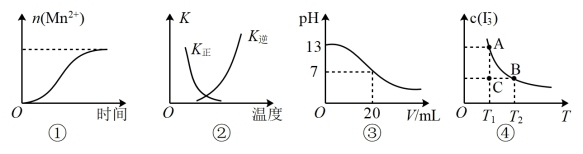
| A.图①可表示5mL 0.01mol•L﹣1KMnO4酸性溶液与过量的0.1mol•L﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 |
B.图②中曲线可表示反应2SO2(g)+O2 (g)  2SO3(g) △H<0的正、逆反应平衡常数K随温度的变化 2SO3(g) △H<0的正、逆反应平衡常数K随温度的变化 |
| C.图③可表示常温下,用0.1mol•L﹣1的NaOH溶液滴定20mL 0.1mol•L﹣1盐酸,溶液pH随加入的NaOH溶液体积的变化 |
D.I2在KI溶液中存在平衡:I2(aq)+I﹣(aq)  I I (aq),c(I (aq),c(I )与温度T的关系如图④,若反应进行到C点状态时,则一定有v(正)>v(逆) )与温度T的关系如图④,若反应进行到C点状态时,则一定有v(正)>v(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用活性炭还原氮氧化物,可防止空气污染。往一恒容密闭容器中加入一定量的活性炭和NO,某温度下发生反应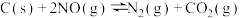 ,测得不同时间内各物质的物质的量数据如表所示:
,测得不同时间内各物质的物质的量数据如表所示:
下列说法错误的是
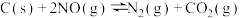 ,测得不同时间内各物质的物质的量数据如表所示:
,测得不同时间内各物质的物质的量数据如表所示:物质 物质的量/mol 时间/min | NO |  |  |
| 0 | 0.400 | 0 | 0 |
| 10 | 0.232 | 0.084 | 0.084 |
| 20 | 0.160 | 0.120 | 0.120 |
| 30 | 0.160 | 0.120 | 0.120 |
A.该反应的平衡常数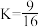 |
B.仅及时移除部分 ,可增大该反应的平衡常数 ,可增大该反应的平衡常数 |
| C.NO的转化率为60% |
| D.反应达平衡后,混合气体的平均相对分子质量为33.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定温度下,在容积恒为 的容器中通入一定量
的容器中通入一定量 ,发生反应
,发生反应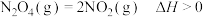 ,体系中各组分浓度随时间(t)的变化如下表。下列说法
,体系中各组分浓度随时间(t)的变化如下表。下列说法不正确 的是
 的容器中通入一定量
的容器中通入一定量 ,发生反应
,发生反应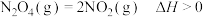 ,体系中各组分浓度随时间(t)的变化如下表。下列说法
,体系中各组分浓度随时间(t)的变化如下表。下列说法| t/s | 0 | 20 | 40 | 60 | 80 |
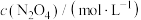 | 0.100 | 0.062 | 0.048 | 0.040 | 0.040 |
 | 0 | 0.076 | 0.104 | 0.120 | 0.120 |
A.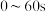 , , 的平均反应速率为 的平均反应速率为 |
B.升高温度,反应 化学平衡常数值增大 化学平衡常数值增大 |
C. 时,再充入 时,再充入 、 、 各 各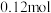 ,平衡不移动 ,平衡不移动 |
| D.若压缩容器使压强增大,达新平衡后混合气颜色比原平衡时深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】可逆反应:X+Y W+Z,反应速率(V)随时间(t)变化的情况如图所示。
W+Z,反应速率(V)随时间(t)变化的情况如图所示。 表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是

 W+Z,反应速率(V)随时间(t)变化的情况如图所示。
W+Z,反应速率(V)随时间(t)变化的情况如图所示。 表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
A. 时条件改变引起的变化是平衡向正反应方向移动 时条件改变引起的变化是平衡向正反应方向移动 |
B.若 改变的条件是压强,则W、Z均为气体,X、Y中只有一种为气体 改变的条件是压强,则W、Z均为气体,X、Y中只有一种为气体 |
C.若 改变的条件是温度,则该反应的正反应是吸热反应 改变的条件是温度,则该反应的正反应是吸热反应 |
D.若 改变的条件是浓度,改变的方法是减小X、Y的浓度 改变的条件是浓度,改变的方法是减小X、Y的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向10 L恒容密闭容器中充入1 mol S2Cl2和1 mol Cl2,发生反应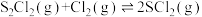 。Cl2与SCl2的消耗速率(
。Cl2与SCl2的消耗速率( )与温度(T)的关系如图所示。
)与温度(T)的关系如图所示。
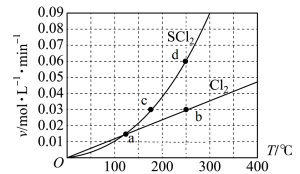
下列说法错误的是
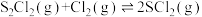 。Cl2与SCl2的消耗速率(
。Cl2与SCl2的消耗速率( )与温度(T)的关系如图所示。
)与温度(T)的关系如图所示。
下列说法错误的是
| A.正反应的活化能小于逆反应的活化能 |
B. 与 与 的转化率始终相等 的转化率始终相等 |
| C.a、b、c、d四点对应状态下,只有a达到平衡状态 |
D.一定温度下,向平衡体系中再充入一定量的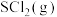 ,重新平衡后, ,重新平衡后, 的物质的量分数不变 的物质的量分数不变 |
您最近一年使用:0次

 的催化氧化:
的催化氧化: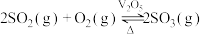
 。当
。当 和
和