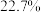用活性炭还原氮氧化物,可防止空气污染。往一恒容密闭容器中加入一定量的活性炭和NO,某温度下发生反应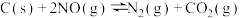 ,测得不同时间内各物质的物质的量数据如表所示:
,测得不同时间内各物质的物质的量数据如表所示:
下列说法错误的是
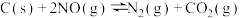 ,测得不同时间内各物质的物质的量数据如表所示:
,测得不同时间内各物质的物质的量数据如表所示:物质 物质的量/mol 时间/min | NO |  |  |
| 0 | 0.400 | 0 | 0 |
| 10 | 0.232 | 0.084 | 0.084 |
| 20 | 0.160 | 0.120 | 0.120 |
| 30 | 0.160 | 0.120 | 0.120 |
A.该反应的平衡常数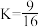 |
B.仅及时移除部分 ,可增大该反应的平衡常数 ,可增大该反应的平衡常数 |
| C.NO的转化率为60% |
| D.反应达平衡后,混合气体的平均相对分子质量为33.6 |
更新时间:2021-12-25 15:27:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g) +2H2(g)  CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是

 CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
| A.T1<T2 |
| B.T1℃时该反应的平衡常数为4.0 L2·mol-2 |
| C.同一温度下,n(H2)/n(CO)越大,平衡常数也越大 |
| D.同条件下n(H2)/n(CO)越大,CO和H2的转化率也越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实能用勒夏特列原理来解释的是
A.SO2被氧化为SO3,往往需要使用催化剂:2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
B.500℃左右的温度比室温更有利于合成氨反应:N2(g)+3H2(g) 2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
| C.实验室采用排饱和食盐水的方法收集氯 |
D.H2、I2、HI平衡混合气体加压后颜色加深:H2(g)+I2(g) 2HI(g) 2HI(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某温度时,两个恒容密闭容器中仅发生反应2NO2(g)⇌2NO(g) +O2 (g) ΔH > 0。实验测得:υ正(NO2)=k正c2(NO2),υ逆(NO)=k逆c2(NO)·c(O2),k正、k逆为化学反应速率常数,只受温度影响。
下列说法不正确 的是
| 容器 编号 | 起始浓度(mol·L−1) | 平衡浓度(mol·L−1) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.6 | 0.1 | 0 | |
| A.Ⅰ中NO2的平衡转化率约为66.7% |
| B.Ⅱ中达到平衡状态时,c(O2)<0.2mol·L−1 |
C.该反应的化学平衡常数可表示为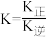 |
| D.升高温度,达到平衡状态时 Ⅰ中c(O2)<0.2mol·L−1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】丙烯腈(C3H3N)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是
 O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是| A.该反应只有在低温下才能自发进行 |
B.该反应的平衡常数K= |
| C.该反应每消耗1molC3H6,转移电子的物质的量为6mol |
| D.其他条件相同,减压和升温均有利于提高丙烯腊的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在催化剂作用下,向容积为1L 的容器中加入1molX 和3molY,发生反应 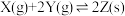 ,平衡时和反应10min 时X的转化率α (X)随温度的变化分别如曲线 I、Ⅱ所示。下列说法错误的是
,平衡时和反应10min 时X的转化率α (X)随温度的变化分别如曲线 I、Ⅱ所示。下列说法错误的是

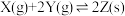 ,平衡时和反应10min 时X的转化率α (X)随温度的变化分别如曲线 I、Ⅱ所示。下列说法错误的是
,平衡时和反应10min 时X的转化率α (X)随温度的变化分别如曲线 I、Ⅱ所示。下列说法错误的是
| A.该反应ΔH 0 |
B.200℃时,前10min的平均反应速率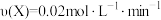 |
| C.400℃时,反应的平衡常数 K = 2 |
| D.ab 段变化可能是随温度升高反应速率加快,bc 段变化可能是催化剂在温度高于 400℃时活性降低导致 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
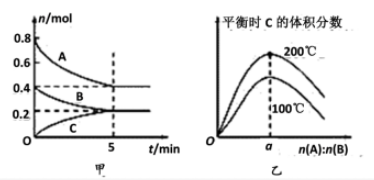
【推荐3】在容积为2 L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是 
| A.200℃时,反应从开始到平衡的平均速率v(A)=v(B) |
| B.200℃时,该反应的平衡常数为25 |
| C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大 |
D.由图乙可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2 zC(g)的ΔH<0,且a=2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应: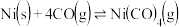 ,已知该反应的平衡常数与温度的关系如表所示:
,已知该反应的平衡常数与温度的关系如表所示:
下列说法正确的是
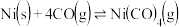 ,已知该反应的平衡常数与温度的关系如表所示:
,已知该反应的平衡常数与温度的关系如表所示:| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
| A.升高温度,CO的平衡转化率增大 |
| B.在80℃达到平衡时,充入一定量的Ni(CO)4气体再次平衡后,CO的体积分数增大 |
| C.在80℃时,测得某时刻,Ni(CO)4、CO的浓度均为0.5mol•L﹣1,则此时v(正)<v(逆) |
| D.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为0.6mol•L﹣1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定量混合气体在密闭容器中发生如下反应: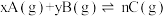 ,达到平衡后,测得A气体的浓度为0.4mol/L。保持温度不变将容器的容积压缩到原来的一半(整个过程无气体液化),再达平衡时,测得A气体的浓度为1.0mol/L,则下列叙述中不正确的是
,达到平衡后,测得A气体的浓度为0.4mol/L。保持温度不变将容器的容积压缩到原来的一半(整个过程无气体液化),再达平衡时,测得A气体的浓度为1.0mol/L,则下列叙述中不正确的是
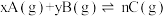 ,达到平衡后,测得A气体的浓度为0.4mol/L。保持温度不变将容器的容积压缩到原来的一半(整个过程无气体液化),再达平衡时,测得A气体的浓度为1.0mol/L,则下列叙述中不正确的是
,达到平衡后,测得A气体的浓度为0.4mol/L。保持温度不变将容器的容积压缩到原来的一半(整个过程无气体液化),再达平衡时,测得A气体的浓度为1.0mol/L,则下列叙述中不正确的是| A.x+y<n | B.压缩后,C的物质的量分数减小 |
| C.压缩后,C的浓度比压缩前更大 | D.压缩后,混合气体的平均摩尔质量减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】煤化工生产中常研究不同温度下平衡常数、投料比及产率等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
则下列说法错误的是( )
已知:CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
| A.在830℃,等物质的量的CO和H2O反应达到平衡时,CO的转化率为50% |
| B.上述正向反应是放热反应 |
| C.某温度下上述反应平衡时,恒容、升高温度,原化学平衡向逆反应方向移动 |
| D.在500℃时,反应达到平衡后,增大压强,化学平衡常数K减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Cu2+与NH3存在如下平衡:Cu2+ [Cu(NH3)]2+
[Cu(NH3)]2+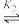 [Cu(NH3)2]2+
[Cu(NH3)2]2+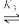 [Cu(NH3)3]2+
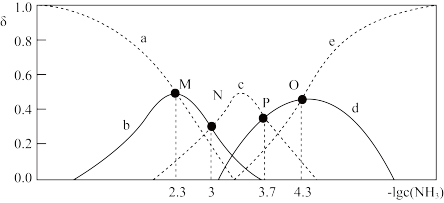
[Cu(NH3)3]2+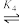 [Cu(NH3)4]2+;向某浓度的硫酸铜溶液中滴加浓氨水,实验测得Cu2+、[Cu(NH3)]2+、[Cu(NH3)2]2+、[Cu(NH3)3]2+、[Cu(NH3)4]2+的物质的量分布分数(δ)与溶液中游离氨的浓度的负对数[-lgc(NH3)]关系如图所示。下列说法正确的是
[Cu(NH3)4]2+;向某浓度的硫酸铜溶液中滴加浓氨水,实验测得Cu2+、[Cu(NH3)]2+、[Cu(NH3)2]2+、[Cu(NH3)3]2+、[Cu(NH3)4]2+的物质的量分布分数(δ)与溶液中游离氨的浓度的负对数[-lgc(NH3)]关系如图所示。下列说法正确的是
 [Cu(NH3)]2+
[Cu(NH3)]2+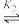 [Cu(NH3)2]2+
[Cu(NH3)2]2+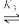 [Cu(NH3)3]2+
[Cu(NH3)3]2+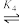 [Cu(NH3)4]2+;向某浓度的硫酸铜溶液中滴加浓氨水,实验测得Cu2+、[Cu(NH3)]2+、[Cu(NH3)2]2+、[Cu(NH3)3]2+、[Cu(NH3)4]2+的物质的量分布分数(δ)与溶液中游离氨的浓度的负对数[-lgc(NH3)]关系如图所示。下列说法正确的是
[Cu(NH3)4]2+;向某浓度的硫酸铜溶液中滴加浓氨水,实验测得Cu2+、[Cu(NH3)]2+、[Cu(NH3)2]2+、[Cu(NH3)3]2+、[Cu(NH3)4]2+的物质的量分布分数(δ)与溶液中游离氨的浓度的负对数[-lgc(NH3)]关系如图所示。下列说法正确的是
| A.曲线b表示[Cu(NH3)]2+ |
B.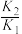 < <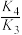 |
C.Q点,2c(Cu2+)<c(SO ) ) |
D.M点,2c(SO )+c(OH-)=2c(Cu2+)+2c{[Cu(NH3)]2+}+2c{[Cu(NH3)2]2+}+2c{[Cu(NH3)3]2+}+2c{[Cu(NH3)4]2+}+c(H+) )+c(OH-)=2c(Cu2+)+2c{[Cu(NH3)]2+}+2c{[Cu(NH3)2]2+}+2c{[Cu(NH3)3]2+}+2c{[Cu(NH3)4]2+}+c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
 PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A.体系平衡时与反应起始时的压强之比为5∶6 |
| B.反应在前50s的平均速率ν(PCl3)=0.0032mol·L-1·s-1 |
| C.相同温度下,起始时向容器中充入0.6mol PCl5、0.20mol PCl3和0.20mol Cl2,反应达到平衡前v(正)>v(逆) |
D.温度为T时,反应PCl5(g) PCl3(g)+Cl2(g)的平衡常数为0.025mol·L-1 PCl3(g)+Cl2(g)的平衡常数为0.025mol·L-1 |
您最近一年使用:0次

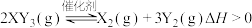 ,测得不同起始浓度和催化剂表面积下
,测得不同起始浓度和催化剂表面积下 浓度随时间的变化,如下表所示,下列说法正确的是
浓度随时间的变化,如下表所示,下列说法正确的是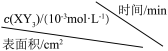

 时处于平衡状态,
时处于平衡状态,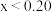
 的体积分数约为
的体积分数约为