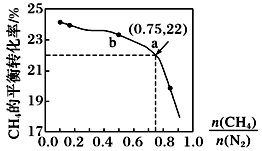
煤化工生产中常研究不同温度下平衡常数、投料比及产率等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
则下列说法错误的是( )
已知:CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
| A.在830℃,等物质的量的CO和H2O反应达到平衡时,CO的转化率为50% |
| B.上述正向反应是放热反应 |
| C.某温度下上述反应平衡时,恒容、升高温度,原化学平衡向逆反应方向移动 |
| D.在500℃时,反应达到平衡后,增大压强,化学平衡常数K减小 |
10-11高三上·辽宁丹东·阶段练习 查看更多[1]
(已下线)2010年辽宁省丹东市四校协作体高三上学期第一次联合考试(理综)化学
更新时间:2016-12-09 00:53:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】最新研究表明,在多孔炭材料上搭载活性组分催化氧化硫化氢,脱硫效果明显优于传统的吸附法。其反应机理如图所示,H2S在某温度下浓度为0.1mol•L-1。下列有关说法正确的是
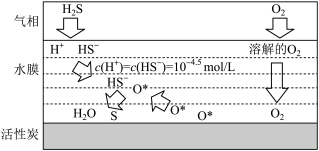

| A.该温度下,H2S一级电离常数数量级为10-8 |
| B.提高水膜的酸性,有利于增强脱硫效果 |
| C.温度越高,反应速率越快,脱硫效果越好 |
| D.多孔炭材料上搭载活性组分,主要的目的是吸附O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
A.恒温恒容下,NH2COONH4(s)  2NH3(g)+CO2(g),当气体的平均相对分子质量不变时,可以判断该反应已经达到平衡 2NH3(g)+CO2(g),当气体的平均相对分子质量不变时,可以判断该反应已经达到平衡 |
B.恒温恒容下,X(g)+Y(g)  2Z(g)+N(s),当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 2Z(g)+N(s),当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 |
C.恒温恒容下,X(g)+Y(g)  2Z(g)+N(s)达到平衡,移走部分N,平衡向正反应方向移动 2Z(g)+N(s)达到平衡,移走部分N,平衡向正反应方向移动 |
D.N2(g)+3H2(g)  2NH3(g) ΔH<0,反应达到平衡后升温,则H2反应速率和平衡转化率均增大 2NH3(g) ΔH<0,反应达到平衡后升温,则H2反应速率和平衡转化率均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】恒压条件下,密闭容器中将CO2、H2按照体积比为1:3合成CH3OH,其中涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1= -49kJ·mol-l
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2= 41kJ·mol-l
在不同催化剂作用下发生反应I和反应Ⅱ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图

已知:CH3OH的选择性=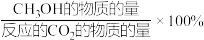
下列说法正确的是
Ⅰ.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1= -49kJ·mol-l
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2= 41kJ·mol-l
在不同催化剂作用下发生反应I和反应Ⅱ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图

已知:CH3OH的选择性=
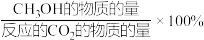
下列说法正确的是
A.反应 CO(g)+2H2(g) CH3OH(g) △H= 90kJ·mol-1 CH3OH(g) △H= 90kJ·mol-1 |
| B.合成甲醇的适宜工业条件是290℃,催化剂选择CZ(Zr-1)T |
| C.230℃以上,升高温度CO2的转化率增大,但甲醇的产率降低,原因是230℃以上,升温对反应Ⅱ的影响更大 |
| D.保持恒压恒温下充入氦气,不影响CO2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某可逆反应平衡常数表达式为  ,达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是
,达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是
 ,达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是
,达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小。下列说法正确的是| A.反应的热化学方程式为 NO2(g)+SO2(g)=NO(g) +SO3(g) △H >0 |
| B.—定条许下达到平衡时,缩小容器体积,增大体系压强,气体颜色如深 |
| C.混合气体的平均摩尔质量保持不变,说明反应已达平衡 |
| D.使用合适的催化剂可使该反应的反应速率和平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在容积固定的密闭容器中发生反应:Fe(s)+CO2(g) FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是 ( )
FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是 ( )
 FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是 ( )
FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是 ( )| A.从700 ℃到900 ℃,平衡体系中气体的密度变大 |
B.该反应的化学平衡常数表达式为K=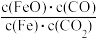 |
| C.绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 |
| D.该反应的正反应是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将一定量纯净的氨基甲酸铵固体置于恒容的密闭真空容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
下列说法正确的是
 2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:| 温度/℃ | 15 | 20 | 25 | 30 | 35 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/ 10-3mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.该反应在低温下可以自发进行 |
| B.当体系中气体的平均相对分子质量不变时,说明该反应达到了平衡状态 |
| C.恒温条件下,向容器中再充入2mol NH3和1molCO2,平衡向左移动,平衡后,NH3的浓度减小 |
| D.15℃时,该反应的平衡常数约为2.05×10-9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】德国化学家Haber因发明合成氨技术获得1918年诺贝尔化学奖,如图为恒温恒压下的密闭容器进行合成氨反应的 图象,下列说法正确的是
图象,下列说法正确的是
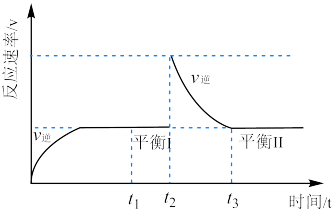
 图象,下列说法正确的是
图象,下列说法正确的是
| A.氢气的体积分数:平衡Ⅰ>平衡Ⅱ |
B. 时段, 时段, |
C. 时刻改变的条件是向密闭容器中充入 时刻改变的条件是向密闭容器中充入 |
D.平衡常数: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某密闭容器中,按物质的量之比1:1充入X、Y两种气体,发生反应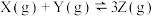
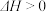 ,达到平衡后,下列有关说法正确的是
,达到平衡后,下列有关说法正确的是
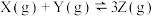
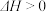 ,达到平衡后,下列有关说法正确的是
,达到平衡后,下列有关说法正确的是| A.继续通入少量物质的量之比为1:1的X、Y气体,保持容器容积不变,达到新平衡时,Z的体积分数增大 |
| B.其他条件不变,升高温度,正逆反应速率都增大,平衡时Z的体积分数比原平衡的体积分数大,平衡常数增大 |
| C.其他条件不变,将容积压缩至原来的一半,平衡逆向移动,平衡时X的体积分数比原平衡的体积分数大,平衡常数减小 |
| D.保持容器容积不变,增加Z的量,平衡逆向移动,平衡时Z的浓度比原平衡的小,体积分数比原平衡的体积分数小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中发生如下反应:mA(g)+nB(g)⇌pC(g),达到平衡后,保持温度不变,将容器的体积缩小到原来的一半,达到新平衡时,C的浓度变为原来的1.9倍。下列说法中错误的是( )
| A.m+m<p | B.平衡向逆反应方向移动 |
| C.A的转化率降低 | D.A的体积分数减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应A(g)+B(g) 3X,在其他条件不变时,通过调节容器体积改变压强,达平衡时c(A)如下表:
3X,在其他条件不变时,通过调节容器体积改变压强,达平衡时c(A)如下表:
下列分析不正确的是
 3X,在其他条件不变时,通过调节容器体积改变压强,达平衡时c(A)如下表:
3X,在其他条件不变时,通过调节容器体积改变压强,达平衡时c(A)如下表:| 平衡状态 | ① | ② | ③ |
| 容器体积/L | 40 | 20 | 1 |
| c(A)( mol·L-1) | 0.022a | 0.05a | 0.75a |
| A.①→②的过程中平衡发生了逆向移动 |
| B.①→③的过程中X的状态发生了变化 |
| C.①→③的过程中A的转化率不断减小 |
| D.与①②相比,③中X的物质的量最大 |
您最近一年使用:0次

 CH3CH2OH(g)+3H2O(g)
CH3CH2OH(g)+3H2O(g) 
 )时,CH4的平衡转化率如图。下列说法正确的是
)时,CH4的平衡转化率如图。下列说法正确的是