已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如表:下列说法正确的是
| H2CO3 | H2SO3 | HClO |
| K1=4.30×10-7 K2=5.61×10-11 | K1=1.54×10-2 K2=1.02×10-7 | K=2.95×10-8 |
A.Na2CO3溶液中通入少量SO2:2CO +SO2+H2O=2HCO +SO2+H2O=2HCO +SO +SO |
| B.相同条件下,同浓度的H2SO3溶液和H2CO3溶液的酸性,后者更强 |
C.NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO |
| D.向氯水中分别加入等浓度的NaHCO3和NaHSO3溶液,均可提高氯水中HClO的浓度 |
20-21高二下·江西景德镇·阶段练习 查看更多[3]
江西省兴国县将军中学2021-2022学年高二上学期10月月考化学试题(已下线)3.1.2 电离平衡常数-2021-2022学年高二化学课后培优练(人教版选修4)江西省景德镇市浮梁一中2020-2021学年高二下学期4月月考化学试题
更新时间:2021-04-20 17:24:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于N的氢化物说法正确的是
| A.氨水溶液显弱碱性,所以氨气是弱电解质 |
| B.肼(N2H4)常用作火箭燃料,在燃料中作氧化剂 |
| C.NH5 是熔融状态下可电离的化合物,其中只存在N-H极性共价键 |
| D.二亚氨(N2H2)不稳定,其分子结构中存在N=N键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列转化中,需要加入氧化剂才能实现的是
| A.Na2SO3→SO2 | B.Fe2+→Fe3+ |
C.MnO →Mn2+ →Mn2+ | D.Cu2+→Cu |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知25℃时,部分弱电解质的电离平衡常数如表:
下列离子方程式或守恒关系正确的是
| 弱电解质 | HClO | H2CO3 | H2SO3 | NH3·H2O |
| 电离平衡常数 | Ka=4.0×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.5×10-2 Ka2=6.0×10-8 | Kb=1.75×10-5 |
A.将Cl2通入到过量Na2CO3溶液中:Cl2+H2O+CO =HCO =HCO +HClO+Cl- +HClO+Cl- |
B.将SO2通入到NaClO溶液中:ClO-+H2O+SO2=HClO+HSO |
C.向亚硫酸溶液中加入氨水至中性:c(NH )=c(SO )=c(SO )+c(H2SO3)+c(HSO )+c(H2SO3)+c(HSO ) ) |
D.向过量Na2CO3溶液中通入少量SO2:SO2+H2O+2CO =2HCO =2HCO +SO +SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,向20mL NaB溶液中滴加等浓度的弱酸HA溶液,所得混合溶液中
NaB溶液中滴加等浓度的弱酸HA溶液,所得混合溶液中 与
与 的关系如图所示。已知
的关系如图所示。已知 。下列说法正确的是
。下列说法正确的是

 NaB溶液中滴加等浓度的弱酸HA溶液,所得混合溶液中
NaB溶液中滴加等浓度的弱酸HA溶液,所得混合溶液中 与
与 的关系如图所示。已知
的关系如图所示。已知 。下列说法正确的是
。下列说法正确的是
A. |
B.恰好完全反应时,溶液中 |
C.当溶液呈中性时,一定存在 |
D.pH=2时 的值比pH=1的大 的值比pH=1的大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】部分弱酸的电离平衡常数如下表:
下列选项错误的是
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka1=1.77×10-4 | Ka1=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
A.CN-+H2O+CO2=HCN+HCO |
| B.相同浓度的HCN和NaHCO3的导电能力:HCN>NaHCO3 |
| C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量,前者小于后者 |
| D.等pH的HCOOH和HCN稀释相同的倍数后,pH前者大于后者 |
您最近一年使用:0次

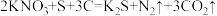 ,该反应中氧化剂为S和KNO3
,该反应中氧化剂为S和KNO3


