Ⅰ.下列各项分别与哪个影响化学反应速率的因素关系最为密切?
(1)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气泡有快有慢:_______ 。
(2)MnO2加入双氧水中放出气泡更快:_______ 。
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
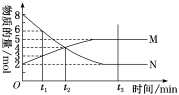
(1)比较t2时刻,正逆反应速率大小v正_______ v逆。(填“>”“=”或“<”)
(2)若t2=2 min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为_______ 。
(3)t3时刻化学反应达到平衡,反应物的转化率为_______ 。
(4)如果升高温度,则v逆_______ (填“增大”“减小”或“不变”)。
(1)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气泡有快有慢:
(2)MnO2加入双氧水中放出气泡更快:
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:

(1)比较t2时刻,正逆反应速率大小v正
(2)若t2=2 min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为
(3)t3时刻化学反应达到平衡,反应物的转化率为
(4)如果升高温度,则v逆
20-21高二上·江苏南通·期中 查看更多[3]
江苏省南通市海门实验学校2020-2021学年高二上学期期中考试化学试题(已下线)第18讲 化学反应速率(练) — 2022年高考化学一轮复习讲练测(新教材新高考)重庆市二0三中学2022-2023学年高二上学期第一次月考化学试题
更新时间:2021-04-21 17:14:43
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】影响化学反应速率的因素内因:____ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】一定温度下,反应H2+Cl2═2HCl中的某一基元反应H2+Cl·→HCl+H·,其能量变化如图所示。 表示反应物分子中旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
表示反应物分子中旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
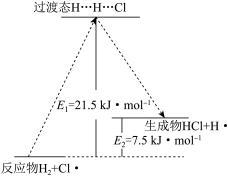
该基元反应的活化能为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)  2HI(g)
2HI(g)
(1)保持容器容积不变,向其中充入1 mol H2,反应速率_____ (填“增大”、“减小”或“不变”,下同)。
(2)升高温度,反应速率_____ 。
(3)扩大容器体积,反应速率_____ 。
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率_____ 。
 2HI(g)
2HI(g)(1)保持容器容积不变,向其中充入1 mol H2,反应速率
(2)升高温度,反应速率
(3)扩大容器体积,反应速率
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】下图为汽车尾气处理系统中“三元催化”的工作原理, 和
和 在催化剂作用下生成无污染性物质的方程式:
在催化剂作用下生成无污染性物质的方程式: 。
。
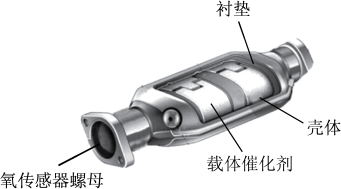
某课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
(1)实验编号②的实验目的为_______ 。
(2)课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是_______ 。
 和
和 在催化剂作用下生成无污染性物质的方程式:
在催化剂作用下生成无污染性物质的方程式: 。
。
某课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
| 实验编号 | 实验目的 | T/℃ |  初始浓度/ 初始浓度/ |  初始浓度/ 初始浓度/ | 同种催化剂的比表面积/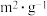 | 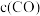 不变时所用的时间/ 不变时所用的时间/ |
| ① | 参照 | 280 | 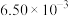 | 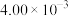 | 80 |  |
| ② | 280 | 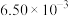 | 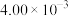 | 120 | 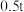 | |
| ③ | 360 | 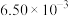 | 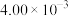 | 80 |  |
(2)课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】甲醇是重要的化工原料,又可作燃料。利用CO生产甲醇的反应为2H2(g)+CO(g) CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
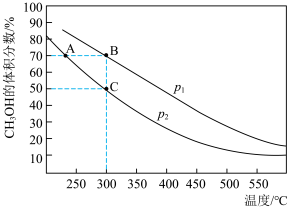
(1)该反应的ΔH______ 0(填“>”或“<”);B点与C点的平衡常数关系为KB______ KC(填“>”“<”或“=”)。向平衡体系中加入高效催化剂, 将
将______ (填“增大”“减小”或“不变”);再次增大体系压强,k正-k逆的值将______ (填“增大”“减小”或“不变”)。
(2)C点对应的平衡常数Kp=______ (Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
(3)一定温度下,将H2和CO按物质的量之比为1∶1、1∶2和2∶1进行初始投料。则达到平衡后,初始投料比为______ 时,H2转化率最大。
 CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
(1)该反应的ΔH
 将
将(2)C点对应的平衡常数Kp=
(3)一定温度下,将H2和CO按物质的量之比为1∶1、1∶2和2∶1进行初始投料。则达到平衡后,初始投料比为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】 甲烷化反应可将
甲烷化反应可将 直接转化为能源气体,具有较高的学术研究价值和工业化前景。反应原理:
直接转化为能源气体,具有较高的学术研究价值和工业化前景。反应原理: (正反应为放热反应)。
(正反应为放热反应)。 时在容积为
时在容积为 的密闭容器中,加入
的密闭容器中,加入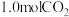 与
与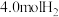 发生上述反应,记录数据如下表:
发生上述反应,记录数据如下表:
1.上述反应中,反应物总能量_______ 生成物总能量。
A.大于 B.小于 C.等于
2.能说明上述反应达到化学平衡状态的标志是_______ 。
A.
B.容器中气体总质量不再变化
C.容器中 与
与 的物质的量之和不再变化
的物质的量之和不再变化
3.上表中
_______ 。
4.分析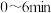 正反应速率的变化趋势并说明理由
正反应速率的变化趋势并说明理由_______ 。
 甲烷化反应可将
甲烷化反应可将 直接转化为能源气体,具有较高的学术研究价值和工业化前景。反应原理:
直接转化为能源气体,具有较高的学术研究价值和工业化前景。反应原理: (正反应为放热反应)。
(正反应为放热反应)。 时在容积为
时在容积为 的密闭容器中,加入
的密闭容器中,加入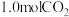 与
与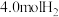 发生上述反应,记录数据如下表:
发生上述反应,记录数据如下表: 物质的量 时间  |
|
|
|
|
0 | 1.0 | 4.0 | 0 | 0 |
2 | 0.35 | 1.4 | 0.65 | 1.3 |
4 | 0.05 | x | 0.95 | 1.9 |
6 | 0.05 | x | 0.95 | 1.9 |
A.大于 B.小于 C.等于
2.能说明上述反应达到化学平衡状态的标志是
A.

B.容器中气体总质量不再变化
C.容器中
 与
与 的物质的量之和不再变化
的物质的量之和不再变化3.上表中

4.分析
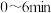 正反应速率的变化趋势并说明理由
正反应速率的变化趋势并说明理由
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】化学平衡状态的建立
(1)如图1所示,N2与H2随着反应的进行,其浓度逐渐___________ ,v正逐渐___________ ,而c(NH3)逐渐___________ ,v逆逐渐___________ ,t1时刻,它们的浓度不再改变,v正=v逆,反应达到平衡。

(2)如图2所示,随着NH3的分解,其浓度逐渐___________ ,v逆逐渐___________ ,而c(N2)、c(H2)逐渐___________ ,v正逐渐___________ ,t2时刻起,它们的浓度不再改变___________ ,反应达到平衡。
(1)如图1所示,N2与H2随着反应的进行,其浓度逐渐

(2)如图2所示,随着NH3的分解,其浓度逐渐
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】在200℃时,将amol H2(g)和bmol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g) 2HI(g)。
2HI(g)。
(1)反应刚开始时,由于c(H2)=______ ,c(I2)= ______ ,而c(HI)=______ ,所以化学反应速率V正最大,而V逆最小(为零)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)______ ,c(I2)______ ,而c(HI)______ ,从而化学反应速率v(正)______ ,而v(逆)______ 。
(3)当反应进行到v(正)与v(逆)相等时,此可逆反应就达到了平衡。
 2HI(g)。
2HI(g)。(1)反应刚开始时,由于c(H2)=
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)
(3)当反应进行到v(正)与v(逆)相等时,此可逆反应就达到了平衡。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】回答下列问题
(1)在恒温条件下将一定量 和
和 的混合气体通入容积为
的混合气体通入容积为 的密闭容器中,
的密闭容器中, 和
和 两物质的浓度随时间的变化情况如下图所示。
两物质的浓度随时间的变化情况如下图所示。 、
、 表示):
表示):_______ 。
② 、
、 、
、 、
、 四个点中,表示化学反应处于平衡状态的点是
四个点中,表示化学反应处于平衡状态的点是_______ 。
(2)如下图所示是可逆反应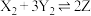 的反应速率
的反应速率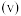 与时间
与时间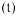 的关系曲线,下列叙述正确的是_______。
的关系曲线,下列叙述正确的是_______。
(3)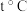 时,将
时,将 和
和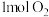 通入体积为
通入体积为 的恒温恒容密闭容器中,发生如下反应:
的恒温恒容密闭容器中,发生如下反应: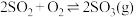 ,
, 时反应达到平衡,此时测得反应物
时反应达到平衡,此时测得反应物 还剩余
还剩余 。从反应开始到化学平衡,平衡时
。从反应开始到化学平衡,平衡时 的转化率为
的转化率为_______ 。
(1)在恒温条件下将一定量
 和
和 的混合气体通入容积为
的混合气体通入容积为 的密闭容器中,
的密闭容器中, 和
和 两物质的浓度随时间的变化情况如下图所示。
两物质的浓度随时间的变化情况如下图所示。
 、
、 表示):
表示):②
 、
、 、
、 、
、 四个点中,表示化学反应处于平衡状态的点是
四个点中,表示化学反应处于平衡状态的点是(2)如下图所示是可逆反应
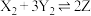 的反应速率
的反应速率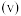 与时间
与时间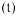 的关系曲线,下列叙述正确的是_______。
的关系曲线,下列叙述正确的是_______。
A. 时,只有正方向反应在进行 时,只有正方向反应在进行 |
B. 时,反应达到最大限度 时,反应达到最大限度 |
C. ,反应不再进行 ,反应不再进行 |
D. ,各物质的浓度不再发生变化 ,各物质的浓度不再发生变化 |
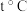 时,将
时,将 和
和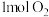 通入体积为
通入体积为 的恒温恒容密闭容器中,发生如下反应:
的恒温恒容密闭容器中,发生如下反应: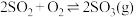 ,
, 时反应达到平衡,此时测得反应物
时反应达到平衡,此时测得反应物 还剩余
还剩余 。从反应开始到化学平衡,平衡时
。从反应开始到化学平衡,平衡时 的转化率为
的转化率为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A(g)+2B(g)=3C(g)。反应2 min后,A的浓度从开始时的1.0 mol·L-1降到0.8 mol·L-1。已知反应开始时B的浓度是1.6 mol·L-1。求:
(1)2 min末B的浓度_______ mol/L。
(2)2 min内A的平均反应速率_______ mol/(L·min)。
(3)2 min末时物质B的转化率为_______ 。
(1)2 min末B的浓度
(2)2 min内A的平均反应速率
(3)2 min末时物质B的转化率为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐3】恒温恒容下,将2mol气体A和2mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g) xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为____________ 。
(2)x=_______ 。
(3)A的转化率与B的转化率之比为_______________ 。
(4)下列各项可作为该反应达到平衡状态的标志是________ (填字母)。
 xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)A的转化率与B的转化率之比为
(4)下列各项可作为该反应达到平衡状态的标志是
| A.压强不再变化 |
| B.气体密度不再变化 |
| C.气体平均相对分子质量不再变化 |
| D.A的消耗速率与B的消耗速率之比为2:1 |
您最近一年使用:0次

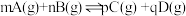 过程中的能量变化如图,回答下列问题。
过程中的能量变化如图,回答下列问题。






