SO2具有抗氧化、保鲜、防腐、脱色等功用,合理利用二氧化硫可服务于人们更好的生活。但空气中过量的二氧化硫会形成酸雨、易引起呼吸道疾病等问题,因此,二氧化硫的污染治理是化学研究的重要课题。
(1)硝化法既能生产硫酸,也能处理二氧化硫,主要反应为:NO2(g)+SO2(g) SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。
SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。
①t℃时,该反应的化学平衡常数为___ 。
②t℃时,向某容器中同时充入NO2、SO2、SO3、NO各1mol,v正___ v逆(填“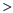 ”、“
”、“ ”或“
”或“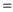 ”)
”)
(2)某实验室尝试变废为宝,模仿工业制硫酸工艺利用SO2,方程式为2SO2(g)+O2(g) 2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:
2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:
①通过分析第1组和第2组实验数据,比较两组实验中SO2的化学反应速率,可得到影响该反应速率因素的相关结论为___ 。
②在第3组的实验中一开始加入了0.5mol的SO3,反应达平衡时c仍为0.4mol,则a=___ ,b=__ 。
(1)硝化法既能生产硫酸,也能处理二氧化硫,主要反应为:NO2(g)+SO2(g)
 SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。
SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。①t℃时,该反应的化学平衡常数为
②t℃时,向某容器中同时充入NO2、SO2、SO3、NO各1mol,v正
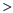 ”、“
”、“ ”或“
”或“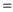 ”)
”)(2)某实验室尝试变废为宝,模仿工业制硫酸工艺利用SO2,方程式为2SO2(g)+O2(g)
 2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:
2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:| 实验组 | 温度(℃) | 起始量/mol | 平衡量/mol | 达到平衡所需时间/h | |
| SO2 | O2 | SO2 | |||
| 1 | 250 | 4 | 2 | 0.4 | 48 |
| 2 | 260 | 2 | 1 | 0.4 | 16 |
| 3 | 260 | a | b | c | t |
①通过分析第1组和第2组实验数据,比较两组实验中SO2的化学反应速率,可得到影响该反应速率因素的相关结论为
②在第3组的实验中一开始加入了0.5mol的SO3,反应达平衡时c仍为0.4mol,则a=
2021高三·山东·专题练习 查看更多[2]
更新时间:2021-05-01 09:06:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某温度下,在 密闭容器中
密闭容器中 三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
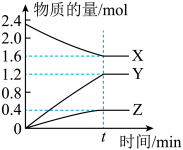
(1)该反应的化学方程式可表示为___________ .
(2)反应起始至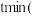 设
设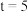 ),
), 的平均反应速率是
的平均反应速率是___________ , 的转化率为
的转化率为___________ (用百分数表示);在此温度下,该反应的平衡常数是___________ .
(3)下列可判断反应已达到平衡状态的是___________ .
A.X、Y、Z的反应速率相等
B.体系的压强保持不变
C.混合气体的密度不变
D.生成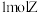 的同时生成
的同时生成
E.混合气体的平均分子质量不变
(4)一定能使该反应的反应速率增大的措施有___________ .
A.其他条件不变,及时分离出产物
B.适当降低温度
C.其他条件不变,增大 的浓度
的浓度
D.保持温度不变,将容器体积压缩为
E.恒容条件下冲入氦气,使压强增大
F.加入合适的催化剂
 密闭容器中
密闭容器中 三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
(1)该反应的化学方程式可表示为
(2)反应起始至
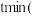 设
设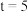 ),
), 的平均反应速率是
的平均反应速率是 的转化率为
的转化率为(3)下列可判断反应已达到平衡状态的是
A.X、Y、Z的反应速率相等
B.体系的压强保持不变
C.混合气体的密度不变
D.生成
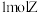 的同时生成
的同时生成
E.混合气体的平均分子质量不变
(4)一定能使该反应的反应速率增大的措施有
A.其他条件不变,及时分离出产物
B.适当降低温度
C.其他条件不变,增大
 的浓度
的浓度D.保持温度不变,将容器体积压缩为

E.恒容条件下冲入氦气,使压强增大
F.加入合适的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.在一定条件下xA+yB  zC的可逆反应达到平衡,
zC的可逆反应达到平衡,
(1)已知A、B、C均为气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是___________ 。
(2)已知C是气体且x+y=z,在加压时如果平衡发生移动,则平衡必向___________ 方向移动。(填“正反应”或“逆反应”)
(3)已知B、C是气体,现增加A的物质的量(其他条件不变),平衡不移动,则A是___________ 态。
II.(4)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 △H1
NaNO3(s)+ClNO(g) K1 △H1
2NO(g)+Cl2(g) 2ClNO(g) K2 △H2
2ClNO(g) K2 △H2
则4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=_______ (用含有K1 、 K2的式子表示);
(5)在 时,2L的密闭容器中A、B、C三种气体的初始浓度和2min末的浓度如下表(该反应为可逆反应):
时,2L的密闭容器中A、B、C三种气体的初始浓度和2min末的浓度如下表(该反应为可逆反应):
请填写下列空白:
该反应方程式可表示为_____ ;从反应开始到2min末,A的平均反应速率为_____ 。
 zC的可逆反应达到平衡,
zC的可逆反应达到平衡,(1)已知A、B、C均为气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是
(2)已知C是气体且x+y=z,在加压时如果平衡发生移动,则平衡必向
(3)已知B、C是气体,现增加A的物质的量(其他条件不变),平衡不移动,则A是
II.(4)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) K1 △H1
NaNO3(s)+ClNO(g) K1 △H12NO(g)+Cl2(g)
 2ClNO(g) K2 △H2
2ClNO(g) K2 △H2则4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(5)在
 时,2L的密闭容器中A、B、C三种气体的初始浓度和2min末的浓度如下表(该反应为可逆反应):
时,2L的密闭容器中A、B、C三种气体的初始浓度和2min末的浓度如下表(该反应为可逆反应): | 物质 | A | B | C |
初始浓度/( ) ) | 1.0 | 2.0 | 0 |
2min末的浓度/( ) ) | 0.4 | 0.2 | 1.2 |
该反应方程式可表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】合成氨对化学工业和国防工业具有重要意义。
(1)已知海水电解制得的氢气用于合成氨,某合成氨厂生产流程如下图:在第(3)个设备中用冷却的方法分离出液氨,其目的是:____________________________________________________________________ 。

(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g)⇌CO(g)+3H2(g)(该反应为吸热反应),一定温度下,在体积为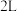 的恒容容器中发生上述反应,各物质的物质的量变化如表:
的恒容容器中发生上述反应,各物质的物质的量变化如表:
①分析表中数据,判断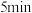 时反应是否处于平衡状态?
时反应是否处于平衡状态?_______ (填“是”或“否”,1分),前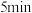 反应的平均反应速率
反应的平均反应速率
_______ 。
②在相同实验条件下,若改为加入 ,若要求平衡后
,若要求平衡后 在反应混合气中质量分数不变,则还需加入CO、H2、H2O这三种物质对应的物质的量分别为
在反应混合气中质量分数不变,则还需加入CO、H2、H2O这三种物质对应的物质的量分别为__________________________
③反应在 内,
内, 的物质的量减少的原因可能是
的物质的量减少的原因可能是_______ (填字母)。
 .减少
.减少 的物质的量
的物质的量  .降低温度
.降低温度  .升高温度
.升高温度  .充入
.充入
(1)已知海水电解制得的氢气用于合成氨,某合成氨厂生产流程如下图:在第(3)个设备中用冷却的方法分离出液氨,其目的是:

(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g)⇌CO(g)+3H2(g)(该反应为吸热反应),一定温度下,在体积为
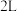 的恒容容器中发生上述反应,各物质的物质的量变化如表:
的恒容容器中发生上述反应,各物质的物质的量变化如表:时间 |  | 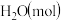 |  |  |
 |  |  |  |  |
 | 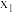 | 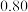 | 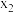 | 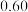 |
 |  | 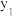 |  |  |
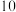 | 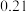 | 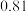 | 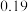 | 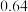 |
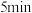 时反应是否处于平衡状态?
时反应是否处于平衡状态?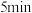 反应的平均反应速率
反应的平均反应速率
②在相同实验条件下,若改为加入
 ,若要求平衡后
,若要求平衡后 在反应混合气中质量分数不变,则还需加入CO、H2、H2O这三种物质对应的物质的量分别为
在反应混合气中质量分数不变,则还需加入CO、H2、H2O这三种物质对应的物质的量分别为③反应在
 内,
内, 的物质的量减少的原因可能是
的物质的量减少的原因可能是 .减少
.减少 的物质的量
的物质的量  .降低温度
.降低温度  .升高温度
.升高温度  .充入
.充入
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】恒温、恒压下,在一个容积可变的容器中发生如下反应:A(g)+B(g) C(g)。
C(g)。
(1)若开始时放入1 mol A和1 mol B,达到平衡后,生成amol C。这时A的物质的量为________ mol。
(2)若开始时放入3 mol A和3 mol B,达到平衡后,生成C的物质的量为________ mol。
 C(g)。
C(g)。(1)若开始时放入1 mol A和1 mol B,达到平衡后,生成amol C。这时A的物质的量为
(2)若开始时放入3 mol A和3 mol B,达到平衡后,生成C的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合成氨是人类科学技术上的一项重大突破,反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:

(1)①步骤Ⅱ中制氢气的原理如下:
a.CH4(g)+H2O(g) CO(g)+3H2(g);K1
CO(g)+3H2(g);K1
b.CO(g)+H2O(g) CO2(g)+H2(g);K2
CO2(g)+H2(g);K2
则反应CH4(g)+2H2O(g) CO2(g)+4H2(g);K=
CO2(g)+4H2(g);K=_______________ (用含K1、K2的代数式表示)。
②T1温度时,对于反应:CO(g)+ H2O(g) CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是
CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是_____________ 。
A.CO的转化率将增大 B.达到新平衡时的反应热ΔH > —Q
C.气体的密度将不变 D.H2O的体积分数增大
(2)将3 molH2和2 molN2充入某恒温恒压容器中,发生合成氨的反应:3H2(g) +N2(g) 2NH3(g)
2NH3(g)
①达平衡时NH3的浓度为c mol·L-1。保持温度不变,按下列配比分别充入该容器,平衡后NH3的浓度不为c mol·L-1的是_________ 。
A.6mol H2 + 4mol N2
B.0.75mol H2 + 0.75mol N2 + 0.5mol NH3
C.3mol H2+ 1mol N2 + 2mol NH3
② 若是在恒温恒容的容器中反应,达到平衡时NH3的浓度为c1 mol·L-1,则c________ c1(填“<”“>”或“=”),原因是________________________________________ 。
 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
(1)①步骤Ⅱ中制氢气的原理如下:
a.CH4(g)+H2O(g)
 CO(g)+3H2(g);K1
CO(g)+3H2(g);K1b.CO(g)+H2O(g)
 CO2(g)+H2(g);K2
CO2(g)+H2(g);K2则反应CH4(g)+2H2O(g)
 CO2(g)+4H2(g);K=
CO2(g)+4H2(g);K=②T1温度时,对于反应:CO(g)+ H2O(g)
 CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是
CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是A.CO的转化率将增大 B.达到新平衡时的反应热ΔH > —Q
C.气体的密度将不变 D.H2O的体积分数增大
(2)将3 molH2和2 molN2充入某恒温恒压容器中,发生合成氨的反应:3H2(g) +N2(g)
 2NH3(g)
2NH3(g)①达平衡时NH3的浓度为c mol·L-1。保持温度不变,按下列配比分别充入该容器,平衡后NH3的浓度不为c mol·L-1的是
A.6mol H2 + 4mol N2
B.0.75mol H2 + 0.75mol N2 + 0.5mol NH3
C.3mol H2+ 1mol N2 + 2mol NH3
② 若是在恒温恒容的容器中反应,达到平衡时NH3的浓度为c1 mol·L-1,则c
您最近一年使用:0次
【推荐3】一定条件下,CO2和CO可以互相转化
(1)某温度下,在容积为2L的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g) CO(g)+H2O(g)。
CO(g)+H2O(g)。
甲容器15min后达到平衡,此时CO2的转化率为75%,则0-15min内平均反应速率 (H2)=
(H2)=______ ,此条件下该反应的平衡常数K=______ 。欲使平衡后乙与甲中相同组分气体的体积分数相等,则w、x、y、z需满足的关系是________________ ,且________________ (用含y的等式表示)。
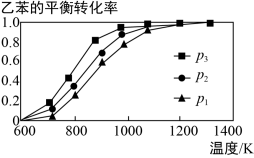
(2)研究表明,温度、压强对反应C6H5CH2CH3(g)+CO2(g) C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH
C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH ______ 0(填“>”“< ” 或“=”),压强p1、p2、p3从大到小的顺序是________________ 。
(3)CO可被NO2氧化CO+NO2 CO2+NO。当温度高于225℃时,反应速率
CO2+NO。当温度高于225℃时,反应速率 正=k正·c(CO) ·c(NO2)、
正=k正·c(CO) ·c(NO2)、 逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为
逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为______ 。
(1)某温度下,在容积为2L的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g)
 CO(g)+H2O(g)。
CO(g)+H2O(g)。| 容器 | 反应物 |
| 甲 | 8molCO2(g)、16molH2(g) |
| 乙 | wmolCO2(g)、xmolH2(g)、ymolCO(g)、zmolH2O(g) |
甲容器15min后达到平衡,此时CO2的转化率为75%,则0-15min内平均反应速率
 (H2)=
(H2)=
(2)研究表明,温度、压强对反应C6H5CH2CH3(g)+CO2(g)
 C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH
C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH (3)CO可被NO2氧化CO+NO2
 CO2+NO。当温度高于225℃时,反应速率
CO2+NO。当温度高于225℃时,反应速率 正=k正·c(CO) ·c(NO2)、
正=k正·c(CO) ·c(NO2)、 逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为
逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
①试比较K1、K2的大小,K1___ K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是___ (填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,2NH3(g) N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=___ (填数值)。
④400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正___ v(N2)逆(填“>”、“<”“=”或“不能确定”)。
⑤若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡___ (填“向左”、“向右”或“不”)移动;使用催化剂__ (填“增大”、“减小”或“不改变”)反应的ΔH。
在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)
 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②下列各项能作为判断该反应达到化学平衡状态的依据是
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,2NH3(g)
 N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=④400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正
⑤若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)⇌N2(g)+2CO2(g),一定温度下,向容积为1L的密闭容器中充入一定量的NO和CO。在t1时刻达到平衡状态,此时n(CO)=0.1mol,n(NO)=0.2mol,n(N2)=amol,且平衡时混合气体压强为初始气体压强的0.8。
①则该反应的平衡常数K=____________ 。若保持温度及容器容积不变,平衡后在此基础上再向容器中充入2amol的N2、0.2mol的NO,平衡将____________ (填“向左”、“向右”或“不”)移动。
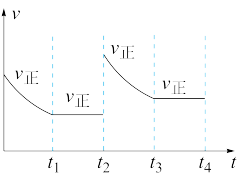
②在t2时刻,改变某一外界条件,正反应速率的变化曲线如图所示,则可能改变的条件是_______ 。
①则该反应的平衡常数K=
②在t2时刻,改变某一外界条件,正反应速率的变化曲线如图所示,则可能改变的条件是

您最近一年使用:0次



