近年来,有机-无机杂化金属卤素钙钛矿作为优良的光电材料受到广泛研究和关注,回答下列问题。
(1) Ca、Ti元素基态原子核外电子占据能级数之比为___________ ,与 Ti 处于同周期单电子数与Ti相同的元素还有___________ 种,Ca的前三级电离能数据分别为589.8 kJ/mol、1145.4 kJ/mol、4912.4 kJ/mol,第三电离能增大较多的原因是___________ 。
(2)卤族元素可与N和P元素形成多种稳定卤化物,其中NCl3分子构型为___________ , P元素可形成稳定的PCl3和PCl5,而氮元素只存在稳定的NCl3,理由是___________ 。
(3)Ti的配合物有多种。Ti(CO)6、Ti(H2O) 、TiF
、TiF 中的配体所含原子中电负性最小的是
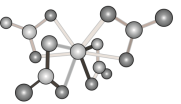
中的配体所含原子中电负性最小的是___________ ;Ti(NO3)4的球棍结构如图,Ti4+的配位数是___________ 。
(4)研究表明,TiO2通过氮掺杂反应生成TiO2-aNb,能使TiO2对可见光具有活性,反应如图所示。
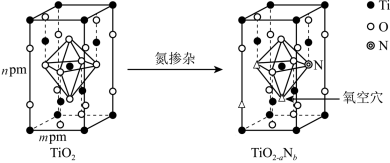
已知TiO2晶胞为长方体,设阿伏加德罗常数的值为NA,TiO2的密度为___________ g/cm3(列出计算式)。TiO2-aNb晶体中a=___________ ,b=___________ 。
(1) Ca、Ti元素基态原子核外电子占据能级数之比为
(2)卤族元素可与N和P元素形成多种稳定卤化物,其中NCl3分子构型为
(3)Ti的配合物有多种。Ti(CO)6、Ti(H2O)
 、TiF
、TiF 中的配体所含原子中电负性最小的是
中的配体所含原子中电负性最小的是
(4)研究表明,TiO2通过氮掺杂反应生成TiO2-aNb,能使TiO2对可见光具有活性,反应如图所示。

已知TiO2晶胞为长方体,设阿伏加德罗常数的值为NA,TiO2的密度为
2021·山东烟台·二模 查看更多[4]
山东省烟台市2021届高三5月二模化学试题河南省新乡名校2020-2021学年高二下学期期末联考化学试题(已下线)专题18 物质结构与性质综合-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)02 物质结构与性质综合题型集训(2) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2021-05-13 08:48:26
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】自然界中存在大量的元素,如钠、镁、铝、铁、铜、砷、锌、镍等在生活中有着广泛的应用。
(1)请写出Fe的基态原子核外电子排布式_________ ,砷属于________ 区元素。
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
则A原子的价电子排布式为______ 。
(3)锌化铜是一种金属互化物,其化学式有多种形式,如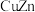 ,
,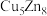 ,
,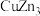 等。其中所含元素铜的第二电离能
等。其中所含元素铜的第二电离能________ (填“大于”“小于”或“等于”)锌的第二电离能。
(4)用锌还原 的盐酸溶液,经后续处理可制得绿色的晶体
的盐酸溶液,经后续处理可制得绿色的晶体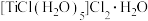 。该晶体所含元素中,电负性最大的元素是
。该晶体所含元素中,电负性最大的元素是________ ,与Ti形成配位键的配体是_____ 和________ , 该配合物中含有σ键的数目为
该配合物中含有σ键的数目为________ 。
(5) 能形成多种配离子,如
能形成多种配离子,如 ,
, 等。
等。 的空间构型为:
的空间构型为:________ ;与 互为等电子体的分子有:
互为等电子体的分子有:_______ (填分子式)。
(1)请写出Fe的基态原子核外电子排布式
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
电离能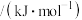 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(3)锌化铜是一种金属互化物,其化学式有多种形式,如
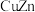 ,
,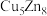 ,
,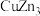 等。其中所含元素铜的第二电离能
等。其中所含元素铜的第二电离能(4)用锌还原
 的盐酸溶液,经后续处理可制得绿色的晶体
的盐酸溶液,经后续处理可制得绿色的晶体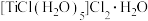 。该晶体所含元素中,电负性最大的元素是
。该晶体所含元素中,电负性最大的元素是 该配合物中含有σ键的数目为
该配合物中含有σ键的数目为(5)
 能形成多种配离子,如
能形成多种配离子,如 ,
, 等。
等。 的空间构型为:
的空间构型为: 互为等电子体的分子有:
互为等电子体的分子有:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态铜原子的电子排布式为_____ ,其基态原子的价电子运动状态有___ 种。基态磷原子的外围电子轨道表示式____
(2)磷化铜与水作用产生有毒的磷化氢(PH3),其分子空间构型______ 。
(3)磷青铜中的锡、磷两种元素电负性的大小为Sn___ P(填“>”“<”或“=”)。
(4)某磷青铜晶胞结构如图所示。
①则其化学式为_______ 。
②该晶体中距离Cu原子最近的Sn原子有___ 个。

(1)基态铜原子的电子排布式为
(2)磷化铜与水作用产生有毒的磷化氢(PH3),其分子空间构型
(3)磷青铜中的锡、磷两种元素电负性的大小为Sn
(4)某磷青铜晶胞结构如图所示。
①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】CdSnAs2是一种高迁移率的新型热电材料。回答下列问题:
(1)砷和磷为同一主族的元素,则As的价层电子排布式为___________ ,第一电离能:磷___________ 砷(填“大于”、“小于”或“等于”)。
(2)SnCl4是制备有机锡化合物的原料,染色的媒染剂,缩合剂。SnCl4中锡原子的杂化方式为___________ ,SnCl4的空间结构为___________ (用文字描述)。
(3)砷化镉(Cd,As)是一种验证三维量子霍尔效应的材料。
①砷和卤素可形成多种卤化物,AsBr3、AsCl3、AsF3的熔点由低到高的顺序为___________
②砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是___________
③Cd2+与 形成配离子[Cd(NH3)4]2+中,中心离子的配位数为
形成配离子[Cd(NH3)4]2+中,中心离子的配位数为___________ ,画出配离子的结构式___________ (不考虑立体构型)。
(4)灰锡的晶胞结构如图。已知:晶胞边长为648.9pm。晶体密度为5.75g•cm-3,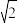 =1.414,
=1.414,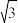 =1.732.则锡原子的半径为
=1.732.则锡原子的半径为___________ pm,锡的相对原子质量为___________ (只需写出计算表达式)。
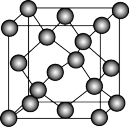
(1)砷和磷为同一主族的元素,则As的价层电子排布式为
(2)SnCl4是制备有机锡化合物的原料,染色的媒染剂,缩合剂。SnCl4中锡原子的杂化方式为
(3)砷化镉(Cd,As)是一种验证三维量子霍尔效应的材料。
①砷和卤素可形成多种卤化物,AsBr3、AsCl3、AsF3的熔点由低到高的顺序为
②砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是
③Cd2+与
 形成配离子[Cd(NH3)4]2+中,中心离子的配位数为
形成配离子[Cd(NH3)4]2+中,中心离子的配位数为(4)灰锡的晶胞结构如图。已知:晶胞边长为648.9pm。晶体密度为5.75g•cm-3,
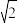 =1.414,
=1.414,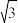 =1.732.则锡原子的半径为
=1.732.则锡原子的半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】下表为周期表的一部分,其中的编号代表对应的元素,请用元素符号回答下列问题

(1)上述元素中,属于ds区的是_______ 。(填元素符号)
(2)写出上述元素⑫正三价离子的电子排布式_______ ,有_______ 个未成对电子。
(3)③、④与⑤三种元素的第一电离能由小到大的顺序_______ (填元素符号)。
(4)对于元素⑨与⑩,不能说明⑨的金属性比⑩强的是_______。
(5)③的最高价氧化物分子中,共价键的类型有_______ (原子轨道重叠方式),其中③原子的杂化轨道类型是_______ 。
(6)④与元素①形成的最简单化合物X的沸点_______ (填“高于”或“低于”)膦( ),原因是
),原因是_______ ;X是_______ 分子(填“极性”或“非极性”)
(7)元素⑫与 可形成
可形成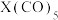 型化合物,该化合物常温下呈液态,熔点为
型化合物,该化合物常温下呈液态,熔点为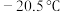 ,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)1mol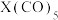 中含有σ键数目为
中含有σ键数目为_______ 。
(8)⑦单质为面心立方晶体,其晶胞参数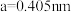 ,晶胞中⑦原子的配位数为
,晶胞中⑦原子的配位数为_______ 。列式表示⑦单质密度的计算表达式为_______  。
。

(1)上述元素中,属于ds区的是
(2)写出上述元素⑫正三价离子的电子排布式
(3)③、④与⑤三种元素的第一电离能由小到大的顺序
(4)对于元素⑨与⑩,不能说明⑨的金属性比⑩强的是_______。
A.⑨与 反应比⑩与 反应比⑩与 反应剧烈; 反应剧烈; |
| B.⑨单质的熔、沸点比⑩的低; |
| C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强; |
| D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少; |
(6)④与元素①形成的最简单化合物X的沸点
 ),原因是
),原因是(7)元素⑫与
 可形成
可形成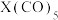 型化合物,该化合物常温下呈液态,熔点为
型化合物,该化合物常温下呈液态,熔点为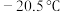 ,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于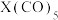 中含有σ键数目为
中含有σ键数目为(8)⑦单质为面心立方晶体,其晶胞参数
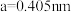 ,晶胞中⑦原子的配位数为
,晶胞中⑦原子的配位数为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的最外层电子中未成对电子数均为1,且C、F原子的核外电子数相差10,基态D、E原子的价层电子中未成对电子数分别为4、2,且原子序数相差2。
(1)六种元素中第一电离能最小的是___________ (填元素符号,下同),电负性最大的是___________ 。
(2)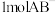 中含有π键的数目为
中含有π键的数目为___________ 。
(3)基态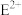 的价层电子轨道表示式为
的价层电子轨道表示式为___________ ,很多不饱和有机物在E的催化作用下可与 发生加成反应,如①
发生加成反应,如① 、②
、② 、③
、③ 、④
、④ 。其中碳原子采取
。其中碳原子采取 杂化的分子有
杂化的分子有___________ (填序号), 分子的空间结构为
分子的空间结构为___________ ,它的加成产物的熔、沸点比 的熔、沸点高,其主要原因是
的熔、沸点高,其主要原因是___________ (指明加成产物是何物质)。
(1)六种元素中第一电离能最小的是
(2)
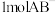 中含有π键的数目为
中含有π键的数目为(3)基态
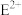 的价层电子轨道表示式为
的价层电子轨道表示式为 发生加成反应,如①
发生加成反应,如① 、②
、② 、③
、③ 、④
、④ 。其中碳原子采取
。其中碳原子采取 杂化的分子有
杂化的分子有 分子的空间结构为
分子的空间结构为 的熔、沸点高,其主要原因是
的熔、沸点高,其主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】科学家预测21世纪中叶将进入“氢能经济”时代,下列物质都是具有广阔应用前景的储氢材料。回答下列问题:
(1)Zr(锆)在元素周期表中位于第五周期,与钛同族,基态Zr的价层电子排布式为_______ 。
(2)亚氨基锂(Li2NH) 所含元素第一电离能最小的是____ ,电负性最大的是_____ (填元素符号)。
(3)咔唑( )的沸点比芴(
)的沸点比芴( )高的主要原因是
)高的主要原因是________ 。
(4)①NH3BH3 (氨硼烷,熔点104℃)与乙烷互为等电子体。NH3BH3的晶体类型为____ 。其中B的杂化类型为____ ,可通过_________ 测定该分子的立体构型。
②NH3BH3可通过环硼氨烷、CH4与H2O进行合成,键角: CH4______ H2O (填“> "或“<"),原因是________ 。
(5)MgH2晶体属四方品系,结构如图,晶胞参数a =b= 450pm, c= 30lpm,原子坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。

①Mg2+的半径为72pm,则H+的半径为______ pm (列出计算表达式)
②用NA表示阿伏加 德罗常数,MgH2晶体中氢的密度是标准状况下氢气密度的_____ 倍(列出计算表达式,氢气密度为0.089g·L-1)。
(1)Zr(锆)在元素周期表中位于第五周期,与钛同族,基态Zr的价层电子排布式为
(2)亚氨基锂(Li2NH) 所含元素第一电离能最小的是
(3)咔唑(
 )的沸点比芴(
)的沸点比芴( )高的主要原因是
)高的主要原因是(4)①NH3BH3 (氨硼烷,熔点104℃)与乙烷互为等电子体。NH3BH3的晶体类型为
②NH3BH3可通过环硼氨烷、CH4与H2O进行合成,键角: CH4
(5)MgH2晶体属四方品系,结构如图,晶胞参数a =b= 450pm, c= 30lpm,原子坐标为A(0,0,0)、B(0.305,0.305,0)、C(1,1,1)、D(0.195,0.805,0.5)。

①Mg2+的半径为72pm,则H+的半径为
②用NA表示阿伏加 德罗常数,MgH2晶体中氢的密度是标准状况下氢气密度的
您最近一年使用:0次
【推荐1】主族元素W、X、Y、Z的原子序数依次增大,W原子最外层电子数是次外层的3倍,X,Y和Z分别属于不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有二组分化合物中,由元素W、Y形成的化合物M常作为耐火材料。请回答下列问题:
(1)W原子L层电子排布式为______________ ,W3空间构形是_________ 。
(2)X单质与水反应的主要化学方程式______________________ 。
(3)化合物M的化学式_________ ,将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂酸醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有___________ ,O-C-O的键角约__________ 。
(4)X、Y、Z可形成立方晶体的化合物,其晶胞中X占有棱的中心,Y位于顶角,Z位于体心位置,则该晶体的组成为X:Y:Z=___________ 。
(5)含有元素Z的盐的焰色反应为____ 色,许多金属盐都可以发生焰色反应,其原因是___________________ 。
(1)W原子L层电子排布式为
(2)X单质与水反应的主要化学方程式
(3)化合物M的化学式
(4)X、Y、Z可形成立方晶体的化合物,其晶胞中X占有棱的中心,Y位于顶角,Z位于体心位置,则该晶体的组成为X:Y:Z=
(5)含有元素Z的盐的焰色反应为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】自然界中有许多矿石,如闪锌矿主要成分为ZnS,硫铁矿主要成分为FeS2等,它们都是化工生产中重要的化工原料。回答下列问题:
(1)FeS2中Fe2+的价层电子排布图为___________
(2)在常温下ZnS与稀硫酸作用时,有气体产生。该气体的沸点比水低的主要原因是______
(3)高温加热闪锌矿生成SO2,SO2中共价键的类型有___________ (填“σ键”或“π键”),属于___________ (填“极性”或“非极性”)分子;SO2与SO3的键角相比,键角更大的是___________ ,氧和硫形成 的空间构型为
的空间构型为___________ ,中心原子S的杂化方式为___________ 。
(4)某矿石主要成分是由A(Fe)、B、C三种元素构成的化合物,其中B、C的价电子排布分别为3d104s1、3s23p4,其晶胞结构如下图所示,该晶胞上下底面为正方形,侧面与底面垂直。

①一个晶胞中有___________ 个B,晶体中与单个B键合的C有_______ 个。
②已知:NA为阿伏加德罗常数的值,根据如图中所示的数据可得该晶体的密度是________ g∙cm-3(列出计算式)。
(1)FeS2中Fe2+的价层电子排布图为
(2)在常温下ZnS与稀硫酸作用时,有气体产生。该气体的沸点比水低的主要原因是
(3)高温加热闪锌矿生成SO2,SO2中共价键的类型有
 的空间构型为
的空间构型为(4)某矿石主要成分是由A(Fe)、B、C三种元素构成的化合物,其中B、C的价电子排布分别为3d104s1、3s23p4,其晶胞结构如下图所示,该晶胞上下底面为正方形,侧面与底面垂直。

①一个晶胞中有
②已知:NA为阿伏加德罗常数的值,根据如图中所示的数据可得该晶体的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铜镍合金曾主要用于造币,亦可用于制作仿银饰品。回答下列问题
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的配位键,提供孤电子对的成键原子是_______ (填“元素符号)。
(2)NiBr2的熔点为963℃,AIBr3的熔点为98℃,二者熔点差距大的原因是_______
(3)某铜镍合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为_______ ,每个镍原子周围距离最近的铜原子数为_______ 。
②合金的晶胞参数为anm,则合金的密度为_______ g·cm-3(用含a和NA的计算式表示)
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的配位键,提供孤电子对的成键原子是
(2)NiBr2的熔点为963℃,AIBr3的熔点为98℃,二者熔点差距大的原因是
(3)某铜镍合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为
②合金的晶胞参数为anm,则合金的密度为
您最近一年使用:0次



