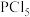X、Y、Z、P、Q为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法不正确的是


| A.X与P形成的化合物是离子化合物 |
| B.X与Z的原子均含有未成对电子 |
| C.Y与P形成的化合物YP2的分子空间构型是直线形 |
| D.Q单质含有自由移动的电子,因此可以导电 |
更新时间:2021-05-14 15:34:54
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】用NA表示阿伏加德罗常数的值,下列叙述中错误的是
| A.标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10NA |
| B.室温下,21.0 g乙烯和丁烯的混合气体含有的碳原子数目为1.5NA |
| C.等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等 |
| D.1 mol乙烷含有的共价键数目为8NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关微粒之间的作用力说法正确的是
①氯化铵受热分解,只破坏了共价键
②熔融状态能导电的化合物是离子化合物
③非金属单质之间一定存在非极性共价键
④含金属元素的化合物不一定是离子化合物
⑤由非金属元素组成的化合物一定是共价化合物
⑥离子化合物一定含离子键,也可能含极性键或非极性键
⑦H2O比H2S分子稳定,是因为H2O分子间能形成氢键
①氯化铵受热分解,只破坏了共价键
②熔融状态能导电的化合物是离子化合物
③非金属单质之间一定存在非极性共价键
④含金属元素的化合物不一定是离子化合物
⑤由非金属元素组成的化合物一定是共价化合物
⑥离子化合物一定含离子键,也可能含极性键或非极性键
⑦H2O比H2S分子稳定,是因为H2O分子间能形成氢键
| A.②④⑥ | B.②④⑥⑦ | C.①③④⑥ | D.①③⑤⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列符号表征或说法正确的是
A. 电离: H2S ⇌ 2H++S2- 电离: H2S ⇌ 2H++S2- | B. 位于元素周期表p区 位于元素周期表p区 |
| C.BF3空间结构:平面三角形 | D.KOH电子式: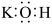 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法或化学用语的使用正确的是
| A.符号为M的能层最多容纳的电子数为32个 |
| B.Se的价层电子排布为:3d104s24p4 |
| C.Ni的简化电子排布式:[Ar]3d94s1 |
| D.构造原理呈现的能级交错源于光谱学实验 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、M、Q为5种前四周期原子序数逐渐增大的元素。X基态原子的核外电子只有1种运动状态,Y的最高能级中未成对电子数为3,Z的价层电子数是其能层数的3倍,Z与M上下相邻,Q+的价层电子轨道全充满。下列说法正确的是
| A.元素电负性:M>Q>X |
| B.X和Z可以形成既含极性键又含非极性键的极性分子 |
| C.简单氢化物的熔沸点:Y>Z>M |
D.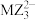 、 、 离子空间结构均为三角锥形 离子空间结构均为三角锥形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】含S元素的某钠盐a能发生如图转化。下列说法错误的是


| A.a可能为正盐,也可能为酸式盐 |
| B.c为不溶于盐酸的白色沉淀 |
C.d分子中心原子杂化轨道类型为 杂化 杂化 |
| D.反应②中还可能生成淡黄色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述中错误的个数有
①σ键可以绕键轴旋转,π键一定不能绕键轴旋转
②处于最低能量状态原子叫基态原子,1s22s22p →1s22s22p
→1s22s22p 过程中形成的是发射光谱
过程中形成的是发射光谱
③金属键和氢键都有方向性和饱和性
④NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
⑤用红外光谱能确定有机物中的官能团
⑥具有规则几何外观的固体一定是晶体
⑦电负性的大小可以作为判断元素非金属性强弱的依据
⑧分子晶体、共价晶体、金属晶体和离子晶体都有过渡型
⑨稀有气体元素都在p区
⑩利用“杯酚”可分离 和
和 利用了超分子具有自组装的特征
利用了超分子具有自组装的特征
①σ键可以绕键轴旋转,π键一定不能绕键轴旋转
②处于最低能量状态原子叫基态原子,1s22s22p
 →1s22s22p
→1s22s22p 过程中形成的是发射光谱
过程中形成的是发射光谱③金属键和氢键都有方向性和饱和性
④NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
⑤用红外光谱能确定有机物中的官能团
⑥具有规则几何外观的固体一定是晶体
⑦电负性的大小可以作为判断元素非金属性强弱的依据
⑧分子晶体、共价晶体、金属晶体和离子晶体都有过渡型
⑨稀有气体元素都在p区
⑩利用“杯酚”可分离
 和
和 利用了超分子具有自组装的特征
利用了超分子具有自组装的特征| A.5个 | B.4个 | C.3个 | D.2个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述错误的是
| A.金属键无方向性和饱和性,原子配位数较高 |
| B.晶体尽量采取紧密堆积方式,以使其变得比较稳定 |
| C.因共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原理 |
| D.金属铜和镁均以ABAB…方式堆积 |
您最近一年使用:0次
【推荐3】元素周期表中第四周期某些过渡元素(如Ti、Mn等)在生产生活中有着广泛的应用。如钛的应用越来越受到人们的关注,锰及其化合物的应用研究是前沿科学之一,下列有关说法错误的是
| A.钛比钢轻、比铝硬,是一种新的结构材料。钛硬度比铝大的原因是Ti的相对原子质量大,分子间作用更强 |
| B.第四周期元素中,基态原子的未成对电子数与钛相同的有Ni、Ge、Se |
| C.已知三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态相同 |
| D.比较Fe和Mn的第三电离能,可得I(3Fe)小于I3(Mn),原因是Mn2+的3d能级是半充满的相对稳定结构,较难失去电子 |
您最近一年使用:0次