钯是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。以硫化铜镍矿(主要含 、
、 ,还有少量的
,还有少量的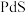 、
、 )制取钯、镍的工艺流程如下:
)制取钯、镍的工艺流程如下:

已知:“抽提”是用适当的溶剂和方法从原料中把有效成分分离出来的过程。
回答下列问题:
(1)“焙烧”需要鼓入空气使矿粉呈“沸腾”状,其目的是___________ 。
(2)“萃取铜”后的无机相中主要含有___________ (填化学式)、 。
。
(3)在实验室经过“结晶”过程获得硫酸铜晶体体的操作是___________ 、___________ 、___________ 、自然干燥。
(4)在“底渣”中加入王水(浓盐酸和浓硝酸的混合溶液)使金属 溶解生成
溶解生成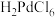 ,假设反应只产生一种污染空气的无色气体,该反应的化学方程式是
,假设反应只产生一种污染空气的无色气体,该反应的化学方程式是___________ 。该过程采用“抽提”的目的是___________ 。
(5)“抽提”后的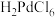 进行沉淀生成
进行沉淀生成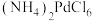 ,先加入氨后加入盐酸,先加入氨的原因是
,先加入氨后加入盐酸,先加入氨的原因是___________ 。
(6)“还原”反应中的氧化剂与还原剂的物质的量之比是___________ 。
 、
、 ,还有少量的
,还有少量的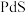 、
、 )制取钯、镍的工艺流程如下:
)制取钯、镍的工艺流程如下:
已知:“抽提”是用适当的溶剂和方法从原料中把有效成分分离出来的过程。
回答下列问题:
(1)“焙烧”需要鼓入空气使矿粉呈“沸腾”状,其目的是
(2)“萃取铜”后的无机相中主要含有
 。
。(3)在实验室经过“结晶”过程获得硫酸铜晶体体的操作是
(4)在“底渣”中加入王水(浓盐酸和浓硝酸的混合溶液)使金属
 溶解生成
溶解生成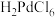 ,假设反应只产生一种污染空气的无色气体,该反应的化学方程式是
,假设反应只产生一种污染空气的无色气体,该反应的化学方程式是(5)“抽提”后的
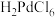 进行沉淀生成
进行沉淀生成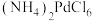 ,先加入氨后加入盐酸,先加入氨的原因是
,先加入氨后加入盐酸,先加入氨的原因是(6)“还原”反应中的氧化剂与还原剂的物质的量之比是
更新时间:2021-05-21 22:13:49
|
相似题推荐
【推荐1】铼被誉为21世纪的超级金属,被广泛应用于航空航天领域,一种由铼渣(主要成分:ReS2)提取铼的工艺流程图如下:

(1)已知铼的价电子排布与锰相似,写出75Re的价电子排布式为_______ 。
(2)第一步酸浸过程中ReS2转化为两种强酸,其中一种为高铼酸(化学式:HReO4),请写出反应的离子方程式:_______ ,根据图1所示,浸出过程中应将铼渣粉碎至_______ 目左右,根据图2所示,操作II过程中萃取液流速应选择6~8BV/h,其原因为_______ 。

(3)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是_______ 。
(4)写出由高铼酸铵热解得到Re2O7的化学方程式:_____ ,通入氧气的目的是______ 。
(5)实际生产过程中,使用氢气还原Re2O7时,氢气的用量始终要大于理论计算值,其原因是_______ 。
(6)整个工艺中可循环利用的物质有硫酸、氨气以及_______ 。
(7)已知铼的晶胞如图3所示,晶胞的参数如图4所示(a、c的单位为Å,1Å=10-10m),则金属铼的密度表达式为_______ g/cm3.(用NA表示阿伏加德罗常数的值,M表示Re的摩尔质量,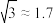 )
)


(1)已知铼的价电子排布与锰相似,写出75Re的价电子排布式为
(2)第一步酸浸过程中ReS2转化为两种强酸,其中一种为高铼酸(化学式:HReO4),请写出反应的离子方程式:

(3)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是
(4)写出由高铼酸铵热解得到Re2O7的化学方程式:
(5)实际生产过程中,使用氢气还原Re2O7时,氢气的用量始终要大于理论计算值,其原因是
(6)整个工艺中可循环利用的物质有硫酸、氨气以及
(7)已知铼的晶胞如图3所示,晶胞的参数如图4所示(a、c的单位为Å,1Å=10-10m),则金属铼的密度表达式为
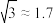 )
)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】用铬渣[含有Na2SO4及少量Na2Cr2O7、Fe2(SO4)3]为原料提取硫酸钠的工艺流程如图1所示:
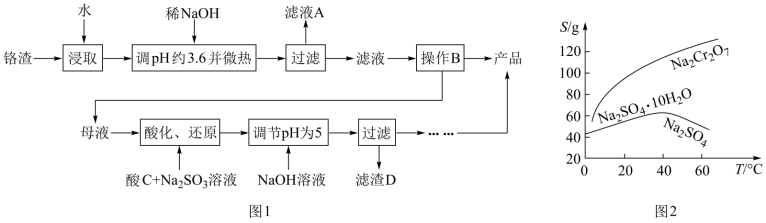
已知:常温下Fe3+、Cr3+完全沉淀时pH分别为3.6和5。
回答下列问题:
(1)为了提高铬渣的浸取率,还可以进行的操作是___ (写出一条即可)
(2)滤渣A的主要成分是___ (填化学式),工艺流程中调节pH约为3.6并微热操作中“微热”的目的是___ 。
(3)根据图2所示溶解度—温度曲线信息,通过操作B制备无水Na2SO4的实验方案是:___ ,用少量乙醇洗涤,干燥,密封保存。
(4)酸化、还原时,酸C应选___ (盐酸、稀硫酸、硝酸),选择理由是___ 。
(5)母液酸化后与Na2SO3发生反应的离子方程式为___ 。
(6)已知Cr(OH)3在溶液中存在平衡:H++CrO +H2O
+H2O Cr(OH)3(s)
Cr(OH)3(s) Cr3++3OH-加入NaOH溶液时要控制pH为5,pH不能过高的理由是
Cr3++3OH-加入NaOH溶液时要控制pH为5,pH不能过高的理由是___ 。

已知:常温下Fe3+、Cr3+完全沉淀时pH分别为3.6和5。
回答下列问题:
(1)为了提高铬渣的浸取率,还可以进行的操作是
(2)滤渣A的主要成分是
(3)根据图2所示溶解度—温度曲线信息,通过操作B制备无水Na2SO4的实验方案是:
(4)酸化、还原时,酸C应选
(5)母液酸化后与Na2SO3发生反应的离子方程式为
(6)已知Cr(OH)3在溶液中存在平衡:H++CrO
 +H2O
+H2O Cr(OH)3(s)
Cr(OH)3(s) Cr3++3OH-加入NaOH溶液时要控制pH为5,pH不能过高的理由是
Cr3++3OH-加入NaOH溶液时要控制pH为5,pH不能过高的理由是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】氧化锌工业品广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,随着工业的飞速发展,我国对氧化锌的需求量日益增加,成为国民经济建设中不可缺少的重要基础化工原料和新型材料。用工业含锌废渣(主要成分为ZnO,还含有铁、铝、铜的氧化物,Mn2+、Pb2+、Cd2+等)制取氧化锌的工艺流程如图所示:
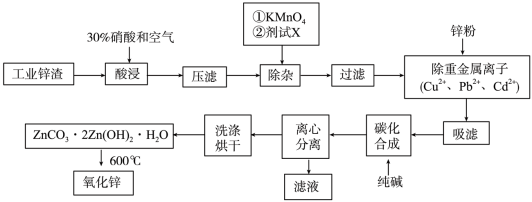
已知:相关金属离子c(Mn+)=0.1mol/L 生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)为保证锌渣酸浸的充分,先保持酸过量,且c(H+)=0.5mol/L左右。写出一种加快锌渣浸出的方法:_______________
(2)为调节溶液的pH,则试剂X为__________________ (填化学式),且调节溶液pH的范围是____________
(3)除杂时加入高锰酸钾的作用是_______________ ,发生反应的离子方程式为_____________
(4)“过滤”所得滤渣的主要成分是_____________________ (填化学式)
(5)写出“碳化合成”的化学方程式:_____________________ ;“碳化合成”过程需纯碱稍过量,请设计实验方案证明纯碱过量:_____________________

已知:相关金属离子c(Mn+)=0.1mol/L 生成氢氧化物沉淀的pH如下表所示:
| Fe3+ | Fe2+ | Al3+ | Mn2+ | Zn2+ | Cu2+ | Cd2+ | |
| 开始沉淀 | 1.5 | 6.3 | 3.4 | 8.1 | 6.2 | 6.0 | 7.4 |
| 沉淀完全 | 2.8 | 8.3 | 4.7 | 10.1 | 8.2 | 8.0 | 9.4 |
(1)为保证锌渣酸浸的充分,先保持酸过量,且c(H+)=0.5mol/L左右。写出一种加快锌渣浸出的方法:
(2)为调节溶液的pH,则试剂X为
(3)除杂时加入高锰酸钾的作用是
(4)“过滤”所得滤渣的主要成分是
(5)写出“碳化合成”的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】I.明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:

已知生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)明矾净水的原理是__________________ (用离子方程式表示)。
(2)操作Ⅱ是____________ 、______________ 、过滤、洗涤、干燥。
(3)检验滤液A中是否存在Fe2+的方法___________________ (只用一种试剂)。
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为:_______ 。
(5)调节pH=3的目的是_______________ ,滤渣2含有的物质是_____ 。
II.(6)取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中c(Pb2+)/c(Cu2+) =______ (保留三位有效数字)。[已知Ksp(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36]

已知生成氢氧化物沉淀的pH如下表所示:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀 | 3.4 | 6.3 | 1.5 |
| 完全沉淀 | 4.7 | 8.3 | 2.8 |
回答下列问题:
(1)明矾净水的原理是
(2)操作Ⅱ是
(3)检验滤液A中是否存在Fe2+的方法
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为:
(5)调节pH=3的目的是
II.(6)取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中c(Pb2+)/c(Cu2+) =
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】聚合硫酸铁铝(PFAS)是一种新型高效水处理剂。利用硫铁矿烧渣(主要成分为Fe3O4、FeO、SiO2等)为铁源、粉煤灰(主要成分为Al2O3、Fe2O3、FeO等)为铝源,制备PFAS的工艺流程如下:
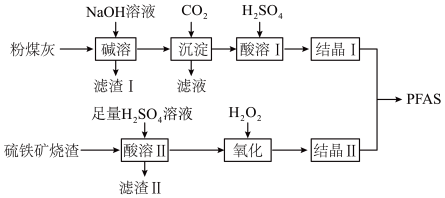
(1)“碱溶”时,Al2O3发生反应的化学方程式为_________________________ 。
(2)“酸溶Ⅱ”时,Fe3O4发生反应的离子方程式为_______________________ 。
(3)“滤渣Ⅰ”、“滤渣Ⅱ”在本流程中能加以利用的是____________________ 。
(4)“氧化”时应控制温度不超过57℃,其原因是________________________ 。
(5)“氧化”时若用酸性高锰酸钾溶液代替,发生反应的离子方程式是_______________________ 。
(6)酸度对絮凝效果和水质有显著影响。若产品中残留过多,使用时产生的不良后果是_______________________________________________

(1)“碱溶”时,Al2O3发生反应的化学方程式为
(2)“酸溶Ⅱ”时,Fe3O4发生反应的离子方程式为
(3)“滤渣Ⅰ”、“滤渣Ⅱ”在本流程中能加以利用的是
(4)“氧化”时应控制温度不超过57℃,其原因是
(5)“氧化”时若用酸性高锰酸钾溶液代替,发生反应的离子方程式是
(6)酸度对絮凝效果和水质有显著影响。若产品中残留过多,使用时产生的不良后果是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】高纯 是广泛用于电子行业的强磁性材料。
是广泛用于电子行业的强磁性材料。 为白色粉末,难溶于水和乙醇,在潮湿环境下易被氧化,温度高于100℃开始分解。实验室以
为白色粉末,难溶于水和乙醇,在潮湿环境下易被氧化,温度高于100℃开始分解。实验室以 为原料制备
为原料制备 。
。
(1)制备 溶液:
溶液:
①主要反应装置如图,缓缓通入经 稀释的
稀释的 气体,三颈烧瓶中反应的化学方程式为
气体,三颈烧瓶中反应的化学方程式为___________ 。反应过程中,为使 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有
比例一定、不改变固液投料的条件下,可采取的合理措施有___________ 。(写出一点) 可采用:
可采用: 。选择如图所示部分装置与上图装置相连制备
。选择如图所示部分装置与上图装置相连制备 溶液,应选择的装置有
溶液,应选择的装置有___________ 。
③若用空气代替 进行实验,缺点是
进行实验,缺点是___________ 。(酸性环境下 不易被氧化)
不易被氧化)
(2)制备 固体:
固体:
实验步骤:①向 溶液中边搅拌边加入饱和
溶液中边搅拌边加入饱和 溶液生成
溶液生成 沉淀,反应结束后过滤;
沉淀,反应结束后过滤;
②……;
③在70-80℃下烘干得到纯净干燥的 固体。
固体。
步骤①需控制溶液的酸碱性,若碱性过强, 粗产品中将混有
粗产品中将混有___________ (填化学式)。
步骤②的操作是洗涤沉淀和检验沉淀是否洗涤干净,则需要用到的试剂有___________ 。
 是广泛用于电子行业的强磁性材料。
是广泛用于电子行业的强磁性材料。 为白色粉末,难溶于水和乙醇,在潮湿环境下易被氧化,温度高于100℃开始分解。实验室以
为白色粉末,难溶于水和乙醇,在潮湿环境下易被氧化,温度高于100℃开始分解。实验室以 为原料制备
为原料制备 。
。(1)制备
 溶液:
溶液:①主要反应装置如图,缓缓通入经
 稀释的
稀释的 气体,三颈烧瓶中反应的化学方程式为
气体,三颈烧瓶中反应的化学方程式为 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有
比例一定、不改变固液投料的条件下,可采取的合理措施有
 可采用:
可采用: 。选择如图所示部分装置与上图装置相连制备
。选择如图所示部分装置与上图装置相连制备 溶液,应选择的装置有
溶液,应选择的装置有
|
|
|
|
|
|
| a | b | c | d | e | f |
 进行实验,缺点是
进行实验,缺点是 不易被氧化)
不易被氧化)(2)制备
 固体:
固体:实验步骤:①向
 溶液中边搅拌边加入饱和
溶液中边搅拌边加入饱和 溶液生成
溶液生成 沉淀,反应结束后过滤;
沉淀,反应结束后过滤;②……;
③在70-80℃下烘干得到纯净干燥的
 固体。
固体。步骤①需控制溶液的酸碱性,若碱性过强,
 粗产品中将混有
粗产品中将混有步骤②的操作是洗涤沉淀和检验沉淀是否洗涤干净,则需要用到的试剂有
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】一氧化二氯(Cl2O)可用作氯化剂,其部分性质如下:
实验室制备原理:2Na2CO3+H2O+2Cl2 2NaCl+2NaHCO3+Cl2O。
2NaCl+2NaHCO3+Cl2O。
现用如图所示装置设计实验制备少量Cl2O,并探究相关物质的性质。
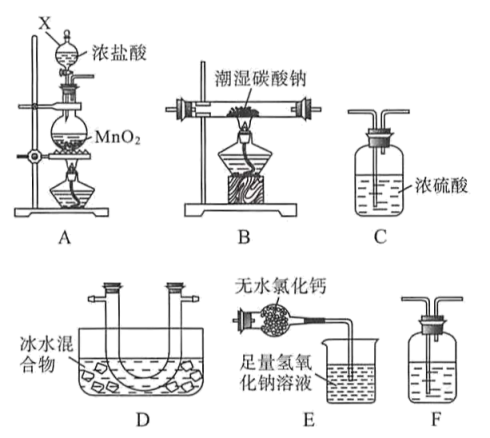
(1)装置A中仪器X的名称为___ 。
(2)若气体从左至右流动,则装置的连接顺序是A、___ (每个装置限用一次)。
(3)装置F中盛装试剂的名称为___ 。
(4)装置A中发生反应的离子方程式为___ 。
(5)装置D的作用为___ 。
(6)装置E中发生的主要反应的离子方程式为___ 。
(7)当装置D中收集到适量液态物质时停止反应,设计简单实验证明装置B中的残留固体中含有NaHCO3:___ 。
| 物理性质 | 化学性质 |
| 常温下,Cl2O是棕黄色有刺激性气味的气体,熔点:-120.6℃:沸点2.0℃ | Cl2O不稳定,接触一般有机物易爆炸;它易溶于水,同时反应生成次氯酸 |
 2NaCl+2NaHCO3+Cl2O。
2NaCl+2NaHCO3+Cl2O。现用如图所示装置设计实验制备少量Cl2O,并探究相关物质的性质。

(1)装置A中仪器X的名称为
(2)若气体从左至右流动,则装置的连接顺序是A、
(3)装置F中盛装试剂的名称为
(4)装置A中发生反应的离子方程式为
(5)装置D的作用为
(6)装置E中发生的主要反应的离子方程式为
(7)当装置D中收集到适量液态物质时停止反应,设计简单实验证明装置B中的残留固体中含有NaHCO3:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】氢化钙(CaH2)是一种常用的储氢材料,也是登山运动员常用的能源提供剂,需要密封保存,遇水反应生成氢氧化钙和氢气。某研究性学习小组模拟生产企业制取氢化钙。
【实验】
用锌粒和稀硫酸反应制得干燥、纯净的氢气,再与金属钙在加热的条件下直接化合,即可制得CaH2。
(1)下列有关该实验的说法正确的是_____________________________________ 。
a.其他条件相同时,粗锌制取氢气的速率比纯锌快
b.加热时,必须通入氮气作为保护气,以防止空气的干扰
c.可以用浓硫酸或碱石灰对H2进行干燥除杂
d.开始实验时,应先通入H2,后给金属钙加热
e.停止实验时,应先停止通入H2,后停止加热
【提出假设】
(2)由于实验中操作不当,金属钙或氢化钙都可能被氧化;该小组甲同学对反应后的固体产物成分提出如下假设:
假设1:含有Ca和CaH2;
假设2:含有CaH2和CaO;
假设3:含有__________________ 。
【设计实验方案,验证假设】
(3)定性实验用化学方法鉴别Ca与CaH2,请设计实验完成下表中内容。
(4)定量实验测定Ca和CaH2混合物中CaH2的质量分数。
①取m1 g样品与水完全反应,利用如图装置测定生成的气体体积时,在________ 时进行收集(填字母)。
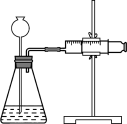
a.刚开始有气泡
b.气泡连续均匀
c.气体经过验纯后,再收集
②如果装置气密性良好,操作正确,乙同学认为:由于液体加入,导致气体的体积测定_____________ (填“偏高”“偏低”或“无影响”),则计算出氢化钙的质量分数_____________ (填“偏高”“偏低”或“无影响”)。
【反思与交流】
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是氢化钙是固体,携带方便。既然金属钙与水反应也能生成氢气,为什么还要将金属钙制备成氢化钙呢?你的观点是_______________________________________________________________________________________________________________ 。
【实验】
用锌粒和稀硫酸反应制得干燥、纯净的氢气,再与金属钙在加热的条件下直接化合,即可制得CaH2。
(1)下列有关该实验的说法正确的是
a.其他条件相同时,粗锌制取氢气的速率比纯锌快
b.加热时,必须通入氮气作为保护气,以防止空气的干扰
c.可以用浓硫酸或碱石灰对H2进行干燥除杂
d.开始实验时,应先通入H2,后给金属钙加热
e.停止实验时,应先停止通入H2,后停止加热
【提出假设】
(2)由于实验中操作不当,金属钙或氢化钙都可能被氧化;该小组甲同学对反应后的固体产物成分提出如下假设:
假设1:含有Ca和CaH2;
假设2:含有CaH2和CaO;
假设3:含有
【设计实验方案,验证假设】
(3)定性实验用化学方法鉴别Ca与CaH2,请设计实验完成下表中内容。
| 实验步骤 | 预期现象和结论 |
| 取少量固体样品, |
①取m1 g样品与水完全反应,利用如图装置测定生成的气体体积时,在

a.刚开始有气泡
b.气泡连续均匀
c.气体经过验纯后,再收集
②如果装置气密性良好,操作正确,乙同学认为:由于液体加入,导致气体的体积测定
【反思与交流】
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是氢化钙是固体,携带方便。既然金属钙与水反应也能生成氢气,为什么还要将金属钙制备成氢化钙呢?你的观点是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】冰晶石(Na3AlF6)微溶于水,可用作助熔剂、遮光剂等。以硅石(SiO2)和萤石(CaF2)为原料制备冰晶石的一种流程如图:

已知:无水氟硅酸(H2SiF6)为易溶于水、不稳定的强酸;滤渣2的主要成分为Na2SiF6。回答下列问题:
(1)反应I进行前硅石和萤石需预先研磨,目的是_____ 。
(2)常温下,滤渣1中CaSO4的溶度积常数Ksp=9×10-6,则其在水中的溶解度约为__ g•(100gH2O)-1 (溶液密度取作1g•mL-3)。
(3)滤液1中主要溶质的化学式为___ 。
(4)“反应Ⅲ”不能在陶瓷器皿中进行的原因为__ ;硅石的用途有___ (答出1点即可)。
(5)“反应Ⅳ”的化学方程式为__ ;滤液2经浓缩后可返回__ 工序循环利用。
(6)测定产品纯度:准确称量mg产品,加入高氯酸充分转化后,加入稍过量EDTA络合Al3+;过量的EDTA用cmol•L-1Pb(NO3)2标准溶液滴定,达到滴定终点时消耗标准液体积为V1mL;向滴定后溶液中加入NH4F形成AlF 同时释放出EDTA,继续用相同Pb(NO3)2标准溶液滴定,消耗标准液体积为V2mL。
同时释放出EDTA,继续用相同Pb(NO3)2标准溶液滴定,消耗标准液体积为V2mL。
(已知:EDTA与Al3+、Pb2+反应的物质的量之比均为1:1,杂质不参加反应。)
则产品中冰晶石的质量分数为__ 。

已知:无水氟硅酸(H2SiF6)为易溶于水、不稳定的强酸;滤渣2的主要成分为Na2SiF6。回答下列问题:
(1)反应I进行前硅石和萤石需预先研磨,目的是
(2)常温下,滤渣1中CaSO4的溶度积常数Ksp=9×10-6,则其在水中的溶解度约为
(3)滤液1中主要溶质的化学式为
(4)“反应Ⅲ”不能在陶瓷器皿中进行的原因为
(5)“反应Ⅳ”的化学方程式为
(6)测定产品纯度:准确称量mg产品,加入高氯酸充分转化后,加入稍过量EDTA络合Al3+;过量的EDTA用cmol•L-1Pb(NO3)2标准溶液滴定,达到滴定终点时消耗标准液体积为V1mL;向滴定后溶液中加入NH4F形成AlF
 同时释放出EDTA,继续用相同Pb(NO3)2标准溶液滴定,消耗标准液体积为V2mL。
同时释放出EDTA,继续用相同Pb(NO3)2标准溶液滴定,消耗标准液体积为V2mL。(已知:EDTA与Al3+、Pb2+反应的物质的量之比均为1:1,杂质不参加反应。)
则产品中冰晶石的质量分数为
您最近一年使用:0次









