碘主要用于制药物、染料和碘化合物等,海带、紫菜等藻类植物中富含碘元素。实验室中从海带中提取碘的流程如图。
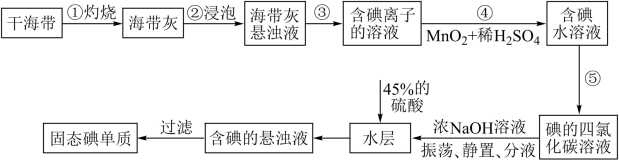
已知:碘元素在海带中以碘化物的形式存在;碘单质与NaOH浓溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O
回答下列问题:
(1)“灼烧”时,应将干海带放在___________________ (填仪器名称) 进行加热。
(2)步骤④发生反应的离子方程式为__________________ 。
(3)“过滤”操作用到的主要玻璃仪器有________________________ 。
(4)下列有关步骤⑤的叙述正确的是_________ (填序号)。
a.用到的主要玻璃仪器是分液漏斗和烧杯
b.也可选择苯或酒精作萃取剂
c.“萃取”实验中,振荡后,分液漏斗下口向上倾斜,打开活塞,使漏斗内气体放出
d.“分液”时,应打开旋塞,先将水层放出
(5)加入45%的硫酸后发生反应的离子方程式为________________________ 。
(6)该学习小组欲探究氯气、溴单质、碘单质的氧化性强弱。设计的实验操作依次为:i.向NaBr溶液中通入氯气 ii.向KI溶液中通入氯气
①若要验证氧化性Cl2>Br2>I2,你认为该小组同学还需完成的实验是______ (用离子方程式表示)。
②请用原子结构知识解释Cl2的氧化性强于I2的原因______________ 。

已知:碘元素在海带中以碘化物的形式存在;碘单质与NaOH浓溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O
回答下列问题:
(1)“灼烧”时,应将干海带放在
(2)步骤④发生反应的离子方程式为
(3)“过滤”操作用到的主要玻璃仪器有
(4)下列有关步骤⑤的叙述正确的是
a.用到的主要玻璃仪器是分液漏斗和烧杯
b.也可选择苯或酒精作萃取剂
c.“萃取”实验中,振荡后,分液漏斗下口向上倾斜,打开活塞,使漏斗内气体放出
d.“分液”时,应打开旋塞,先将水层放出
(5)加入45%的硫酸后发生反应的离子方程式为
(6)该学习小组欲探究氯气、溴单质、碘单质的氧化性强弱。设计的实验操作依次为:i.向NaBr溶液中通入氯气 ii.向KI溶液中通入氯气
①若要验证氧化性Cl2>Br2>I2,你认为该小组同学还需完成的实验是
②请用原子结构知识解释Cl2的氧化性强于I2的原因
20-21高一下·山东德州·期中 查看更多[3]
山东德州齐河县第一中学2020-2021学年高一下学期期中化学试题(已下线)专题11 开发利用金属矿物和海水资源【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)(已下线)期末综合检测卷03【综合检测】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)
更新时间:2021-05-24 06:38:04
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】浩瀚的海洋约占地球表面积的71%,它是一个巨大的宝藏。海水中水储量约为1.3×1018吨,约占地球上总水量的97%。
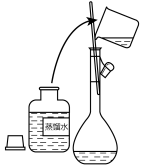
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有_______ (选填必要序号)。
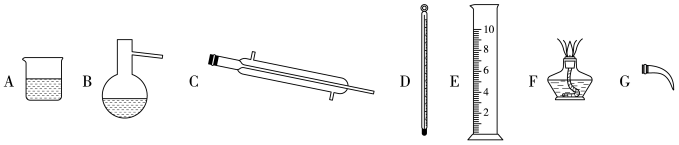
(2)某苦卤水中主要含有Mg2+、 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量_______ 试剂,过滤,_______ 析晶。所得晶体中含有少量KCl杂质,简述实验检验其中Cl-的实验操作与现象_______ 。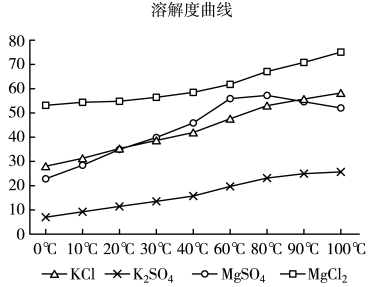
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为_______ 。
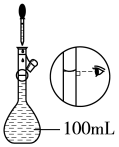
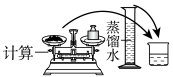
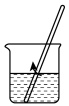
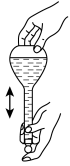
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序_______ (填数字序号)。
(5)溶解了CO2的水可以溶解自然界中的碳酸钙,产生含 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式_______ 。
(6)海水中含有大量矿物质,你认为海水中会富含石油吗?_______ (填“会”或“不会”)。
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有

(2)某苦卤水中主要含有Mg2+、
 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序
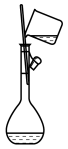 |  |  |  |  |  |
① | ② | ③ | ④ | ⑤ | ⑥ |
 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式(6)海水中含有大量矿物质,你认为海水中会富含石油吗?
您最近一年使用:0次
【推荐2】研究物质的组成和性质时,首先要将该物质从混合物中分离出来,并加以提纯。
Ⅰ.
(1)乙二醇和丙三醇是两种重要的有机溶剂,它们的性质如下表所示:
现有一瓶乙二醇和丙三醇的混合物,则将其相互分离的最佳方法是___________(填序号)。
Ⅱ.分离提纯的实验方法同样适用于工业生产。已知某工厂的工业废水中含有大量的FeSO4、较多的Cu2+,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜,请根据流程图完成回收碗酸亚铁和铜的简单实验方案并回答下列问题:

(2)操作②的名称为___________ 。
(3)试剂⑤化学式为___________ ,加入试剂⑤后反应的化学方程式为___________ 。
(4)将④和⑧混合的目的是___________ 。
(5)操作⑨为蒸发浓缩、___________ ,过程中需要用到的玻璃仪器除烧杯、漏斗、酒精灯外,还有___________ 。写出该仪器在操作⑨过程中的两个作用___________ 。
Ⅰ.
(1)乙二醇和丙三醇是两种重要的有机溶剂,它们的性质如下表所示:
| 物质 | 分子式 | 熔点/℃ | 沸点/℃ | 密度g/mL | 溶解性 |
| 乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水酒精任意比互溶 |
| A.萃取法 | B.结晶法 | C.分液法 | D.蒸馏法 |
Ⅱ.分离提纯的实验方法同样适用于工业生产。已知某工厂的工业废水中含有大量的FeSO4、较多的Cu2+,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜,请根据流程图完成回收碗酸亚铁和铜的简单实验方案并回答下列问题:

(2)操作②的名称为
(3)试剂⑤化学式为
(4)将④和⑧混合的目的是
(5)操作⑨为蒸发浓缩、
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某玻璃粉末的主要成分有GeO2、Al2O3和SiO2等物质。下图为玻璃粉末的回收利用工艺流程:

已知:①GeO2是一种难溶于水的偏弱酸性的两性氧化物
②GeCl4的熔点为-49.5℃,沸点是84℃。
(1)焙烧时发生多个反应,写出GeO2与Na2CO3发生反应的化学方程式___________ 。
(2)为了提高含锗化合物的浸出率,除了延长浸取时间,还可采取的措施有__________ (答两条)。
(3)“滤渣”的主要成分是___________ (填化学式)。
(4)调节pH时,盐酸与硅的化合物反应的离子方程式为___________ 。
(5)“滤液”与7mol∙L−1盐酸反应生成四氯化锗,写出该反应的化学方程式_________ 。
(6)操作“X”的名称为___________ 。

已知:①GeO2是一种难溶于水的偏弱酸性的两性氧化物
②GeCl4的熔点为-49.5℃,沸点是84℃。
(1)焙烧时发生多个反应,写出GeO2与Na2CO3发生反应的化学方程式
(2)为了提高含锗化合物的浸出率,除了延长浸取时间,还可采取的措施有
(3)“滤渣”的主要成分是
(4)调节pH时,盐酸与硅的化合物反应的离子方程式为
(5)“滤液”与7mol∙L−1盐酸反应生成四氯化锗,写出该反应的化学方程式
(6)操作“X”的名称为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】甘氨酸铜[Cu( H2 NCH2COO)2]是常用的食品补铜剂,微溶于乙醇,溶于水,在水中电离程度小。实验小组在实验室中以废旧白铜(含有铜、镍及其氧化物)为原料与H2NCH2COOH反应制备甘氨酸铜,并测定产品中铜元素的含量。回答下列问题:
(1)将废旧白铜充分焙烧后,用稀硫酸溶解得CuSO4和NiSO4的混合溶液。与直接用浓硫酸加热溶解废旧白铜相比,此法的优点为_______ 。
(2)调节CuSO4和NiSO4混合溶液的pH,抽滤、洗涤、干燥,制得Cu(OH)2。
①实验过程中,必须使用的玻璃仪器有_______ (填选项字 母)。
A.蒸发皿 B.烧杯 C.玻璃棒 D.冷凝管
②相比常压过滤,抽滤(减压过滤)的优点为_______ 。
③证明Cu(OH)2洗净的方法为_______ 。
(3)将新制Cu(OH)2与甘氨酸按适当比例混合,加适量蒸馏水,维持温度为65~70℃,反应一段时间;趁热过滤,向滤液中加入无水乙醇,冷却结晶、过滤、洗涤烘干,得到Cu(H2NCH2COO)2。
①控制温度为65~70℃的方式为_______ 。
②滤液中加入无水乙醇的作用为_______ 。
(4)产品中铜元素含量的测定步骤如下:
①称取m g制得的产品溶于水,加入适量硫酸酸化后,反应产物之一为H2NCH2COOH,,再加入适当过量的KI溶液(还原产物为CuI)。酸化时反应的离子方程式为_______ 。
②用c mol· L-1标准Na2S2O3溶液滴定①溶液中的I2,消耗标准Na2S2O3溶液的体积为VmL。则产品中Cu元素的质量分数为_______ (用含 m、c、V的代数式表示,已知I2+2 =2I-+
=2I-+ );下列情况对测定结果没有影响的是
);下列情况对测定结果没有影响的是_______ (填选项字母)。
A.部分I2被CuI吸附
B.少量I2与水反应
C.滴定前读取滴定管初始读数时仰视
D.滴定结束后滴定管尖嘴处出现气泡
(1)将废旧白铜充分焙烧后,用稀硫酸溶解得CuSO4和NiSO4的混合溶液。与直接用浓硫酸加热溶解废旧白铜相比,此法的优点为
(2)调节CuSO4和NiSO4混合溶液的pH,抽滤、洗涤、干燥,制得Cu(OH)2。
①实验过程中,必须使用的玻璃仪器有
A.蒸发皿 B.烧杯 C.玻璃棒 D.冷凝管
②相比常压过滤,抽滤(减压过滤)的优点为
③证明Cu(OH)2洗净的方法为
(3)将新制Cu(OH)2与甘氨酸按适当比例混合,加适量蒸馏水,维持温度为65~70℃,反应一段时间;趁热过滤,向滤液中加入无水乙醇,冷却结晶、过滤、洗涤烘干,得到Cu(H2NCH2COO)2。
①控制温度为65~70℃的方式为
②滤液中加入无水乙醇的作用为
(4)产品中铜元素含量的测定步骤如下:
①称取m g制得的产品溶于水,加入适量硫酸酸化后,反应产物之一为H2NCH2COOH,,再加入适当过量的KI溶液(还原产物为CuI)。酸化时反应的离子方程式为
②用c mol· L-1标准Na2S2O3溶液滴定①溶液中的I2,消耗标准Na2S2O3溶液的体积为VmL。则产品中Cu元素的质量分数为
 =2I-+
=2I-+ );下列情况对测定结果没有影响的是
);下列情况对测定结果没有影响的是A.部分I2被CuI吸附
B.少量I2与水反应
C.滴定前读取滴定管初始读数时仰视
D.滴定结束后滴定管尖嘴处出现气泡
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】干燥的二氧化碳和氨气反应可生成氨基甲酸铵固体,氨基甲酸铵遇水立即反应。化学方程式为:2NH3(g)+CO2(g) NH2COONH4(s) ΔH<0,在四氯化碳中通入二氧化碳和氨制备氨基甲酸铵的实验装置如下图所示,回答下列问题:
NH2COONH4(s) ΔH<0,在四氯化碳中通入二氧化碳和氨制备氨基甲酸铵的实验装置如下图所示,回答下列问题:
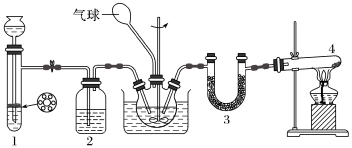
(1)装置1中用来添加液体药品的仪器名称为___________ 。
(2)装置1用来制备二氧化碳气体:将块状石灰石放置在试管中的带孔塑料板上,然后所加入稀盐酸;所发生反应的离子方程式为___________ ,装置2中所盛放的试剂为___________ 。
(3)装置4是用来制取NH3,则发生反应的化学方程式为___________ ,装置3中所盛放的试剂为___________ 。
(4)用装置1来制取气体的优点是___________ 。
(5)反应时三颈烧瓶需用冷水浴冷却,其目的是___________ 。
(6)恒温恒容条件下,发生NH2COONH4(s) 2NH3(g)+CO2(g)这一反应,向容器中加入一定量的氨基甲酸铵固体,一段时间达平衡,下列不能说明该反应达平衡状态的是
2NH3(g)+CO2(g)这一反应,向容器中加入一定量的氨基甲酸铵固体,一段时间达平衡,下列不能说明该反应达平衡状态的是___________ (填字母)。
a.容器内压强保持不变 b.氨基甲酸铵固体的质量不变
c.NH3的体积百分含量保持不变 d.混合气体的平均相对分子质量保持不变
 NH2COONH4(s) ΔH<0,在四氯化碳中通入二氧化碳和氨制备氨基甲酸铵的实验装置如下图所示,回答下列问题:
NH2COONH4(s) ΔH<0,在四氯化碳中通入二氧化碳和氨制备氨基甲酸铵的实验装置如下图所示,回答下列问题:
(1)装置1中用来添加液体药品的仪器名称为
(2)装置1用来制备二氧化碳气体:将块状石灰石放置在试管中的带孔塑料板上,然后所加入稀盐酸;所发生反应的离子方程式为
(3)装置4是用来制取NH3,则发生反应的化学方程式为
(4)用装置1来制取气体的优点是
(5)反应时三颈烧瓶需用冷水浴冷却,其目的是
(6)恒温恒容条件下,发生NH2COONH4(s)
 2NH3(g)+CO2(g)这一反应,向容器中加入一定量的氨基甲酸铵固体,一段时间达平衡,下列不能说明该反应达平衡状态的是
2NH3(g)+CO2(g)这一反应,向容器中加入一定量的氨基甲酸铵固体,一段时间达平衡,下列不能说明该反应达平衡状态的是a.容器内压强保持不变 b.氨基甲酸铵固体的质量不变
c.NH3的体积百分含量保持不变 d.混合气体的平均相对分子质量保持不变
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、纺织等工业。乙酸乙酯的实验室制法常采用如图装置:
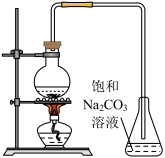
(1)烧瓶中除了乙酸和乙醇之外,还必须加的药品是___ ,其作用是___ 。
(2)能不能把饱和Na2CO3溶液换成饱和NaCl溶液?___ ,为什么?___ 。
(3)为了乙酸和乙醇回流,减少它们损失,该装置应该改进之处是:___ 。
(4)分离乙酸乙酯和饱和溶液,所需要的操作是___ 。

(1)烧瓶中除了乙酸和乙醇之外,还必须加的药品是
(2)能不能把饱和Na2CO3溶液换成饱和NaCl溶液?
(3)为了乙酸和乙醇回流,减少它们损失,该装置应该改进之处是:
(4)分离乙酸乙酯和饱和溶液,所需要的操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】亚硝酰氯(NOCl)可作为有机合成试剂。
已知:①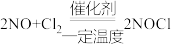
②沸点:NOCl为-6℃,Cl2为-34℃,NO为-152℃。
③NOCl易水解,能与O2反应。
某研究小组用NO和Cl2在如图所示装置中制备NOCl,并分离回收未反应的原料。
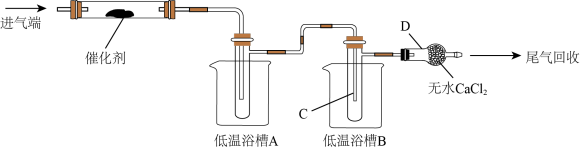
回答问题:
(1)通入Cl2和NO前先通入氩气,作用是_______ ;仪器D的名称是_______ 。
(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是_______ 。
(3)实验所需的NO可用NaNO2和FeSO4溶液在稀H2SO4中反应制得,离子反应方程式为_______ 。
(4)为分离产物和未反应的原料,低温浴槽A的温度区间应控制在_______ ,仪器C收集的物质是_______ 。
已知:①
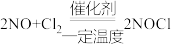
②沸点:NOCl为-6℃,Cl2为-34℃,NO为-152℃。
③NOCl易水解,能与O2反应。
某研究小组用NO和Cl2在如图所示装置中制备NOCl,并分离回收未反应的原料。
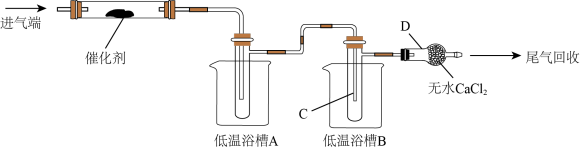
回答问题:
(1)通入Cl2和NO前先通入氩气,作用是
(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是
(3)实验所需的NO可用NaNO2和FeSO4溶液在稀H2SO4中反应制得,离子反应方程式为
(4)为分离产物和未反应的原料,低温浴槽A的温度区间应控制在
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】FeCl3是一种常用的净水剂,化学研究小组用如图装置制备无水FeCl3。已知无水FeCl3在空气中易潮解,加热易升华。结合下列制备无水FeCl3的装置,回答以下问题:

(1)A中发生反应的离子方程式为_____ 。
(2)装置接口的连接顺序为a→ → → → → → →b(用b、c……i表示)_____ 。
(3)装置B的作用_____ 。
(4)如果拆去E和F装置,可能的后果是_____ 。
(5)证明产品中存在Fe3+的操作是_____ 。

(1)A中发生反应的离子方程式为
(2)装置接口的连接顺序为a→ → → → → → →b(用b、c……i表示)
(3)装置B的作用
(4)如果拆去E和F装置,可能的后果是
(5)证明产品中存在Fe3+的操作是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
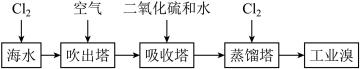
(1)溴元素在元素周期表中的位置为_______
(2)吸收塔用二氧化硫和水吸收 的离子方程式为:
的离子方程式为:_______
(3)蒸馏塔的蒸馏温度应控制在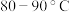 最有利于生产,原因可能为:温度过高,
最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______
(4)两次通入 的离子反应相同,其离子方程式为
的离子反应相同,其离子方程式为_______ ,通 反应后使用了空气吹出法,该方法利用了溴单质
反应后使用了空气吹出法,该方法利用了溴单质_______ 的性质。
Ⅱ.海水提镁
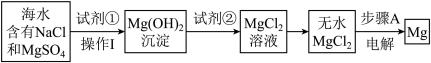
(5)工业上常用于沉淀 的廉价试剂①的俗名是
的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(6)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘
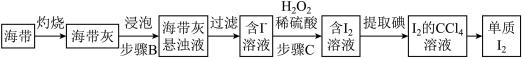
(7)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收
 的离子方程式为:
的离子方程式为:(3)蒸馏塔的蒸馏温度应控制在
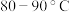 最有利于生产,原因可能为:温度过高,
最有利于生产,原因可能为:温度过高,(4)两次通入
 的离子反应相同,其离子方程式为
的离子反应相同,其离子方程式为 反应后使用了空气吹出法,该方法利用了溴单质
反应后使用了空气吹出法,该方法利用了溴单质Ⅱ.海水提镁

(5)工业上常用于沉淀
 的廉价试剂①的俗名是
的廉价试剂①的俗名是(6)步骤A的化学方程式为
Ⅲ.海带提碘

(7)步骤B需搅拌、加热煮沸的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】海洋中蕴含丰富的资源。
Ⅰ.利用海水提取淡水、溴、镁和碘的部分过程如图所示:
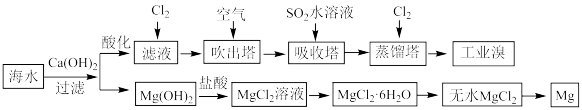
(1)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是_______ mol/L。海水淡化的方法有_______ 、离子交换法和电渗析法等。
(2)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是_______ ,然后再通入Cl2。
(3)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为_______ L(忽略Cl2的溶解)。
(4)由无水MgCl2制取Mg的化学方程式为_______ 。
Ⅱ.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:
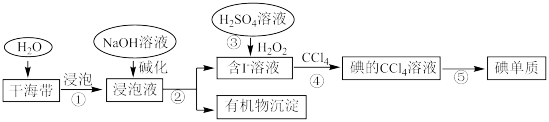
(5)步骤②的操作是_______ 。
(6)步骤③反应的离子方程式有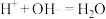 和
和_______ 。
(7)步骤④还可以选用的试剂是_______填字母序号)
Ⅰ.利用海水提取淡水、溴、镁和碘的部分过程如图所示:

(1)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO | 2560 |
(2)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是
(3)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为
(4)由无水MgCl2制取Mg的化学方程式为
Ⅱ.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:

(5)步骤②的操作是
(6)步骤③反应的离子方程式有
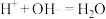 和
和(7)步骤④还可以选用的试剂是_______填字母序号)
| A.苯 | B.乙醇 | C.己烷 | D.乙酸 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】小铭同学为了从海带浸取液中提取碘,设计了如图所示实验方案:
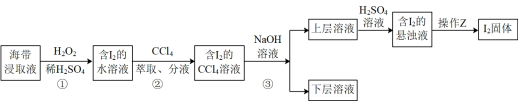
(1)实验中操作Z的名称是_______ ,在步骤②萃取操作时需用到一种重要的玻璃仪器,其名称是_______
(2)步骤①发生的离子反应方程式为_______ ;
(3)步骤②用于提取碘的物质还可以是_______
(4)步骤③可通过反萃取法得到单质碘。向含碘的CCl4溶液中加入浓 溶液,得到含
溶液,得到含 的溶液,反应的离子方程式为
的溶液,反应的离子方程式为_______ 。

(1)实验中操作Z的名称是
(2)步骤①发生的离子反应方程式为
(3)步骤②用于提取碘的物质还可以是_______
| A.乙醇 | B.苯 | C.乙酸 | D.葡萄糖 |
 溶液,得到含
溶液,得到含 的溶液,反应的离子方程式为
的溶液,反应的离子方程式为
您最近一年使用:0次




