镧( )、硼、钴及铟等形成的晶体用途非常广泛。回答下列问题:
)、硼、钴及铟等形成的晶体用途非常广泛。回答下列问题:
(1)镧是一种稀土元素,稀土元素共有_____ 种。
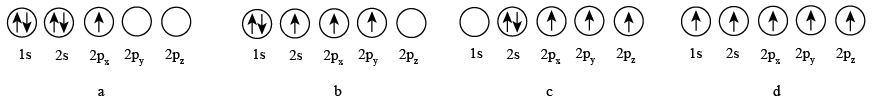
(2)下列 原子的电子排布图表示的状态中,能量最低和最高的分别为
原子的电子排布图表示的状态中,能量最低和最高的分别为____ 、____ 。(填标号)
(3)钴位于元素周期表第_______ 周期_______ 族。
(4)由 与
与 形成的化合物其晶胞结构如图(a)所示,由镧构成的晶体八面体空隙由六个硼原子构成的正八面体占据,该化合物的化学式为
形成的化合物其晶胞结构如图(a)所示,由镧构成的晶体八面体空隙由六个硼原子构成的正八面体占据,该化合物的化学式为_______ 。
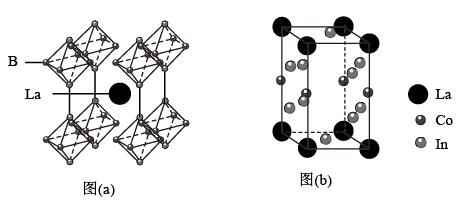
(5)由 ,
, 及
及 形成的合金的晶胞如图(b)所示,该晶胞中有
形成的合金的晶胞如图(b)所示,该晶胞中有______ 个 原子(
原子( 均位于面上),晶胞为长方体,底边边长均为
均位于面上),晶胞为长方体,底边边长均为 ,高为
,高为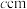 ,则该合金的密度为
,则该合金的密度为_______ (填表达式) 。
。
 )、硼、钴及铟等形成的晶体用途非常广泛。回答下列问题:
)、硼、钴及铟等形成的晶体用途非常广泛。回答下列问题:(1)镧是一种稀土元素,稀土元素共有
(2)下列
 原子的电子排布图表示的状态中,能量最低和最高的分别为
原子的电子排布图表示的状态中,能量最低和最高的分别为
(3)钴位于元素周期表第
(4)由
 与
与 形成的化合物其晶胞结构如图(a)所示,由镧构成的晶体八面体空隙由六个硼原子构成的正八面体占据,该化合物的化学式为
形成的化合物其晶胞结构如图(a)所示,由镧构成的晶体八面体空隙由六个硼原子构成的正八面体占据,该化合物的化学式为
(5)由
 ,
, 及
及 形成的合金的晶胞如图(b)所示,该晶胞中有
形成的合金的晶胞如图(b)所示,该晶胞中有 原子(
原子( 均位于面上),晶胞为长方体,底边边长均为
均位于面上),晶胞为长方体,底边边长均为 ,高为
,高为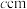 ,则该合金的密度为
,则该合金的密度为 。
。
更新时间:2021-06-09 21:59:39
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)h的原子结构示意图是_______ 。
(2)c、d、e的简单离子半径由大到小的顺序是_______ (填离子符号)。
(3)d、f、g的气态氢化物的稳定性由强到弱的顺序_______ (填化学式)。
(4)a、c和e三种元素形成化合物含_______ (填化学键类型),它的电子式为_______ 。
(5)用电子式表示由a、g两元素组成的化合物的形成过程:_______ 。
| 周期 | IA | |||||||
| 1 | a | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | |||||
| 4 | h |
(2)c、d、e的简单离子半径由大到小的顺序是
(3)d、f、g的气态氢化物的稳定性由强到弱的顺序
(4)a、c和e三种元素形成化合物含
(5)用电子式表示由a、g两元素组成的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼 的是:___________ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________ 。
(3)最高价氧化物是两性氧化物的元素是___________ ;写出它的氧化物与氢氧化钠溶液反应的离子方程式___________ 。
写出金属性最强的元素的单质与水反应的化学方程式___________ 。
(4)写出③和④形成的既含离子键又含共价键的化合物的电子式___________ 。
(5)写出⑦的单质与氢氧化钠溶液反应的离子方程式:___________ 。
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物是两性氧化物的元素是
写出金属性最强的元素的单质与水反应的化学方程式
(4)写出③和④形成的既含离子键又含共价键的化合物的电子式
(5)写出⑦的单质与氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
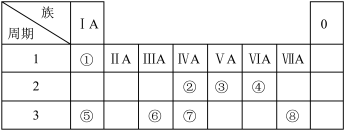
(1)地壳中含量居于第二位的元素在周期表中的位置是______ 。
(2)②的最高价氧化物的分子式为______ ;⑦的最高价氧化物对应水化物的分子式为______ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:______ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是______ (填字母)。
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为_________ 。
②铯单质与H2O反应的化学反应方程式为________ 。
③预测铯单质的还原性比钠单质的还原性________ (填“弱”或“强”)。
④下列推断正确的是________ (填字母)。
A.与铯处于同一主族的元素都是金属元素 B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱 D.铯离子的氧化性强于钾离子
(6)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为
②铯单质与H2O反应的化学反应方程式为
③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素 B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱 D.铯离子的氧化性强于钾离子
(6)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、 E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为___________ ,C的元素符号为___________ 。
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为___________
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为___________
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=___________ ;原子中能量最高的是___________ 电子。
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ ,___________ (填标号)
A.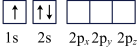 B.
B.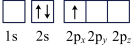 C.
C.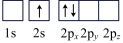 D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是___________ ,某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为___________ ,最高正价为___________ ,该原子位于元素周期表第___________ 周期第___________ 族,位于元素周期表___________ 区。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. C.
C. D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
您最近一年使用:0次
【推荐2】已知A、B、C、D、E是原子序数依次增大的短周期主族元素,F是第四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号 完成下列空白:
①元素:A___________ 、D___________ 、F___________
②B、C两种元素第一电离能的大小关系为:___________
(2)元素F的基态价层电子排布式是:___________
(3)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________
(4)F元素位于周期表的___________ 区。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用
①元素:A
②B、C两种元素第一电离能的大小关系为:
(2)元素F的基态价层电子排布式是:
(3)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
电离能( ) ) | I1 | I2 | I3 | I4 | I5 |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】已知A、B、C、D是元素周期表中前20号的4种元素,原子序数和电子层数均依次增大。A元素的某种同位素原子核内无中子,B在地壳中含量最丰富,C是常见的非金属元素且最外层有1个未成对电子,D的+2价阳离子的核外电子排布与氩原子相同。
根据以上信息,回答问题:
(1)元素符号:A_______ ;B_______ ;C_______ ;D_______ 。
(2)B原子的电子式:_______ ,C离子的结构示意图:_______ 。
(3)C原子核外共有_______ 种不同运动状态的电子,D离子的最外层电子排布式是_______ 。
(4)A、B、C三种元素组成的化合物易分解,写出其方程式:___ 。
(5)C的单质与A、B、D三种元素组成物质反应的化学方程式为:___ ,生成物中可用于杀菌消毒的是_______ (写化学式)。
根据以上信息,回答问题:
(1)元素符号:A
(2)B原子的电子式:
(3)C原子核外共有
(4)A、B、C三种元素组成的化合物易分解,写出其方程式:
(5)C的单质与A、B、D三种元素组成物质反应的化学方程式为:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】原子序数小于36的X、Y、Z、W、J、G六种元素,原子序数依次增大,其中X元素的含量在宇宙中最高,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子核外的3p能级有两个电子,G元素原子核外有6个未成对电子(用元素符号或化学式表示)。
(1)写出G元素的基态原子的价电子排布式_______ ;Y2X2分子中σ键与π键数目之比为_______ 。
(2)Y、Z、W三种元素第一电离能由大到小的顺序为_______ (用元素符号表示)。
(3)XYZ分子中Y原子轨道的杂化类型为_______ ,ZX3在水中的溶解度较大,可能的原因有ZX3能与水反应、_______ 、_______ 。
(4)Z与W可形成Z2W分子,写出一种由短周期元素形成的与该分子互为等电子体的阴离子_______ 。
(5)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为_______ 。

(1)写出G元素的基态原子的价电子排布式
(2)Y、Z、W三种元素第一电离能由大到小的顺序为
(3)XYZ分子中Y原子轨道的杂化类型为
(4)Z与W可形成Z2W分子,写出一种由短周期元素形成的与该分子互为等电子体的阴离子
(5)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】硅因为具有半导体的性质被认为是一种比较特殊的非金属元素,它的单质是硬度较大的非金属单质。铬单质为钢灰色金属,是自然界硬度最大的金属。
(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布_______ 。
(2)与硅同周期的金属第一电离能由大到小排列:_______ 。与硅同周期的非金属电负性由小到大排列:_______ 。
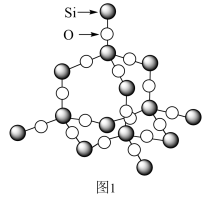
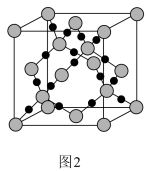
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是_______ (选填“原子晶体”、“分子晶体”或“离子晶体”,下同)。与硅同主族的元素碳的氧化物干冰是_______ 。1mol二氧化硅晶体所含有的σ键个数为_______ 。1mol的乙炔含有π键的个数为_______ 。
(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度_______ g/cm3。(列出计算式)

(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布
(2)与硅同周期的金属第一电离能由大到小排列:
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是

(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。回答下列问题:
(1)D2+的价层电子排布图为_____ 。
(2)四种元素中第一电离最小的是____ ,电负性最大的是____ 。(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
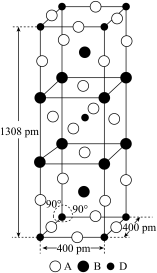
①该化合物的化学式为_____________ ;D的配位数为_______ ;
②列式计算该晶体的密度为___________ g·cm-3。(列式并计算)
(1)D2+的价层电子排布图为
(2)四种元素中第一电离最小的是
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。

①该化合物的化学式为
②列式计算该晶体的密度为
您最近一年使用:0次



