Ⅰ.下面列出了几组物质,请将物质的合适序号填写在空格上。
①金刚石和石墨②12C和13C③O2和O3④CH2=CHCH3和CH2=CH2⑤CH3CH(CH3)CH2CH3和CH3(CH2)3CH3⑥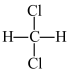 和
和
(1)互称为同系物的有___ 。
(2)互称为同分异构体的有___ 。
(3)互称为同位素的有___ 。
(4)互称为同素异形体的有___ 。
Ⅱ.(5)异丁烷的二氯代物的种数有___ 种。
Ⅲ.在一定温度下,体积为2L的恒容密闭容器中,NO2和N2O4之间发生反应2NO2(g) N2O4(g),如图所示。
N2O4(g),如图所示。
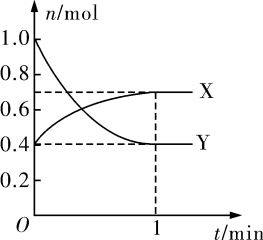
(6)曲线___ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(7)该反应达到限度时,Y的转化率是___ ,反应开始时与反应达到平衡状态时的压强之比为___ 。
(8)能说明上述反应达到化学平衡状态的依据有___ 。
A.v(X)=2v(Y)
B.容器中的压强不再发生变化
C.混合气的平均相对分子质量不变
D.容器内混合气的密度不变
E.混合气体的颜色不再改变
①金刚石和石墨②12C和13C③O2和O3④CH2=CHCH3和CH2=CH2⑤CH3CH(CH3)CH2CH3和CH3(CH2)3CH3⑥
 和
和
(1)互称为同系物的有
(2)互称为同分异构体的有
(3)互称为同位素的有
(4)互称为同素异形体的有
Ⅱ.(5)异丁烷的二氯代物的种数有
Ⅲ.在一定温度下,体积为2L的恒容密闭容器中,NO2和N2O4之间发生反应2NO2(g)
 N2O4(g),如图所示。
N2O4(g),如图所示。
(6)曲线
(7)该反应达到限度时,Y的转化率是
(8)能说明上述反应达到化学平衡状态的依据有
A.v(X)=2v(Y)
B.容器中的压强不再发生变化
C.混合气的平均相对分子质量不变
D.容器内混合气的密度不变
E.混合气体的颜色不再改变
更新时间:2021-06-22 13:05:27
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】草酸( )广泛存在于食品中,人们对其及相关产品进行了深入研究。
)广泛存在于食品中,人们对其及相关产品进行了深入研究。
(1) (s)═
(s)═  O(g)+CO(g)+C
O(g)+CO(g)+C (g)△H=+340
(g)△H=+340  在密闭容器中反应,保持温度不变,下列有关选项正确的是
在密闭容器中反应,保持温度不变,下列有关选项正确的是_____ (填序号)
A 恒容时,容器的压强不再变化,说明该反应已达到化学平衡状态
B 恒压时,容器的体积不再变化,说明该反应已达到化学平衡状态
C 气体摩尔体积不再发生变化,说明该反应已达到化学平衡状态
D 气体平均摩尔质量不再发生变化,说明该反应已达到化学平衡状态
E 气体总质量不再发生变化,说明该反应已达到化学平衡状态
(2)草酸分解所需燃料可以是CO,通过甲烷制备CO:C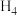 (g)+C
(g)+C (g)→2CO(g)+2
(g)→2CO(g)+2 (g)△H>O.常温下,在2L的密闭容器中通入4molC
(g)△H>O.常温下,在2L的密闭容器中通入4molC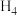 气体和6molC
气体和6molC 气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1mol•
气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1mol• 。
。
①平衡时,该反应的平均反应速率v(C )=
)=_____  。
。
②在不改变反应混合物用量的前提下,为了提高C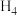 气体的转化率,可采取的措施是
气体的转化率,可采取的措施是_____ 。(答出一方面即可)
(3)草酸( )是二元弱酸,KH
)是二元弱酸,KH 溶液呈酸性。向10mL 0.01
溶液呈酸性。向10mL 0.01  的
的 溶液滴加0.01
溶液滴加0.01  KOH溶液V(mL),回答下列问题。
KOH溶液V(mL),回答下列问题。
①当V=10mL时,溶液中H 、
、 、
、 、
、 的浓度从大到小的顺序为
的浓度从大到小的顺序为_____ 。
② 当V=a mL时,溶液中离子浓度有如下关系:c( )=2c(
)=2c( )+c(H
)+c(H );当V=b mL时,溶液中离子浓度有如下关系:c(
);当V=b mL时,溶液中离子浓度有如下关系:c( )=c(
)=c( )+c(H
)+c(H )+c(
)+c( );则a
);则a_____ b(填“<”,“=”或“>”)。

(4)电解饱和草酸溶液可以制得高档香料乙醛酸( ),装置如图所示,写出复合膜电极的电极反应式
),装置如图所示,写出复合膜电极的电极反应式_____ 。
 )广泛存在于食品中,人们对其及相关产品进行了深入研究。
)广泛存在于食品中,人们对其及相关产品进行了深入研究。(1)
 (s)═
(s)═  O(g)+CO(g)+C
O(g)+CO(g)+C (g)△H=+340
(g)△H=+340  在密闭容器中反应,保持温度不变,下列有关选项正确的是
在密闭容器中反应,保持温度不变,下列有关选项正确的是A 恒容时,容器的压强不再变化,说明该反应已达到化学平衡状态
B 恒压时,容器的体积不再变化,说明该反应已达到化学平衡状态
C 气体摩尔体积不再发生变化,说明该反应已达到化学平衡状态
D 气体平均摩尔质量不再发生变化,说明该反应已达到化学平衡状态
E 气体总质量不再发生变化,说明该反应已达到化学平衡状态
(2)草酸分解所需燃料可以是CO,通过甲烷制备CO:C
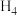 (g)+C
(g)+C (g)→2CO(g)+2
(g)→2CO(g)+2 (g)△H>O.常温下,在2L的密闭容器中通入4molC
(g)△H>O.常温下,在2L的密闭容器中通入4molC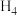 气体和6molC
气体和6molC 气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1mol•
气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1mol• 。
。①平衡时,该反应的平均反应速率v(C
 )=
)= 。
。②在不改变反应混合物用量的前提下,为了提高C
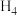 气体的转化率,可采取的措施是
气体的转化率,可采取的措施是(3)草酸(
 )是二元弱酸,KH
)是二元弱酸,KH 溶液呈酸性。向10mL 0.01
溶液呈酸性。向10mL 0.01  的
的 溶液滴加0.01
溶液滴加0.01  KOH溶液V(mL),回答下列问题。
KOH溶液V(mL),回答下列问题。①当V=10mL时,溶液中H
 、
、 、
、 、
、 的浓度从大到小的顺序为
的浓度从大到小的顺序为② 当V=a mL时,溶液中离子浓度有如下关系:c(
 )=2c(
)=2c( )+c(H
)+c(H );当V=b mL时,溶液中离子浓度有如下关系:c(
);当V=b mL时,溶液中离子浓度有如下关系:c( )=c(
)=c( )+c(H
)+c(H )+c(
)+c( );则a
);则a
(4)电解饱和草酸溶液可以制得高档香料乙醛酸(
 ),装置如图所示,写出复合膜电极的电极反应式
),装置如图所示,写出复合膜电极的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】合成氨的反应为N2+3H2 2NH3+Q。下表是某次反应时NH3的浓度变化:
2NH3+Q。下表是某次反应时NH3的浓度变化:
完成下列填空:
(1)由表中数据计算0~10 min时,用H2表示的平均反应速率为________________ 。降低温度,反应的平衡常数将______________ (填“增大”、“减小”或“不变”)。若要增大反应速率且提高H2利用率,可采取的措施有________________ 。
(2)若反应中气体混合物的密度保持不变,能否说明该反应已经达到平衡状态?并说明理由。____________________________________________________________________
(3)用右图所示装置进行有关氨气性质的实验,挤出胶头滴管中的水,打开止水夹后的实验现象是_____________ 。

(4)氨气溶于水后溶液显碱性的原因是(用方程式表示)____________________________________________ 。若在氨水中逐滴滴加盐酸,则溶液的pH将__________ (填“增大”、“减小”或“不变”);当恰好完全反应时,则c(NH4+)________ c(Cl-)(填“>”、“<”或“=”)。
 2NH3+Q。下表是某次反应时NH3的浓度变化:
2NH3+Q。下表是某次反应时NH3的浓度变化:| 时间(min) | 0 | 5 | 10 | 15 | 20 |
| c(NH3)(mol/L) | 0 | 0.30 | 0.44 | 0.50 | 0.50 |
完成下列填空:
(1)由表中数据计算0~10 min时,用H2表示的平均反应速率为
(2)若反应中气体混合物的密度保持不变,能否说明该反应已经达到平衡状态?并说明理由。
(3)用右图所示装置进行有关氨气性质的实验,挤出胶头滴管中的水,打开止水夹后的实验现象是

(4)氨气溶于水后溶液显碱性的原因是(用方程式表示)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】随着现代工业的发展,二氧化碳污染的处理成为科学研究的重点,回答下列问题:
I.有人提出利用H2还原CO2使其转化为有机化工的主要原料乙烯。
(1)查阅资料:H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为l41lkJ/mol,lmolH2O(1)转化为H2O(g)需吸收44kJ的热量。则反应6H2(g)+2CO2(g) C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
△H=___________ kJ/mol。
(2)下图是探究不同温度对CO2的转化率和催化剂的催化效率影响的示意图。
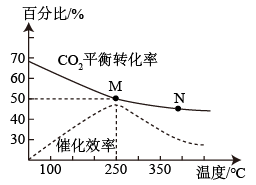
①生产中通常选用的温度最好是___________ ,理由是___________ 。
②图中表示的化学平衡常数:M___________ N(填>、=、<)
③250℃时,在2L密闭容器中分别充入6molH2和2 molCO2,到达平衡时体系中C2H4的体积分数为___________ 。
Ⅱ.CO在一定条件下,能与H2合成二甲醚:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
(1)在1L的密闭容器中分别充入2.5molH2与 bmol CO2发生反应,在不同温度下达到平衡状态时测得实验数据如下表:
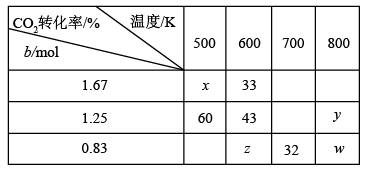
①到达平衡时若升高温度,则上述平衡___________ 方向移动(填“正反应”或“逆反应”)。
②转化率:x___________ y(填>、=、<)
(2)新型高效的二甲醚燃料电池工作时总反应式:CH3OCH3+3O2=2CO2+3H2O。
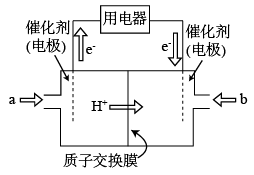
①该电池的负极是___________ (填a或b),负极电极反应式为___________ ;
②利用该电池冶铝,若制得金属铝54g理论上消耗二甲醚___________ g。
I.有人提出利用H2还原CO2使其转化为有机化工的主要原料乙烯。
(1)查阅资料:H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为l41lkJ/mol,lmolH2O(1)转化为H2O(g)需吸收44kJ的热量。则反应6H2(g)+2CO2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)△H=
(2)下图是探究不同温度对CO2的转化率和催化剂的催化效率影响的示意图。

①生产中通常选用的温度最好是
②图中表示的化学平衡常数:M
③250℃时,在2L密闭容器中分别充入6molH2和2 molCO2,到达平衡时体系中C2H4的体积分数为
Ⅱ.CO在一定条件下,能与H2合成二甲醚:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。(1)在1L的密闭容器中分别充入2.5molH2与 bmol CO2发生反应,在不同温度下达到平衡状态时测得实验数据如下表:

①到达平衡时若升高温度,则上述平衡
②转化率:x
(2)新型高效的二甲醚燃料电池工作时总反应式:CH3OCH3+3O2=2CO2+3H2O。

①该电池的负极是
②利用该电池冶铝,若制得金属铝54g理论上消耗二甲醚
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳与氢气可以合成甲醇:


一般认为可通过如下两个步骤来实现:
步骤①

步骤②

(1)
______  ,该反应在
,该反应在______ 条件下能自发进行(填“高温”、“低温”、“任意温度”)。
(2)步骤①为慢反应,下列示意图中能体现上述反应能量变化的是______(填标号)。
(3)在恒温恒压条件下,若 和
和 的物质的量之比为
的物质的量之比为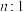 ,相应平衡体系中
,相应平衡体系中 的物质的量分数为
的物质的量分数为 ,请在下图中绘制
,请在下图中绘制 随
随 变化的示意图(不考虑副反应)
变化的示意图(不考虑副反应)____

(4)恒压条件下,按 和
和 的物质的量之比为
的物质的量之比为 投料,发生反应Ⅰ、Ⅱ。实验测得
投料,发生反应Ⅰ、Ⅱ。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如下图所示。
的选择性随温度的变化如下图所示。
Ⅰ.

Ⅱ.


已知: 的选择性
的选择性
①下列能说明体系已达到平衡状态的是______ (填序号)。
A.混合气体的密度不再变化
B.混合气体的总压强不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内每形成 键,同时形成
键,同时形成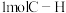 键
键
②当温度高于 时,
时, 平衡转化率随温度升高而上升的原因:
平衡转化率随温度升高而上升的原因:______ 。
③ 时,在该压强及投料比的条件下,
时,在该压强及投料比的条件下, 的转化率为
的转化率为______ (保留三位有效数字)。


一般认为可通过如下两个步骤来实现:
步骤①


步骤②


(1)

 ,该反应在
,该反应在(2)步骤①为慢反应,下列示意图中能体现上述反应能量变化的是______(填标号)。
A. | B. |
C. | D. |
(3)在恒温恒压条件下,若
 和
和 的物质的量之比为
的物质的量之比为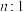 ,相应平衡体系中
,相应平衡体系中 的物质的量分数为
的物质的量分数为 ,请在下图中绘制
,请在下图中绘制 随
随 变化的示意图(不考虑副反应)
变化的示意图(不考虑副反应)
(4)恒压条件下,按
 和
和 的物质的量之比为
的物质的量之比为 投料,发生反应Ⅰ、Ⅱ。实验测得
投料,发生反应Ⅰ、Ⅱ。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如下图所示。
的选择性随温度的变化如下图所示。Ⅰ.


Ⅱ.



已知:
 的选择性
的选择性
①下列能说明体系已达到平衡状态的是
A.混合气体的密度不再变化
B.混合气体的总压强不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内每形成
 键,同时形成
键,同时形成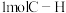 键
键②当温度高于
 时,
时, 平衡转化率随温度升高而上升的原因:
平衡转化率随温度升高而上升的原因:③
 时,在该压强及投料比的条件下,
时,在该压强及投料比的条件下, 的转化率为
的转化率为
您最近一年使用:0次
【推荐3】2019年国际非政府组织“全球碳计划”12月4日发布报告:研究显示,全球二氧化碳排放量增速趋于缓。CO2的综合利用是解决温室问题的有效途径。
(1)一种途径是将CO2转化为成为有机物实现碳循环。如:
C2H4(g)+H2O(l)=C2H5OH(l) ΔH=-44.2 kJ·mol-1
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) ΔH=+1411.0 kJ·mol-1
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) ΔH=_______ 。
(2)CO2甲烷化反应是由法国化学家PaulSabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程:

①上述过程中,产生H2反应的化学方程式为:_______ 。
②HCOOH是CO2转化为CH4的中间体:CO2 HCOOH
HCOOH CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉的用量时,CO2镍催化氢化制甲烷的两步反应中反应活化能E1
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉的用量时,CO2镍催化氢化制甲烷的两步反应中反应活化能E1_______ E2(填大于或小于)。
(3)CO2经催化加氢可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
反应II:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g)
在1 L密闭容器中冲入1 mol CO2和4 mol H2,测得平衡时有关物质的物质的量随温度变化如图所示。

T1℃时,CO2的转化率为_______ 。
(1)一种途径是将CO2转化为成为有机物实现碳循环。如:
C2H4(g)+H2O(l)=C2H5OH(l) ΔH=-44.2 kJ·mol-1
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) ΔH=+1411.0 kJ·mol-1
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) ΔH=
(2)CO2甲烷化反应是由法国化学家PaulSabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程:

①上述过程中,产生H2反应的化学方程式为:
②HCOOH是CO2转化为CH4的中间体:CO2
 HCOOH
HCOOH CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉的用量时,CO2镍催化氢化制甲烷的两步反应中反应活化能E1
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉的用量时,CO2镍催化氢化制甲烷的两步反应中反应活化能E1(3)CO2经催化加氢可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
反应II:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g)
在1 L密闭容器中冲入1 mol CO2和4 mol H2,测得平衡时有关物质的物质的量随温度变化如图所示。

T1℃时,CO2的转化率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示(石墨仅表示出其中的一层结构):
(1)C60、金刚石和石墨三者的关系是互为_____ 。
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于_____ (填“原子”或“分子”)晶体。
(3)晶体硅的结构跟金刚石相似,1mol晶体硅中含有硅﹣硅单键的数目约是_____ NA。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是_____ 。
(5)观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有_____ 个与之紧邻且等距的CO2分子;该结构单元平均占有_____ 个CO2分子。
(6)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为_____ ,每个Cs+配位数为_____ 。

(1)C60、金刚石和石墨三者的关系是互为
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于
(3)晶体硅的结构跟金刚石相似,1mol晶体硅中含有硅﹣硅单键的数目约是
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
(5)观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有
(6)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)下面列出了几组物质,请用序号填空。
①金刚石与“足球烯” C 60 ;② D 与 T ;③氧气与臭氧;④CH4 和 CH3CH2 CH3 ;⑤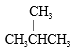 和CH3CH2CH2CH2CH3;⑥
和CH3CH2CH2CH2CH3;⑥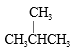 和 CH3CH2CH2CH3
和 CH3CH2CH2CH3
属于同位素的是________________ ,属于同系物的是_______________ ,属于同素异形体的是____________ ,属于同 分异构体的是______________ 。
(2)已知一定条件下,金刚石转化为石墨释放出能量,则等质量的金刚石比石墨具有的能量__________ (填“高”、“低”),故金刚石比石墨稳定性______ (填“强”、“弱”),等质量的金刚石和石墨充分燃烧均生成二 氧化碳,____________ 放出热量多。
(3)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

①B 中 Sn 极的电极反应式为____________________ ,
Sn 极附近溶液的 pH___________________ 。
②C 中总反应离子方程式为_________________ 。 比较 A、B、C 中铁被腐蚀的速率,由快到慢的顺 序是___________ 。
(4)如图是甲烷燃料电池原理示意图,回答下列问题:
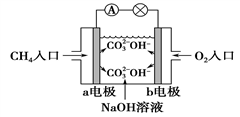
①电池的负极是____________ (填“a”或“b”)电极, 该极的电极反应是_______________________ 。
② 电池工作一段时间后电解质溶液的 pH______________ 。
①金刚石与“足球烯” C 60 ;② D 与 T ;③氧气与臭氧;④CH4 和 CH3CH2 CH3 ;⑤
 和CH3CH2CH2CH2CH3;⑥
和CH3CH2CH2CH2CH3;⑥ 和 CH3CH2CH2CH3
和 CH3CH2CH2CH3属于同位素的是
(2)已知一定条件下,金刚石转化为石墨释放出能量,则等质量的金刚石比石墨具有的能量
(3)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

①B 中 Sn 极的电极反应式为
Sn 极附近溶液的 pH
②C 中总反应离子方程式为
(4)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
② 电池工作一段时间后电解质溶液的 pH
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列填空
(1)下列选项中互为同系物的是_______ ;互为同分异构体的是_______ ;属于同种物质的是_______ 。
①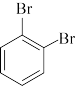 和
和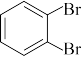 ②CH3CHO和CH3COCH3③
②CH3CHO和CH3COCH3③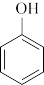 和
和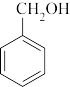 ④戊烯和环戊烷 ⑤
④戊烯和环戊烷 ⑤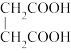 和
和 ⑥HCOOC2H5和CH3COOH
⑥HCOOC2H5和CH3COOH
(2)甲基的电子式_______ 。相对分子质量为72且沸点最低的烷烃的结构简式_______ 。
(3)有机物A是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平,请回答下列问题。
i.A的结构简式为_______ ;
ii.分子中非极性键与极性键的数目之比为_______ 。
(4)制取聚四氯乙烯的方程式如下: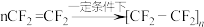 ,请指出聚四氯乙烯的单体:
,请指出聚四氯乙烯的单体:_______ 链节:_______ 。
(1)下列选项中互为同系物的是
①
 和
和 ②CH3CHO和CH3COCH3③
②CH3CHO和CH3COCH3③ 和
和 ④戊烯和环戊烷 ⑤
④戊烯和环戊烷 ⑤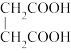 和
和 ⑥HCOOC2H5和CH3COOH
⑥HCOOC2H5和CH3COOH(2)甲基的电子式
(3)有机物A是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平,请回答下列问题。
i.A的结构简式为
ii.分子中非极性键与极性键的数目之比为
(4)制取聚四氯乙烯的方程式如下:
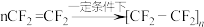 ,请指出聚四氯乙烯的单体:
,请指出聚四氯乙烯的单体:
您最近一年使用:0次

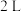 密闭容器中,800℃时反应
密闭容器中,800℃时反应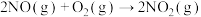 体系中,
体系中,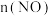 随时间的变化如表:
随时间的变化如表:
 变化曲线的是
变化曲线的是 内该反应的平均速率v=
内该反应的平均速率v=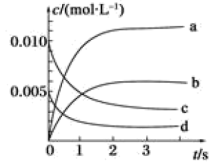
 b.容器内压强保持不变
b.容器内压强保持不变

